

2024年重庆市永川区质量监测(一模)化学试题
展开一、选择题
1.没有空气就没有生命。下列对空气的说法中错误的是
A.氧气约占空气体积的1/5
B.空气中的臭氧属于混合物
C.分离液态空气法制取氧气是物理变化
D.二氧化硫是大气主要污染物之一
2.在“一定溶质质量分数的氯化钠溶液的配制”和“粗盐中难溶性杂质的去除”实验中都必需用到的仪器是
A.玻璃棒B.漏斗
C.蒸发皿D.托盘天平
3.为探究不同物质在水中的溶解情况,某同学将少量下列物质分别加入适量水中,充分搅拌,不能得到溶液的是
A.纯碱B.小苏打C.植物油D.烧碱
4.2024年“世界水日”“中国水周”活动主题为“精打细算用好水资源,从严从细管好水资源”。下列有关水的说法正确的是
A.地球上可利用的淡水资源取之不尽,用之不竭
B.为防止水体污染,应全面禁止使用农药和化肥
C.在地表水缺乏的情况下应大量取用地下水满足人类需求
D.生活中常用煮沸的方法将硬水转化成软水
5.2021年4月16日,我国自主研发出超流氦大型低温制冷装备技术达到国际先进水平,当温度低到-271℃时,液氦就会变成超流氦。根据图中信息判断,下列说法正确的是
A.氦属于金属元素
B.He既可表示氦元素,也可表示氦分子
C.氦原子的质量是4.003g
D.氦原子化学性质活泼
6.清华大学研究人员成功研制出一种纳米纤维催化剂,有利于二氧化碳转化为甲醇,该反应的微观示意图如图所示。下列说法错误的是
A.反应中乙和丙的分子个数比为3:1
B.反应前后原子的种类不变
C.反应中甲和丙的质量比为11:8
D.甲、乙、丙、丁都属于化合物
7.一些元素在不同化合物中可显不同化合价。已知氮在某种氧化物中显+3价,这种氮的氧化物化学式是
A.NOB.N2OC.N2O3D.N2O4
8.2023年6月,重庆大学潘复生院士团队成功试制出镁合金一体化超大压铸件,是目前世界同类产品中最大的镁合金汽车压铸结构件。下列说法正确的是
A.镁合金比金属镁的硬度更大B.镁合金是金属镁的一种单质
C.镁合金比金属镁更易腐蚀D.镁合金比金属镁的密度更大
9.已知CaCl2溶液显中性。向CaCl2与盐酸混合溶液中逐滴滴加Na2CO3溶液,边滴边搅拌,用pH计测得混合溶液pH的变化如图。下列说法正确的是
①混合溶液中Ca2+个数始终保持不变
②AB段发生中和反应
③BC段有沉淀产生
④CD段表明Na2CO3溶液显碱性
A.③④B.①②③C.①③④D.①②③④
10.常温下,在能使紫色石蕊试液变红的无色溶液中大量存在的是
A.B.
C.D.
11.香椿在重庆是一种较为常见的植物,香椿叶中含有丰富的谷氨酸(C5H9NO4)。下列说法正确的是
A.谷氨酸的相对分子质量是147g
B.谷氨酸在氧气中燃烧只能生产CO2和H2O
C.谷氨酸分子中氢元素质量分数最小
D.谷氨酸是一种氧化物
12.分类方法是人类认识自然世界的重要方法。下列物质分类正确的是
A.氧化物:氧化铁、四氧化三铁、氢氧化铁
B.碱:烧碱、火碱、纯碱
C.纯净物:冰水混合物、干冰、液氮
D.酸:盐酸、硫酸、二氧化碳
13.实验是化学的基础。下列实验操作(括号内为杂质或需要检验的物质)能达到实验目的的是
A.AB.BC.CD.D
14.向AgNO3和Cu(NO3)2的混合溶液中加入一定质量的铁粉,充分反应后过滤得滤液和滤渣,下列对滤液和滤渣分析正确的是
A.若向滤液中滴加氯化钠溶液有白色沉淀,则滤渣中可能含有Cu
B.若向滤渣中滴加稀硫酸,无气泡产生,则滤液中一定没有Ag+
C.若向滤渣中滴加稀硫酸,无气泡产生,则滤液中一定有Cu2+
D.以上分析均不正确
15.已知铜在加热条件下能与浓硫酸发生如下反应:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O,将一定质量的铜片加入浓硫酸中并加热,使其充分反应(忽略SO2在溶液中的溶解以及水的蒸发)。下列图像(t表示反应时间)正确的是
A.B.C.D.
16.某纯碱样品中混有杂质氢氧化钠,取18.6g样品,向其中加入100g质量分数为a%的稀盐酸充分反应后,恰好得到只含溶质氯化钠的溶液114.2g(忽略生成的气体溶解以及水的蒸发),则a的值是
A.7.3B.14.6C.16.8D.10.6
二、填空与简答
17.化学源于生活也服务于生活。请用适当的化学用语完成下列填空:
(1)医用生理盐水溶质的化学式 。
(2)小苏打的化学式 。
(3)小麦植株矮小应施 (在氮肥、磷肥、钾肥中选择)。
(4)醋酸的化学式 。
18.书写下列化学方程式并完成基本反应类型的判断。
(1)实验室用氯酸钾制氧气 基本反应类型是 。
(2)氢氧化铝治疗胃酸过多 基本反应类型是 。
19.A~G是七种常见化合物,转化关系如图所示。常温下D是液体、C是无色气体,C、D也是植物光合作用主要原料,F是强酸,A、B、E、G含有人体含量最多的金属元素,A在高温下转化成B和C,B和G均可以作干燥剂。请回答:
(1)A的化学式是 ,G的化学式是 ;
(2)A转化成B和C的反应方程式 ;
(3)E与F能够发生中和反应,反应方程式是 。
20.碳酸锂(Li2CO3)是制备锂电池的重要原料。工业上以锂辉石精矿(主要成分为Li2O,其余成分不溶于水且不与酸反应)为原料制取Li2CO3,其主要工艺流程如下图所示:
已知:
①Li2CO3微溶于水,其溶解度随温度的升高而减小。
②酸浸槽中发生反应的化学方程式:Li2O+H2SO4=Li2SO4+H2O。
(1)写出反应器中发生反应的化学方程式: 、 ;
(2)反应器中加入的饱和Na2CO3溶液必须过量的目的是 ;
(3)洗涤槽洗涤时使用热水的目的是 。
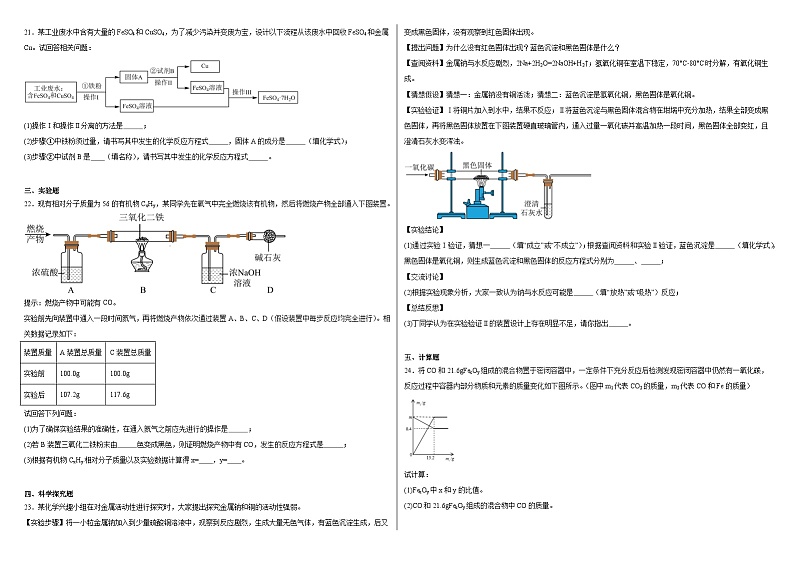
21.某工业废水中含有大量的FeSO4和CuSO4,为了减少污染并变废为宝,设计以下流程从该废水中回收FeSO4和金属Cu。试回答相关问题:
(1)操作Ⅰ和操作Ⅱ分离的方法是 ;
(2)步骤①中铁粉须过量,请书写其中发生的化学反应方程式 ,固体A的成分是 (填化学式);
(3)步骤②中试剂B是 (填名称),请书写其中发生的化学反应方程式 。
三、实验题
22.现有相对分子质量为56的有机物CxHy,某同学先在氧气中完全燃烧该有机物,然后将燃烧产物全部通入下图装置。
提示:燃烧产物中可能有CO。
实验前先向装置中通入一段时间氮气,再将燃烧产物依次通过装置A、B、C、D(假设装置中每步反应均完全进行)。相关数据记录如下:
试回答下列问题:
(1)为了确保实验结果的准确性,在通入氮气之前应先进行的操作是 ;
(2)若B装置三氧化二铁粉末由 色变成黑色,则证明燃烧产物中有CO,发生的反应方程式是 ;
(3)根据有机物CxHy相对分子质量以及实验数据计算得x= ,y= 。
四、科学探究题
23.某化学兴趣小组在对金属活动性进行探究时,大家提出探究金属钠和铜的活动性强弱。
【实验步骤】将一小粒金属钠加入到少量硫酸铜溶液中,观察到反应剧烈,生成大量无色气体,有蓝色沉淀生成,后又变成黑色固体,没有观察到红色固体出现。
【提出问题】为什么没有红色固体出现?蓝色沉淀和黑色固体是什么?
【查阅资料】金属钠与水反应剧烈,2Na+2H2O=2NaOH+H2↑;氢氧化铜在室温下稳定,70°C-80°C时分解,有氧化铜生成。
【猜想假设】猜想一:金属钠没有铜活泼;猜想二:蓝色沉淀是氢氧化铜,黑色固体是氧化铜。
【实验验证】Ⅰ将铜片加入到水中,结果不反应;Ⅱ将蓝色沉淀与黑色固体混合物在坩埚中充分加热,结果全部变成黑色固体,再将黑色固体放置在下图装置硬直玻璃管内,通入过量一氧化碳并高温加热一段时间,黑色固体全部变红,且澄清石灰水变浑浊。
【实验结论】
(1)通过实验Ⅰ验证,猜想一 (填“成立”或“不成立”);根据查阅资料和实验Ⅱ验证,蓝色沉淀是 (填化学式),黑色固体是氧化铜,则生成蓝色沉淀和黑色固体的反应方程式分别为 、 ;
【交流讨论】
(2)根据实验现象分析,大家一致认为钠与水反应可能是 (填“放热”或“吸热”)反应;
【总结反思】
(3)丁同学认为在实验验证Ⅱ的装置设计上存在明显不足,请你指出 。
五、计算题
24.将CO和21.6gFexOy组成的混合物置于密闭容器中,一定条件下充分反应后检测发现密闭容器中仍然有一氧化碳,反应过程中容器内部分物质和元素的质量变化如下图所示。(图中m1代表CO2的质量,m2代表CO和Fe的质量)
试计算:
(1)FexOy中x和y的比值。
(2)CO和21.6gFexOy组成的混合物中CO的质量。
选项
物质
目的
主要实验操作
A
NaCl溶液(CaCl2)
检验
向溶液样品中通CO2
B
CO(CO2)气体
检验
取气体样品通入澄清石灰水
C
NH3(H2O)气体
除杂
将气体通过浓硫酸
D
FeCl2溶液(CuCl2)
除杂
加入适量的锌粉,然后过滤
装置质量
A装置总质量
C装置总质量
实验前
100.0g
100.0g
实验后
107.2g
117.6g
参考答案:
1.B
2.A
3.C
4.D
5.B
6.D
7.C
8.A
9.A
10.D
11.C
12.C
13.B
14.D
15.D
16.B
17.(1)NaCl
(2)NaHCO3
(3)磷肥
(4)CH3COOH
18.(1)
分解反应
(2)
复分解反应
19.(1) CaCO3 CaCl2
(2)CaCO3CaO+CO2↑
(3)
20.(1) Li2SO4+Na2CO3=Li2CO3↓+Na2SO4 H2SO4+Na2CO3=CO2↑+H2O+Na2SO4
(2)使酸浸槽滤液中的Li+完全沉淀
(3)尽量减少Li2CO3在水中的溶解
21.(1)过滤
(2)
Fe 、Cu
(3) 稀硫酸
22.(1)检查装置气密性
(2) 红 Fe2O3+3CO2Fe+3CO2
(3) 4 8
23.(1) 不成立 Cu(OH)2 2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
(2)放热
(3)没有进行尾气处理
24.(1)
设发生反应的CO的质量为a ,根据碳元素守恒,可得关系式:CO~CO2,则
a=8.4g
根据氧元素守恒,可知FexOy中O的质量为生成的CO2质量减去反应的CO质量,即13.2g-8.4g=4.8g,则其中铁元素的质量为21.6g-4.8g=16.8g,则x :y=
答:FexOy中x和y的比值为1:1。
(2)由图可知,反应过程中一氧化碳减少,铁生成,且生成铁的质量等于开始时加入的一氧化碳的质量,则开始时混合物中一氧化碳的质量为16.8g。
答: CO和21.6gFexOy组成的混合物中CO的质量为16.8g。
重庆市永川区2024年中考化学模拟试卷附答案: 这是一份重庆市永川区2024年中考化学模拟试卷附答案,共9页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
重庆市梁平区2022-2023学年九年级上学期期末质量监测化学试题(图片版 无答案): 这是一份重庆市梁平区2022-2023学年九年级上学期期末质量监测化学试题(图片版 无答案),共6页。
重庆市永川区某校2022-2023学年九年级下学期第一次月考化学试题: 这是一份重庆市永川区某校2022-2023学年九年级下学期第一次月考化学试题,共4页。












