



江苏省徐州市第一中学2023-2024学年高二下学期4月期中考试化学试题(原卷版+解析版)
展开(满分:100分 时长:75分钟)
可能用到的分子量:Cr:52 O:16 Cu:64
单选题:本题包括13小题,每小题4分,共计52分。
1. 生活与生产都离不开化学。下列说法不正确的是
A. 用碳酸钠溶液可以洗涤油污
B. 用氯化铵和氯化锌溶液去除铁器表面的锈迹
C. 用明矾可以对自来水杀菌消毒
D. 含氟牙膏可以有效防止龋齿
2. 下列实验事实不能证明醋酸是弱电解质的是
A. 相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B. 常温下,测得0.1 ml·L-1醋酸溶液的pH=4
C. 常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4
D. 相同浓度盐酸和醋酸,醋酸溶液的导电性比盐酸的弱
3. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 水电离出的c(H+)=1.0×10-13ml/L的溶液中:Na+、、Cl-、
B. 与Al反应放出H2的溶液:Mg2+、Cu2+、、
C. 加入少量KSCN后变为红色的溶液中:K+、Mg2+、I-、
D. 无色透明的溶液中:CH3COO-、、K+、Na+
4. 已知:X(s)+2Y(g)⇌3Z(g),,下列说法错误的是
A. 增加 X 的用量,对反应速率没有影响
B. 升高反应温度,逆反应速率增大,正反应速率减小
C. 达到化学平衡状态时,Z 的浓度不再发生变化
D. 0.1 ml X 和 0.2 ml Y 充分反应生成 Z 的物质的量一定小于 0.3 ml
5. 哈伯法合成氨的反应原理为,新研制的催化剂可使该反应在常温、常压下进行。下列有关哈伯法合成氨反应的说法正确的是
A. 该反应在低温下能自发进行,则
B. 选用高效催化剂,可降低该反应的
C. 其它条件不变,增大起始的比值,可提高N2的平衡转化率
D. 提高体系的压强可增大反应的化学平衡常数
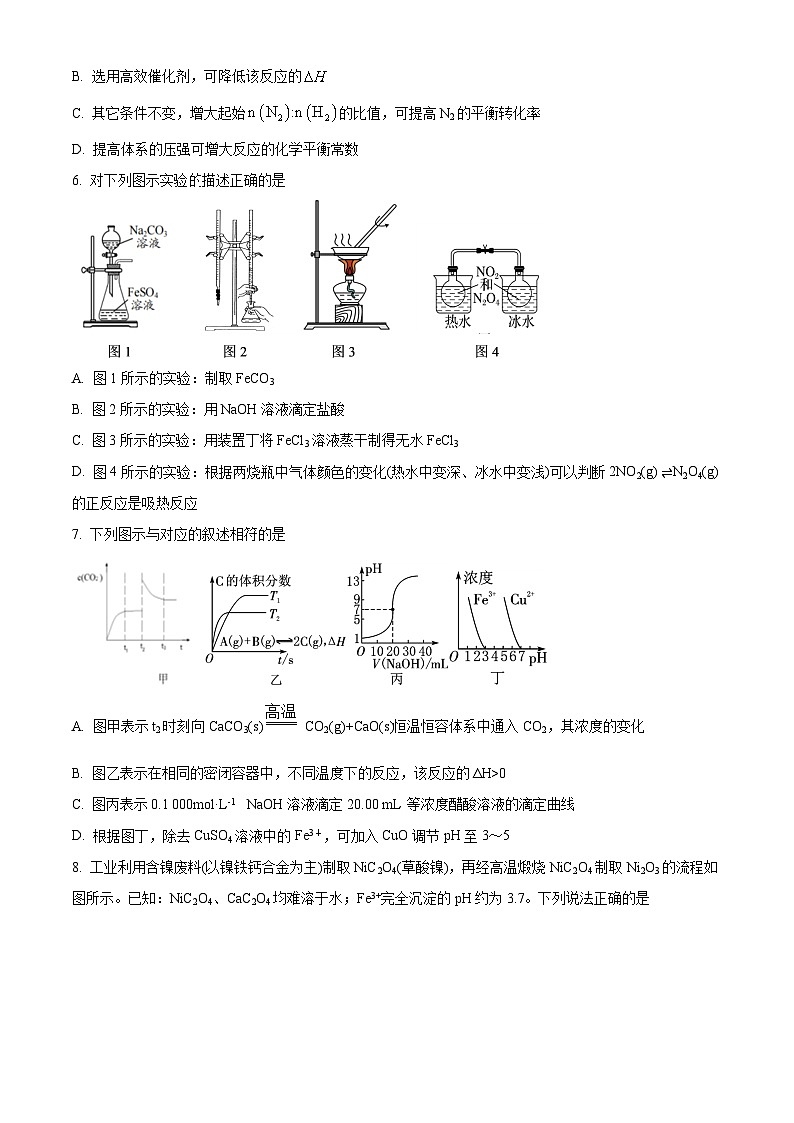
6. 对下列图示实验描述正确的是
A. 图1所示的实验:制取FeCO3
B. 图2所示的实验:用NaOH溶液滴定盐酸
C. 图3所示的实验:用装置丁将FeCl3溶液蒸干制得无水FeCl3
D. 图4所示的实验:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断2NO2(g) ⇌N2O4(g)的正反应是吸热反应
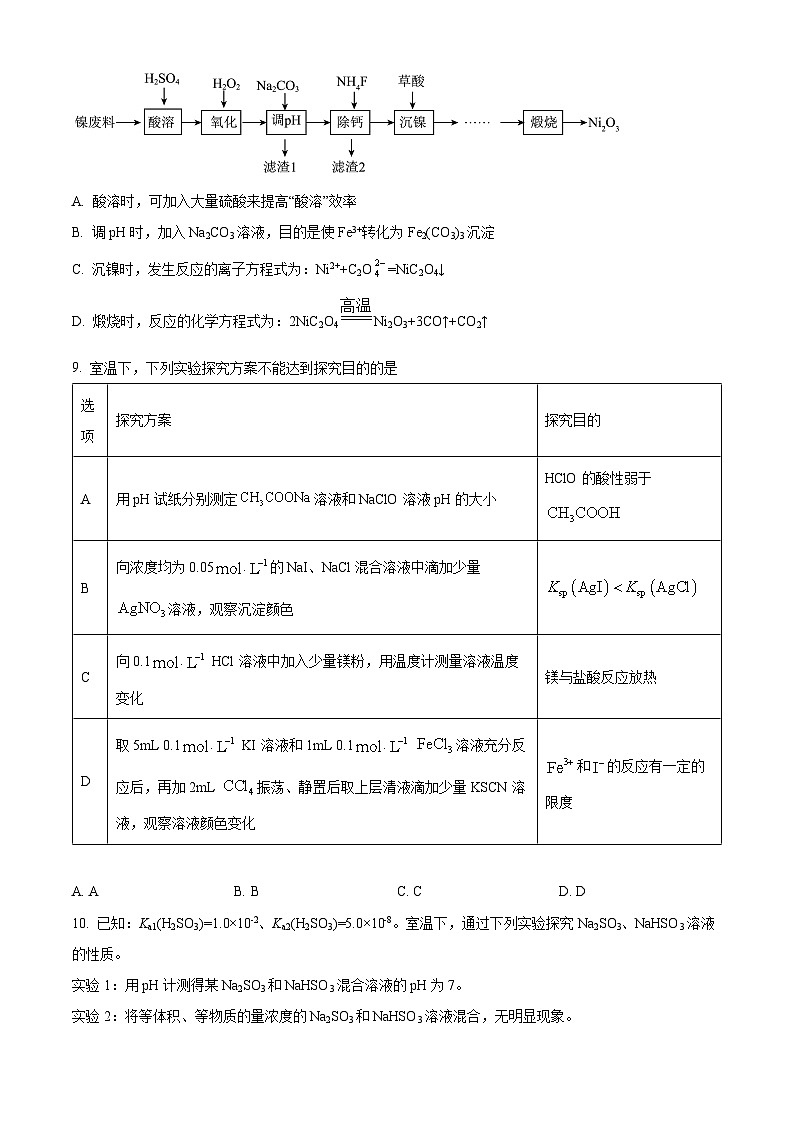
7. 下列图示与对应的叙述相符的是
A. 图甲表示t2时刻向CaCO3(s) CO2(g)+CaO(s)恒温恒容体系中通入CO2,其浓度的变化
B. 图乙表示在相同的密闭容器中,不同温度下的反应,该反应的ΔH>0
C. 图丙表示0.1 000ml·L-1 NaOH溶液滴定20.00 mL 等浓度醋酸溶液的滴定曲线
D. 根据图丁,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5
8. 工业利用含镍废料(以镍铁钙合金为主)制取NiC2O4(草酸镍),再经高温煅烧NiC2O4制取Ni2O3的流程如图所示。已知:NiC2O4、CaC2O4均难溶于水;Fe3+完全沉淀的pH约为3.7。下列说法正确的是
A. 酸溶时,可加入大量硫酸来提高“酸溶”效率
B. 调pH时,加入Na2CO3溶液,目的是使Fe3+转化为Fe2(CO3)3沉淀
C. 沉镍时,发生反应的离子方程式为:Ni2++C2O=NiC2O4↓
D. 煅烧时,反应的化学方程式为:2NiC2O4Ni2O3+3CO↑+CO2↑
9. 室温下,下列实验探究方案不能达到探究目的的是
A. AB. BC. CD. D
10. 已知:Ka1(H2SO3)=1.0×10-2、Ka2(H2SO3)=5.0×10-8。室温下,通过下列实验探究Na2SO3、NaHSO3溶液的性质。
实验1:用pH计测得某Na2SO3和NaHSO3混合溶液的pH为7。
实验2:将等体积、等物质的量浓度的Na2SO3和NaHSO3溶液混合,无明显现象。
实验3:向Na2SO3溶液中滴几滴酚酞,加水稀释,溶液红色变浅。
实验4:向NaHSO3溶液中滴加少量Ba(OH)2溶液,产生白色沉淀。
下列说法正确的是
A 实验1混合溶液中=5.0×104
B. 实验2混合后的溶液中存在:3c(Na+)=2[c()+c()+c(H2SO3)]
C. 实验3中随水的不断加入,溶液中的值逐渐变小
D. 实验4中反应的离子方程式为Ba2++=BaSO3↓
11. H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+c(HC2O)+c(C2O)=0.100ml•L﹣1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是
A. pH=2.5的溶液中:c(H2C2O4)+c(C2O)>c(HC2O)
B. c(Na+)=0.100 ml•L﹣1的溶液中:c(H+)+c(H2C2O4)=c(OH﹣)+c(C2O)
C. c(HC2O)=c(C2O)的溶液中:c(Na+)>0.100 ml•L﹣1+c(HC2O)
D. pH=7的溶液中:c(Na+)< 2c(C2O)
12. 三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。已知 。下列 说法不正确的是
A. a点无ZnS沉淀生成
B. 可用MnS除去MnCl2溶液中混有的少量ZnCl2
C. CuS和MnS共存的悬浊液中, =10-20
D. 向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c(S2-)减小
13. CO2催化加氢可合成二甲醚,发生的主要反应有:
反应Ⅰ: 2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g);ΔH1=-122.5 kJ·ml-1
反应Ⅱ: CO2(g)+H2(g) CO(g)+H2O(g);ΔH2=a kJ·ml-1
在恒压、n始(CO2)和n始(H2)=1∶3时,若仅考虑上述反应,平衡时CH3OCH3和CO的选择性及CO2的转化率随温度的变化如图中实线所示。CH3OCH3的选择性=×100%,下列说法错误的是
A. 图中曲线③表示平衡时CO2转化率随温度的变化
B. a>0
C. 平衡时H2转化率随温度的变化可能如图中虚线所示
D. 200 ℃时, 使用对反应Ⅰ选择性高的催化剂可提高CH3OCH3的生产效率
二、非选择题(本题包括3题,共48分。)
14. 以工业废铜渣(主要含CuO,还含有CuS、Fe2O3等)为原料制备CuCl,并测定其纯度。其制备过程可表示为
已知:室温下,Ksp[Fe(OH)3]=1×10-39,Ksp[Cu(OH)2]=2×10-20。
(1)焙烧。将废铜渣放在空气中加热至300℃充分焙烧,反应中CuS转化成CuO,其反应的化学方程式为_______。
(2)酸浸。将焙烧后的产物与一定浓度的硫酸溶液放入反应器中,以一定的速率搅拌进行反应。在该过程中,还可以提高铜元素浸出效率的措施是_______。
(3)除铁。酸浸后,测得溶液中c(Fe3+)=0.1 ml·L-1,c(Cu2+)=2 ml·L-1.向其中滴加NaOH溶液调节溶液pH除去Fe3+,则需调节溶液pH范围为____。已知:Fe3+完全沉淀后其浓度应小于1×10-6 ml·L-1。
(4)沉铜。除铁后,过滤,向滤液中加入Na2SO3溶液、NaCl溶液, 搅拌下充分反应,过滤,洗涤,干燥得到CuCl。
①得到CuCl沉淀的离子方程式为_______。
②相同条件下,CuCl沉淀率随的变化如下图所示。大于2.5,CuCl沉淀率几乎不变的原因_______。
15. 工业废水中常含有一定量的,利用滴定原理测定含量的方法如下:
步骤Ⅰ:量取30.00 mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤Ⅱ:加入过量的碘化钾溶液并放于暗处充分反应,其中转化为。
步骤Ⅲ:向锥形瓶中滴加几滴淀粉溶液。用滴定管量取0.1 000 ml·L-1溶液进行滴定,数据记录如下:()
(1)步骤Ⅰ量取30.00 mL废水,选择的仪器是_______。
(2)滴定达到终点时的实验现象是_______。
(3)以下操作会造成废水中含量测定值偏小的是_______(填字母)。
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D.量取溶液的滴定管用蒸馏水洗后未用标准液润洗
E.步骤Ⅱ中“放于暗处反应”,若未放于暗处
(4)步骤Ⅲ中a的读数如下图所示,则的含量为_______g·L(写出计算过程)。
16. 有效去除大气中的NOx和水体中的氮,并且转化为可利用的资源是重要课题。
(1)在微生物作用的条件下,经过两步反应被氧化成。两步反应的能量变化示意图如下:
则(aq)+2O2(g)=(aq)+2H+(aq)+H2O(l) ΔH=_______kJ·ml-1
(2)近年来,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中的c(OH-)制备纳米Cu2O备受关注,其模拟装置如图甲、乙。
①图甲中A极应于图乙中_______(请填“C”或“D”)极相连。
②该电解池的阳极反应式为_______。
③该电解池(图乙)中离子交换膜为_______(请填“阴”或“阳”)离子交换膜。
④理论上,每生产144g纳米Cu2O,需要消耗肼(N2H4)_______ml。
(3)纳米颗粒发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示。
①容易得到的副产物有CO和CH2O,其中相对较多的副产物为_______。
②上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_______(填字母)的活化能。
A.*CO+*OH→*CO+*H2O
B.*CO→*OCH
C.*OCH2→*OCH3
D.*OCH3→*CH3OH
(4)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(和NH3)。实验室中模拟氨氮处理:1 L的模拟氨氮废水(主要含),置于搅拌器上,设定反应温度为25 ℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30 min后,取液面下2 cm处清液测定氨氮质量浓度。已知:常温下,磷酸铵镁(MgNH4PO4)微溶于水;H3PO4的Ka1=6.9×10-3, Ka2=6.2×10-8 ,Ka3=4.8×10-13。
①测得反应pH对氨氮去除率的影响如图所示,当pH从7.5增至9.0的过程中,水中氨氮的去除率明显增加,原因是_______。
②当反应pH为9.0时,该沉淀法对氨氮的去除率达到最高,当pH继续增至10.0时,氨氮的去除率下降,原因是_______。选项
探究方案
探究目的
A
用pH试纸分别测定溶液和NaClO溶液pH的大小
HClO的酸性弱于
B
向浓度均为0.05的NaI、NaCl混合溶液中滴加少量溶液,观察沉淀颜色
C
向0.1 HCl溶液中加入少量镁粉,用温度计测量溶液温度变化
镁与盐酸反应放热
D
取5mL 0.1 KI溶液和1mL 0.1 溶液充分反应后,再加2mL 振荡、静置后取上层清液滴加少量KSCN溶液,观察溶液颜色变化
和的反应有一定的限度
实验次数
第一次(mL)
第二次(mL)
第三次(mL)
溶液原始读数
1.02
2.00
0.20
溶液终点读数
19.03
1999
a
贵州省贵阳市第一中学2023-2024学年高二下学期期中考试化学试题(原卷版+解析版): 这是一份贵州省贵阳市第一中学2023-2024学年高二下学期期中考试化学试题(原卷版+解析版),文件包含贵州省贵阳市第一中学2023-2024学年高二下学期期中考试化学试题原卷版docx、贵州省贵阳市第一中学2023-2024学年高二下学期期中考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共20页, 欢迎下载使用。
江苏省扬州市邗江中学2023-2024学年高一下学期期中考试化学试题(原卷版+解析版): 这是一份江苏省扬州市邗江中学2023-2024学年高一下学期期中考试化学试题(原卷版+解析版),文件包含江苏省扬州市邗江中学2023-2024学年高一下学期期中考试化学试题原卷版docx、江苏省扬州市邗江中学2023-2024学年高一下学期期中考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。
江苏省扬州市新华中学2023-2024学年高二下学期4月期中考试化学试题(原卷版+解析版): 这是一份江苏省扬州市新华中学2023-2024学年高二下学期4月期中考试化学试题(原卷版+解析版),文件包含江苏省扬州市新华中学2023-2024学年高二下学期4月期中考试化学试题原卷版docx、江苏省扬州市新华中学2023-2024学年高二下学期4月期中考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共25页, 欢迎下载使用。












