







- 主题三 第二节 弱电解质的解离平衡【中职专用】高中化学(高教版2021加工制造类) 课件+同步练习含解析卷 课件 1 次下载
- 主题三 第三节 水的离子积和溶液的pH【中职专用】高中化学(高教版2021加工制造类) 课件+同步练习含解析卷 课件 1 次下载
- 主题三 学生实验一 实验二 实验三(课件)【中职专用】高中化学(高教版2021加工制造类) 课件 1 次下载
- 主题四 第一节 常见非金属单质及其化合物【中职专用】高中化学(高教版2021加工制造类) 课件+同步练习含解析卷 课件 1 次下载
- 主题四 第二节 常见金属单质及其化合物【中职专用】高中化学(高教版2021加工制造类) 课件+同步练习含解析卷 课件 1 次下载
中职化学高教版(2021)加工制造类第五节 盐的水解课前预习ppt课件
展开1.能从原子的结构和组成出发,初步
【学习目标】1.认识强酸弱碱盐和强碱弱酸盐水解的原理及其水溶液酸碱性的判断,了解影响盐类水解的主要因素; 2.认识水解反应的本质,能结合实例书写水解反应方程式; 3.能运用离子反应、化学平衡原理解释不同盐溶液的酸碱性。
【核心素养】1.通过测定等浓度的氯化钠、醋酸钠、氯化铵和醋酸铵四种溶液的pH,培养学生现象观察与规律认知、变化观念与平衡思想等化学学科核心素养; 2.通过明矾净水原理的实践与探究,培养学生现象观察与规律认知、变化观念与平衡思想等化学学科核心素养。
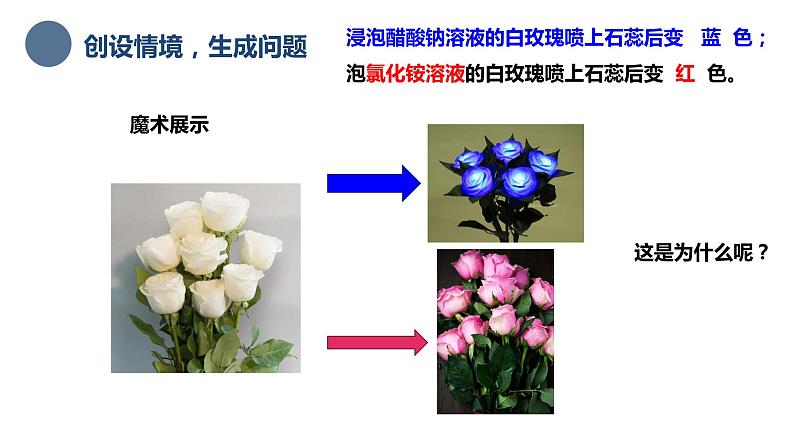
浸泡醋酸钠溶液的白玫瑰喷上石蕊后变 蓝 色;
泡氯化铵溶液的白玫瑰喷上石蕊后变 红 色。
电镀工业在清洗镀件时常用的一种碱类助洗剂是Na2CO3,即纯碱(图3-5-1)。
盐溶液呈现不同酸碱性的原因
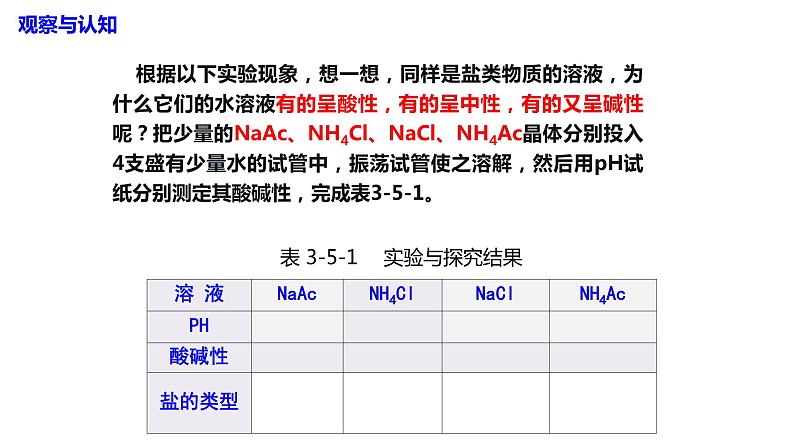
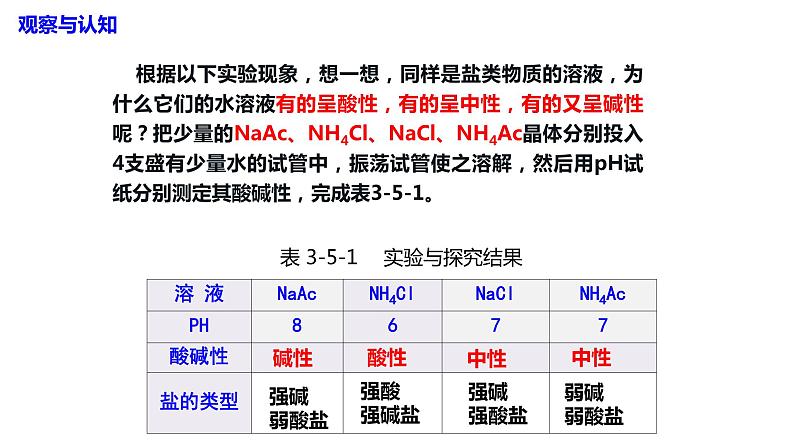
根据以下实验现象,想一想,同样是盐类物质的溶液,为什么它们的水溶液有的呈酸性,有的呈中性,有的又呈碱性呢?把少量的NaAc、NH4Cl、NaCl、NH4Ac晶体分别投入4支盛有少量水的试管中,振荡试管使之溶解,然后用pH试纸分别测定其酸碱性,完成表3-5-1。
表 3-5-1 实验与探究结果
醋酸铵NH4Ac0.1ml/L
二、盐溶液呈现不同酸碱性的原因
有弱才水解,无弱不水解,谁弱谁水解,谁强显谁性。
Na+、Cl-、H+、OH-、H2O
NH4+、H+、Cl-、OH-、NH3·H2O、H2O
H+、Na+、 OH-、 CH3COO-、H2O、 CH3COOH
1. 强碱弱酸盐的水解
NaAc是由一种强碱(NaOH)和一种弱酸(HAc)中和生成的盐,即强碱弱酸盐。它在水溶液中存在着以下解离及反应:
上述反应的总反应(结果)可表示为:
c(OH - )>c(H + ) 呈碱性
在溶液中盐的离子跟水解离出来的H+或OH-生成弱电解质的反应。
强碱弱酸盐都能水解,其水溶液都显碱性,如Na2CO3、NaHCO3与NaAc等
2. 强酸弱碱盐的水解
NH4Cl是由强酸(HCl)和弱碱(NH3·H2O)所生成的盐,即强酸弱碱盐
溶液中[H+]>[OH-],溶液显酸性
强酸弱碱盐都能水解,其水溶液都显酸性
由弱酸和弱碱所生成的弱酸弱碱盐,在水溶液中也会发生水解反应。
NH4Ac可以看成是由弱酸(HAc)和弱碱(NH3·H2O)生成的盐:
上述水解反应可用离子方程式表示为
对于NH4Ac来说,由于氨水和醋酸的解离常数几乎相等,故其溶液显中性。
明矾[又称白矾、钾矾、钾铝矾等,是一种含有结晶水的硫酸钾和硫酸铝的复盐,其化学式是KAl(SO4)2 · 12H2O],在日常生活中常用来沉淀水中的杂质,以达到净化水的目的。那么,你知道明矾为什么能净化水吗?请查阅资料,并通过交流,进一步认识水溶液中的离子反应对人们日常生产生活的作用。
水解方程式: Al3++3OH- = Al(OH)3+3H+ 明矾净水原理: 电离,水解,吸附,沉降
1. 泡沫灭火器内含高浓度NaHCO3溶液(置于铁桶内)和Al2(SO4)3溶液(置于玻璃瓶内),使用时把灭火器倒置即有泡沫状物质喷出以灭火。(1)写出灭火器倒置时反应的离子方程式;(2)泡沫灭火器内NaHCO3溶液与Al2(SO4)3溶液物质的量浓度相同,而体积比约为5:1,为什么?(3)能否用Na2CO3溶液代替NaHCO3溶液?简述理由。
Na2CO3俗称纯碱,其溶液呈碱性。
【问题一】向Na2CO3溶液中滴加酚酞溶液,可观察到什么现象?
【问题二】观察Na2CO3和NaCl两种盐的类型,分析Na2CO3呈碱性而NaCl呈中性的原因。
有弱才水解,谁弱谁水解
谁强显谁性,同强显中性
盐类水解离子方程式的书写
找“弱”离子。不生成沉淀或气体,也不会发生分解。用“ ”不写 “↑”“↓”注意:NH3·H2O、H2CO3写化学式3.多元弱酸盐分步水解,但以第一步水解为主。4.多元弱碱盐的水解,常写成一步完成。
弱离子 + 水 弱酸(或弱碱) + OH– ( 或 H+ )
“阴生阴,阳生阳”阴离子水解生成OH–,阳离子水解生成H+
1.下列离子在水溶液中不会发生水解的是( ) A. NH 4 + B. SO 4 2— C. Al 3+ D. F _
2.下列溶液能使酚酞指示剂显红色的是( ) K 2 CO 3 B. NaHSO 4 C. Na 2 SO 4 D. FeCl 3
3. 下列溶液pH小于7的是( ) A.氯化钾 B. 硫酸铜 C.硫化钠 D. 硝酸钡
中职化学第五节 盐的水解优质课ppt课件: 这是一份中职化学<a href="/hx/tb_c4035053_t3/?tag_id=26" target="_blank">第五节 盐的水解优质课ppt课件</a>,文件包含35盐的水解课件中职专用高中化学高教版2021医药卫生类pptx、35盐的水解练习中职专用高中化学高教版2021医药卫生类原卷版docx、35盐的水解练习中职专用高中化学高教版2021医药卫生类解析版docx等3份课件配套教学资源,其中PPT共24页, 欢迎下载使用。
中职化学第二节 蛋白质精品ppt课件: 这是一份中职化学<a href="/hx/tb_c4035066_t3/?tag_id=26" target="_blank">第二节 蛋白质精品ppt课件</a>,文件包含62蛋白质课件中职专用高中化学高教版2021医药卫生类pptx、62蛋白质练习中职专用高中化学高教版2021医药卫生类原卷版docx、62蛋白质练习中职专用高中化学高教版2021医药卫生类解析版docx等3份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
高教版(2021)医药卫生类第一节 糖类完整版课件ppt: 这是一份高教版(2021)医药卫生类<a href="/hx/tb_c4035065_t3/?tag_id=26" target="_blank">第一节 糖类完整版课件ppt</a>,文件包含61糖类课件中职专用高中化学高教版2021医药卫生类pptx、61糖类练习中职专用高中化学高教版2021医药卫生类原卷版docx、61糖类练习中职专用高中化学高教版2021医药卫生类解析版docx等3份课件配套教学资源,其中PPT共30页, 欢迎下载使用。












