




2024福建中考一轮复习 人教版化学 微专题二 溶解度曲线课件PPT
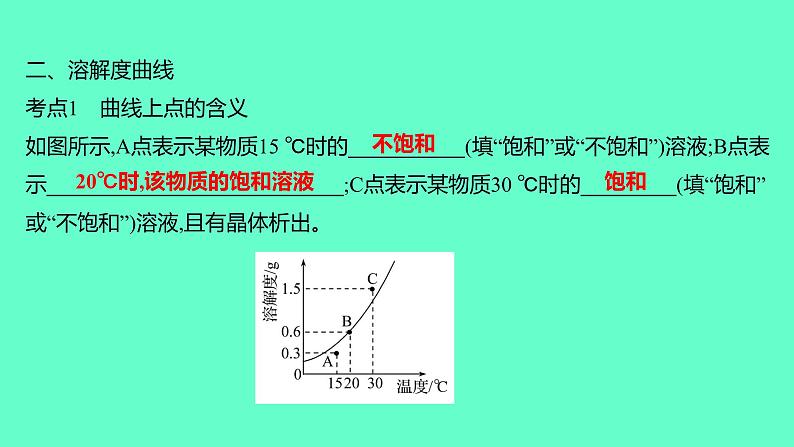
展开二、溶解度曲线考点1 曲线上点的含义如图所示,A点表示某物质15 ℃时的___________(填“饱和”或“不饱和”)溶液;B点表示____________________________;C点表示某物质30 ℃时的_________(填“饱和”或“不饱和”)溶液,且有晶体析出。
20℃时,该物质的饱和溶液
考点2 曲线上交点的含义如图所示,N点表示t3 ℃时,甲、乙两物质的溶解度_________,均为_________。 考点3 物质溶解度大小比较如图所示,t2 ℃时,甲、乙、丙溶解度大小关系为_____________。 考点4 物质溶解度随温度变化情况如图所示,甲物质的溶解度随温度的升高而_________,丙物质的溶解度随温度的升高而_________。
考点5 提纯某溶液的方法(1)当甲中混有少量的乙时,提纯甲所用的方法为________________________________。 (2)当乙中混有少量的甲时,提纯乙所用的方法为_____________。 考点6 物质溶质质量分数随温度变化情况(1)分别将甲、乙、丙三种物质的饱和溶液从t3 ℃降温到t1 ℃,所得溶液的溶质质量分数由大到小的顺序为_____________。 (2)分别将甲、乙、丙三种物质的饱和溶液从t1 ℃升温到t3 ℃,所得溶液的溶质质量分数由大到小的顺序为_____________。 (3)t3 ℃时甲、乙饱和溶液溶质的质量分数大小比较为__________。
降温结晶(或冷却热的饱和溶液)
[特别提醒] 温度改变比较物质溶质质量分数变化情况可以根据公式进行判断,改变温度,溶剂质量不变,溶解度减小有晶体析出则质量分数减小,溶解度不变或增大无晶体析出则质量分数不变。再根据图示可以比较出改变温度后不同物质溶质质量分数的大小情况。
考点7 饱和溶液和不饱和溶液的判断如图所示,t3 ℃时,150 g水中加入80 g甲物质,得到_____________。t1 ℃时,50 g水中加入25 g丙物质得到_____________。 考点8 饱和溶液和不饱和溶液的转换(1)将接近饱和的甲溶液转化为饱和溶液的方法:加溶质、降低温度、蒸发溶剂。(2)将接近饱和的丙溶液转化为饱和溶液的方法:加溶质、升高温度、蒸发溶剂。(3)t1 ℃时,将甲的不饱和溶液转化为饱和溶液的方法:_________________________。
加溶质、恒温蒸发溶剂
考点9 溶液、溶剂、溶质质量的计算(1)t2 ℃时,100 g水中溶解_______g甲恰好形成饱和溶液。 (2)t1 ℃时,配制甲、乙的相同质量的饱和溶液,所需溶剂的质量关系为__________。 (3)t3 ℃时,将等质量的甲、乙、丙三种物质分别配制成饱和溶液,所得溶液的质量大小关系为_____________。
1.如图是甲、乙两种物质的溶解度曲线,下列叙述正确的是( )A.20 ℃时,甲、乙两种物质的溶解度均为30B.40 ℃时,甲的饱和溶液中溶质的质量分数为50%C.甲、乙饱和溶液从40 ℃降温到20 ℃,析出晶体质量甲大于乙 D.将20 ℃时甲、乙饱和溶液恒温蒸发等质量的水,析出晶体质量相等
2.(2023·福州延安中学模拟)如图为MgSO4和KCl的溶解度曲线。下列说法正确的是( )A.T1 ℃时,MgSO4溶液和KCl溶液的溶质质量分数相等B.T2 ℃时,分别向100 g水中加入等质量(m)的MgSO4和KCl,搅拌后均无固体剩余,质量m应满足0
加入适量的硝酸钾(或恒温蒸发一部分的水)
4.(2023·滨州中考)如图为甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,请回答下列问题:(1)当温度为______℃时,甲物质的溶解度等于丙物质的溶解度;(2)图中A点表示乙物质在t1 ℃时的___________(填“饱和”或“不饱和”)溶液; (3)若甲中含有少量乙时,可以采用_____________(填“降温结晶”或“蒸发结晶”)的方法提纯甲;
微专题05 溶解度曲线及溶解度表分析-备战2024年中考化学一轮复习考点(人教版): 这是一份微专题05 溶解度曲线及溶解度表分析-备战2024年中考化学一轮复习考点(人教版),文件包含微专题5溶解度曲线及溶解度表分析-备战2024年中考化学一轮复习考点帮人教版原卷版docx、微专题5溶解度曲线及溶解度表分析-备战2024年中考化学一轮复习考点帮人教版解析版docx等2份试卷配套教学资源,其中试卷共26页, 欢迎下载使用。
中考化学二轮专题突破 微专题 溶解度及溶解度曲线 课件PPT: 这是一份中考化学二轮专题突破 微专题 溶解度及溶解度曲线 课件PPT,共36页。PPT课件主要包含了蒸发结晶,不饱和,物质的溶解度,t3℃时甲,甲或恒温蒸发溶剂,加溶剂,降温或增加溶剂,加溶质,乙>甲=丙,丙>乙>甲等内容,欢迎下载使用。
2024福建中考一轮复习 人教版化学 专题一 坐标曲线题课件PPT: 这是一份2024福建中考一轮复习 人教版化学 专题一 坐标曲线题课件PPT,共17页。PPT课件主要包含了专题突破·明技法,题组精练·提素能等内容,欢迎下载使用。












