




第七章 化学反应速率和化学平衡 章末综合检测卷 -备战2023年高考化学【一轮·夯实基础】复习精讲精练
展开第I卷(选择题)
一、选择题(每小题3分,共48分)
1.(2022·全国·课时练习)10mL浓度为的溶液与过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是( )
A.加入适量的的溶液B.加入适量的蒸馏水
C.加入数滴硫酸铜溶液D.加入适量的硫酸钠溶液
2.(2022·辽宁抚顺期末)T℃时,在2L的密闭容器中,气体A与气体B反应生成气体C,反应过程中A、B、C的浓度变化如图所示。则下列结论正确的是( )
A.10s时反应生成了0.4ml C
B.该反应进行到10s时,消耗了0.4ml A
C.该反应的化学方程式为
D.10s内用B表示的反应速率为
3.(2022·全国课时练习)一定温度下,在恒容反应器中发生反应,化学反应速率(k为化学反应速率常数,其数值与温度有关)。实验测得该温度下反应物浓度与化学反应速率的关系如表所示:
根据表中的测定结果,下列结论不正确的是( )
A.表中x的值为
B.化学反应速率
C.升高温度,各物质浓度不变,化学反应速率不变
D.催化剂影响k的大小
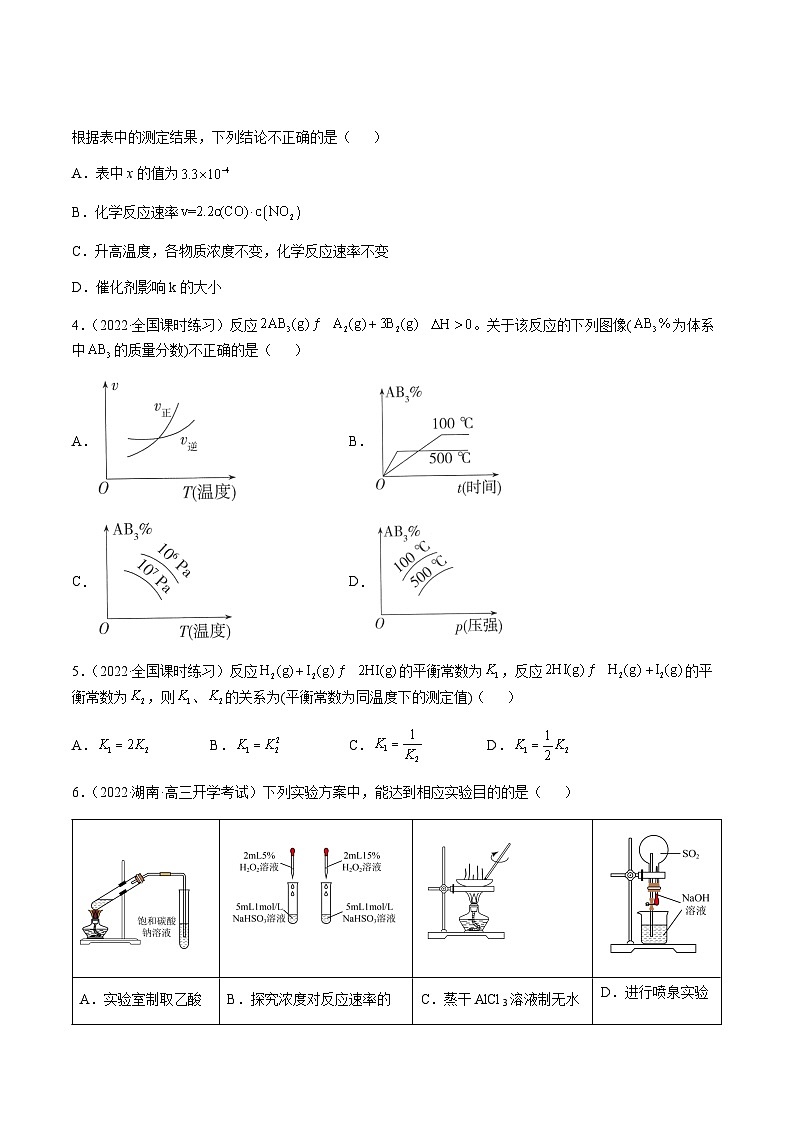
4.(2022·全国课时练习)反应 。关于该反应的下列图像(为体系中的质量分数)不正确的是( )
A.B.
C.D.
5.(2022·全国课时练习)反应的平衡常数为,反应的平衡常数为,则、的关系为(平衡常数为同温度下的测定值)( )
A.B.C.D.
6.(2022·湖南·高三开学考试)下列实验方案中,能达到相应实验目的的是( )
A.AB.BC.CD.D
7.(2022·全国课时练习)用合成甲醇()的化学方程式为,按照相同的物质的量投料,测得在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
A.温度:
B.正反应速率:、
C.平衡常数:、
D.平均摩尔质量:、
8.(2022·全国课时练习)一定温度下,向容积为2L的恒容密闭容器中通入2A和1B,发生反应,3min后达到平衡,此时A的物质的量是0.8。下列说法正确的是( )
A.0~3min内为0.1
B.当压强不变时,说明反应达到平衡状态
C.如果此时再向容器中通入少量C,平衡逆向移动,再次平衡时C的体积分数增大
D.反应达到平衡时,
9.(2022·山西·大同市第二中学校高三开学考试)化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是( )
A.AB.BC.CD.D
10.(2022·全国课时练习)一定温度下,把2.5A和2.5B混合充入容积为2L的密闭容器里,发生如下反应:,经5s反应达平衡,在此5s内C的平均反应速率为0.2,同时生成1D。下列叙述中不正确的是( )
A.反应达到平衡状态时A的转化率为60%
B.
C.若混合气体的密度不再变化,则该可逆反应达到化学平衡状态
D.反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强之比为6∶5
11.(2022·全国课时练习)将一定量纯净的氨基甲酸铵固体置于密闭真空容器中(容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:。下列各项:①;②密闭容器中压强不变;③密闭容器中混合气体的密度不变;④密闭容器中氨气的体积分数不变;⑤密闭容器中不变。能判断该反应已经达到化学平衡状态的是( )
A.②③⑤B.②③④C.①④D.全部
12.(2022·湖南阶段练习)下列在常温下不能自发进行且是熵增过程的反应为( )
A.工业合成氨的反应B.碳与二氧化碳的反应
C.碳酸氢钠与盐酸的反应D.与的反应
13.(2022·四川绵阳期末)我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。下列说法错误的是( )
A.总反应为放热反应B.第①步有C=O键断裂
C.第②步有C-C键形成D.催化剂可有效提高化学反应速率
14.(2022·重庆八中高一期末)下列关于化学反应速率或化学平衡图象的说法不正确的是( )
A.图①为反应aA(s)+2B(g)xC(g)中物质的量随时间的变化关系,则x=2
B.图②中φ可表示反应X(g)+3Y(g)2W(g) ΔH<0中X的体积分数
C.图③表示压强对可逆反应2A(g)+2B(g)C(g)+3D(g)的影响,则p甲
15.(2022·四川·乐山市教育科学研究)反应CO2(g)+H2(g)CO(g)+H2O(l)的能量变化示意图如图所示,已知H2O(g)=H2O(l) △H=-44.0kJ·ml-1,下列说法正确的是( )
A.使用催化剂后,反应能量变化曲线可能为①
B.温度升高,该反应的平衡常数减小
C.该反应的△S>0
D.CO2(g)+H2(g)CO(g)+H2O(g)是放热反应
16.(2022·河南·宝丰县第一高级中学高三阶段练习)在亚纳米金属钯(Pd)团簇作用下,过氧化氢可以直接将苯高效催化转化为苯酚,催化剂中掺杂碱金属离子可改变催化能力,反应历程如图(*表示吸附态,TS表示过渡态),下列说法错误的是( )
A.苯与H2O2反应生成苯酚是放热反应
B.反应历程中,存在反应+O*→
C.使用Pd-Na+催化剂后,每一步的产物均比使用Pd催化剂更稳定
D.其他条件相同时,使用掺杂Na+的催化剂,单位时间内可得更多苯酚产品
第II卷(非选择题)
二、非选择题(共52分)
17.(2022·全国课时练习) 的反应机理如下:
反应i:
反应ii:
其能量与反应过程的关系如图所示。
已知:对于基元反应,其速率方程为。
回答下列问题:
(1)△H1_______0(填“>”或“<”)。
(2)反应i逆反应的活化能为_______kJ/ml(用含a、b、c的代数式表示)。
(3)决定总反应速率快慢的是_______(填“反应i”或“反应ii”)。
(4)各步反应速率方程如表,其中k1、k2、k3、k4分别为v1(正)、v1(逆)、v2(正)、v2(逆)的速率常数,且仅与温度有关。
实验测得总反应的速率方程为v(正)= kc(I2)∙c(H2),则k=_______(用仅含k1、k2、k3的代数式表示)。
18.(2022·河南·宝丰县第一高级中学高三阶段练习)甲烷干重整反应可以同时转化CH4和CO2两种温室气体,并制备高附加值的合成气(H2和CO混合气体)。
(1)已知转化2ml CH4吸收386.6kJ热量,则可逆反应甲烷干重整的热化学方程式为_______________________________________,反应物总键能_________生成物总键能(填“大于”“小于”或“等于”)。
(2)T℃、压强为p时,以n(CH4):n(CO2):n(Ar)=1:1:3的投料比,在密闭容器中发生甲烷干重整反应,主要副反应为CO2(g)+H2(g)CO(g)+H2O(g)。
①反应体系中加入Ar的作用是___________________。
②CH4和CO2的平衡转化率分别是60%和80%,则H2的产率为_________,T℃下副反应的平衡常数K=______________。
(3)北京大学徐东升教授团队开发了一种甲烷干重整光催化剂—Rh/CexWO3,光诱导过程机理如图(V表示氧空位)。光照时,光催化剂产生电子(e-)和空穴(h+),驱动反应进行,下列叙述错误的是_______________。
A.反应过程中有非极性键的断裂和形成
B.e-从Ce原子转移到W,进而转移到吸附在氧空位的CO2分子上
C.h+和Rh附近的晶格氧结合,促进沉积在Rh上的C快速被消耗移除
D.CO2解离后在氧空位留下氧原子,一段时间后催化剂含氧量增加
(4)碱性甲烷燃料电池中,负极的电极反应式为____________________。
19.(2022·全国·高二课时练习)和均为重要的工业原料。已知:
Ⅰ
Ⅱ
请回答下列问题:
(1)与反应生成、和氯气的热化学方程式为___________。升高温度对该反应的影响为___________。
(2)若反应Ⅱ的逆反应的活化能为E,则E___________(填“>”“<”或“=”)220.9。
(3)t℃时,向10L恒容密闭容器中充入1和2,发生反应Ⅰ。5min时达到平衡,测得的物质的量为0.2。
①0~5min内,用表示的反应速率___________。
②的平衡转化率为___________。
③下列措施,既能加快逆反应速率又能增大的平衡转化率的是___________(填字母)。
A.缩小容器容积 B.加入催化剂 C.分离出部分 D.增大浓度
20.(2022·浙江·高三开学考试)工业合成尿素(H2NCONH2)以CO2和NH3为原料,在合成塔中存在如图转化:
图1
(1)液相中,合成尿素总反应的热化学反应方程式为____________________。
(2)一定条件下,CO2的平衡转化率与温度、初始氨碳比[L=]、水碳比[M=]的关系如图2和图3所示,回答下列问题:
①图2可知,其他条件不变,随温度升高,CO2的平衡转化率先上升后下降,“先升高”的原因是__________________________________;“后下降”的原因是由于设备腐蚀加剧等因素造成CO2的平衡转化率下降。
②下列说法正确的是_________。
A.图2两曲线中L1
C.图3曲线M1>M2,增大水碳比有利于尿素生成
D.实际工业生产时,可选用初始条件为氨碳比L1和水碳比M1
③若已知M1>M0,请在图2中画出在初始L1和M1条件下,CO2的平衡转化率随温度变化曲线_________。
(3)氨基甲酸钱(H2NCOONH4)为尿素生产过程中的产物,易分解,发生反应:H2NCOONH4(s)2NH3(g)+CO2(g)。某实验在恒容条件下,发生上述反应,根据实验测得数据绘制图像如图:
已知:RlnKp=-+C(C为常数)。根据图4计算该反应△H=_________kJ·ml-1。
21.(2022·浙江·高三开学考试)氢气是一种理想的能源,探索绿色化制氢是化学界一个热门话题。(本题反应中涉及△H、△S、△G均为298K条件值)。
(1)传统制备氢气方法之一为水煤气法:C(s)+H2O(g)=CO(g)+H2(g) △H=+132kJ·ml-1,该反应自发进行的条件是___________________。
(2)利用生物质可再生资源乙醇制备氢气具有良好的开发前景。乙醇在Ni-MgO催化下,制取氢气有如下方法:
方法a:水蒸气催化重整
CH3CH2OH(g)+H2O(g)4H2(g)+2CO(g)
△H1=+257kJ·ml-1 △S1=+459J·ml-1·K-1 △G1=+122.9kJ·ml-1
方法b:部分催化重整CH3CH2OH(g)+O2(g)3H2(g)+2CO(g)
△H2 △S2=+400J·ml-1·K-1 △G2
己知:298K时,相关物质的相对能量如图1。
①依据图1数据,计算方法b反应的△H2=_____kJ·ml-1。
②已知体系自由能变化:△G=△H-T△S,△G<0时反应自发进行。请从△G的角度分析方法a、b哪个更有利?__________________________。
③在某恒温和恒压(p0)体系中,CH3CH2OH和H2O以系数比投料进行方法a制氢,若平衡时H2的产率为50%,该条件下方法a反应的平衡常数Kp=______________。[如H2的平衡压强p(H2)= χ(H2)×p,χ(H2)为平衡系统中H2的物质的量分数,p为平衡时总压]
(3)有化学工作者提出,在Ni-MgO催化剂中添加纳米CaO强化,开展“催化氧化重整”制氢,是一种优化的制氢方法。
方法c:CH3CH2OH(g)+2H2O(g)+O2(g)5H2(g)+2CO2(g) △H=-67kJ·ml-1
①下列有关说法正确的是_________。
A.方法c制氢时,充分提高廉价原料O2的浓度,一定能增加氢气产率
B.方法c与a比,相同条件下方法c能耗更低,制氢速率更快
C.乙醇制氢的三种方法中原子利用率(期望产物的总质量与生成物总质量之比)大小关系为:c>a>b
D.方法c相当于方法b与水煤气变换CO(g)+H2O(g)CO2(g)+H2(g)的优化组合水醇比对乙醇平衡转化率有较大影响
②已知:常压、800K,反应在Ni-MgO催化下,测得乙醇平衡转化率与水醇比关系如图。请在图2中画出相同条件下,添加纳米CaO强化下的乙醇平衡转化率曲线____。
22.(2022·江苏南京·高三阶段练习)
I.已知:
①NaHCO3(s)= Na+(aq)+(aq) ΔH=+18.81 kJ·m1-1
②Na2CO3(s)= 2Na+(aq)+(aq) ΔH=-16.44 kJ· ml-1
③2NaHCO3(s)= Na2CO3(s)+CO2(g)+H2O(l) ΔH=+92.34 kJ·ml-1
请回答:
(1)资料显示,NaHCO3固体加热到100℃发生分解,但是加热 NaHCO3溶液不到80℃就有大量CO2气体放出,用反应热角度说明原因_________________。
(2)NaHCO3溶液中主要存在2种化学平衡:
a.+H2O⇌H2CO3+OH-,
b.2⇌+H2O+CO2。
根据理论计算0.10 ml·L-1NaHCO3溶液中2个反应的转化率随温度变化如图1所示(不考虑相互影响):
计算25℃0.10 ml·L-1NaHCO3溶液中CO2与H2CO3的总浓度最大可能为_______ml·L-1。
II. SO2和NOx都是大气污染物
(3)利用图2所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2。b极的电极反应式为_________________。
(4)其他条件相同,以一定流速分别向含催化剂A和B的反应管中通入一定比例O2、NH3、NO和N2的模拟烟气,测得NO的去除率与温度的关系图3所示。使用催化剂B,当温度高于360℃,NO的去除率下降的原因是______________________。
(5)O2在一定条件下能有效去除烟气中的SO2、NO,可能的反应机理图4所示,该过程可描述为_________________。
0.01
0.02
0.02
0.01
0.01
0.01
0.015
0.015
x
A.实验室制取乙酸乙酯
B.探究浓度对反应速率的影响
C.蒸干AlCl3溶液制无水AlCl3固体
D.进行喷泉实验
选项
操作或做法
目的
A
用玻璃棒蘸取某样品进行焰色反应
检验样品中的钠元素
B
用pH计测定同浓度的与NaY溶液的pH
比较和HY的酸性
C
向酸性溶液中先通入少量,充分反应后,再滴入几滴溶液
验证被氧化为
D
向溶液中加入过量的KI溶液,充分反应后,再滴入几滴KSCN溶液
探究KI与反应的可逆性
反应i
反应ii
v1 (正)
v1(逆)
v2 (正)
v2 (逆)
第十一章 有机化学基础 章末综合检测卷 -备战2023年高考化学【一轮·夯实基础】复习精讲精练: 这是一份第十一章 有机化学基础 章末综合检测卷 -备战2023年高考化学【一轮·夯实基础】复习精讲精练,文件包含第十一章有机化学基础章末综合检测卷原卷版-备战2023年高考化学一轮·夯实基础复习精讲精练docx、第十一章有机化学基础章末综合检测卷解析版-备战2023年高考化学一轮·夯实基础复习精讲精练docx等2份试卷配套教学资源,其中试卷共41页, 欢迎下载使用。
第九章 化学实验基础及综合实验 章末综合检测卷 -备战2023年高考化学【一轮·夯实基础】复习精讲精练: 这是一份第九章 化学实验基础及综合实验 章末综合检测卷 -备战2023年高考化学【一轮·夯实基础】复习精讲精练,文件包含第九章化学实验基础及综合实验章末综合检测卷原卷版-备战2023年高考化学一轮·夯实基础复习精讲精练docx、第九章化学实验基础及综合实验章末综合检测卷解析版-备战2023年高考化学一轮·夯实基础复习精讲精练docx等2份试卷配套教学资源,其中试卷共39页, 欢迎下载使用。
第六章 化学反应与能量 章末综合检测卷 -备战2023年高考化学【一轮·夯实基础】复习精讲精练: 这是一份第六章 化学反应与能量 章末综合检测卷 -备战2023年高考化学【一轮·夯实基础】复习精讲精练,文件包含第六章化学反应与能量章末综合检测卷原卷版-备战2023年高考化学一轮·夯实基础复习精讲精练docx、第六章化学反应与能量章末综合检测卷解析版-备战2023年高考化学一轮·夯实基础复习精讲精练docx等2份试卷配套教学资源,其中试卷共47页, 欢迎下载使用。












