

安徽省滁州市定远县八一学校2023-2024学年九年级下学期开学检测化学试题
展开可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Si-28
一、选择题(本题包括12个小题。每小题1分,共12分。每小题只有一个选项符合题意。)
1. “绿色化学”是21世纪化学科学发展的重要方向之一,其核心是从源头上减少对环境的污染.你认为下列不符合“绿色化学”的是( )
A. 对废气、废水、废渣进行严格处理
B. 少用或不用有害物质以及少排或不排放有害物质
C. 不使用任何化学物质
D. 路灯采用太阳能光伏发电技术
【答案】C
【解析】
【详解】A、对废气、废水、废渣进行严格处理符号绿色化学理念,故A正确;
B、少用或不用有害物质以及少排或不排放有害物质不符合绿色化学的理念,应该是不能排放有毒物质,而非少排,故B正确;
C、自然界的所有物质都是化学物质,故C错误;
D、路灯采用太阳能光伏发电技术与绿色化学有关,故D正确。
故选C。
2. 以下归纳和总结完全正确的一组是
您看到的资料都源自我们平台,20多万份试卷,家威杏 MXSJ663 每日最新,性比价最高
A. AB. BC. CD. D
【答案】D
【解析】
【详解】A、①稀有气体包括氦氖氩氪氙氡多种气体,属于混合物。②MnO2和KC1O3都属于化合物,氯酸钾含有三种元素因此不属于氧化物,选项不完全正确;
B、①氢气不纯点燃可能爆炸,使用氢气之前先验纯,②家中液化气泄漏应关闭阀门,开窗,不能打火否则会引起爆炸,选项不完全正确;
C、①煤气泄漏时闻到一股怪味是由于分子在不断的运动,被人闻到,②Mg和Al化学性质不同的主要原因:原子核外最外层电子数不同,选项不完全正确;
D、①门捷列夫发现元素的规律并制作出元素周期表;②张青莲参与并测定相对原子质量,选项完全正确;
故选:D。
3. H7N9 禽流感发病 5 日内使用达菲可显著减少重症,达菲主要有效成分是莽草酸(C7H10O5),下列关于莽草酸说法正确的是
A. 属于氧化物
B. 一个莽草酸分子中含有 5 个氧分子
C. 174g 莽草酸中含有 84g 碳元素
D. 由 7 个碳元素、10 个氢元素、5 个氧元素组成
【答案】C
【解析】
【详解】A、氧化物的定义:由两种元素组成且其中一种元素为氧元素的化合物为氧化物;莽草酸是由碳、氢、氧三种元素组成的,不属于氧化物,此选项错误;
B、分子是由原子构成的,所以一个莽草酸分子中含有 5 个氧原子,此选项错误;
C、174g 莽草酸中含有碳元素的质量= 174g =84g,此选项正确;
D、元素只讲种类不讲个数,所以是莽草酸是由碳元素、氢元素、氧元素组成,此选项错误;
故选C。
4. 盐酸与氢氧化钠溶液发生反应HCl+NaOH===NaCl+H2O,此反应属于( )
A. 化合反应
B. 分解反应
C. 置换反应
D. 复分解反应
【答案】D
【解析】
【详解】盐酸与氢氧化钠溶液发生反应HCl+NaOH===NaCl+ H2O,是两种化合物互相交换成分,得到两种新的化合物的反应,此反应属于复分解反应。故选答案D。
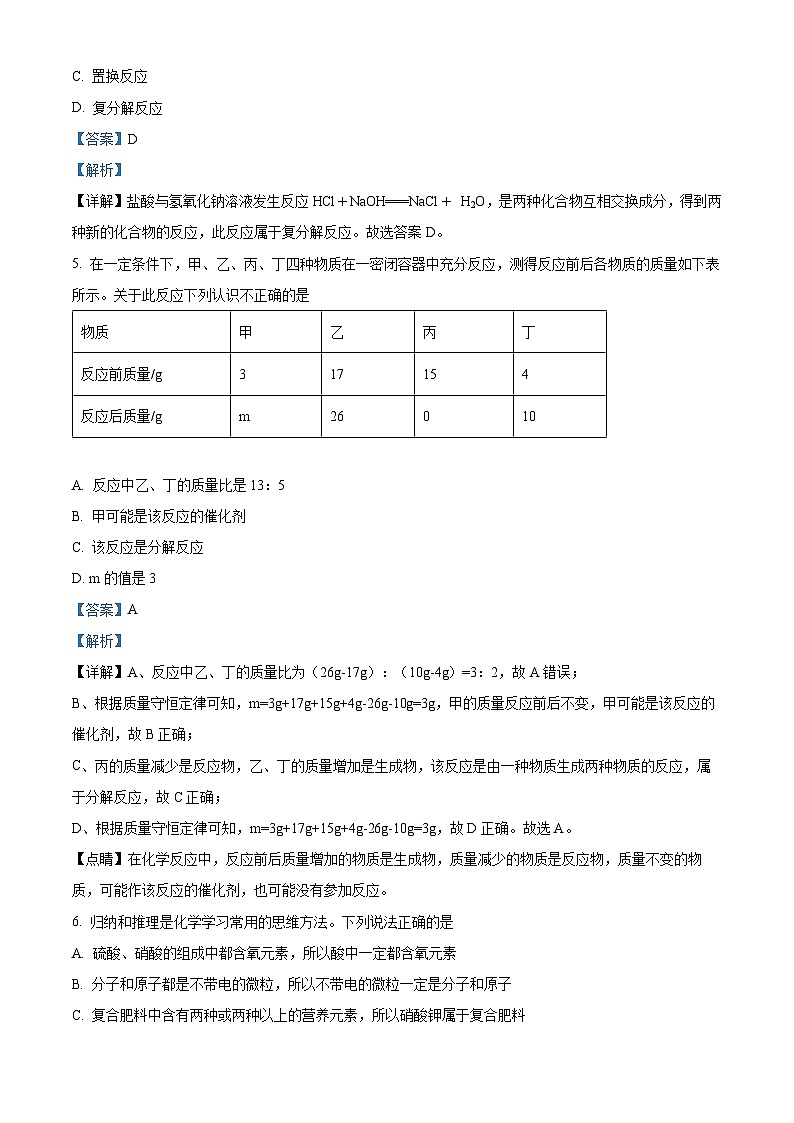
5. 在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如下表所示。关于此反应下列认识不正确的是
A. 反应中乙、丁的质量比是13:5
B. 甲可能是该反应的催化剂
C. 该反应是分解反应
D. m的值是3
【答案】A
【解析】
【详解】A、反应中乙、丁的质量比为(26g-17g):(10g-4g)=3:2,故A错误;
B、根据质量守恒定律可知,m=3g+17g+15g+4g-26g-10g=3g,甲的质量反应前后不变,甲可能是该反应的催化剂,故B正确;
C、丙的质量减少是反应物,乙、丁的质量增加是生成物,该反应是由一种物质生成两种物质的反应,属于分解反应,故C正确;
D、根据质量守恒定律可知,m=3g+17g+15g+4g-26g-10g=3g,故D正确。故选A。
【点睛】在化学反应中,反应前后质量增加的物质是生成物,质量减少的物质是反应物,质量不变的物质,可能作该反应的催化剂,也可能没有参加反应。
6. 归纳和推理是化学学习常用的思维方法。下列说法正确的是
A. 硫酸、硝酸的组成中都含氧元素,所以酸中一定都含氧元素
B. 分子和原子都是不带电的微粒,所以不带电的微粒一定是分子和原子
C. 复合肥料中含有两种或两种以上的营养元素,所以硝酸钾属于复合肥料
D. 二氧化碳排放过多会造成温室效应加剧,所以造成温室效应加剧的气体只有二氧化碳
【答案】C
【解析】
【分析】
【详解】A、硫酸、硝酸的组成中都含氧元素,而酸中不一定都含氧元素,如盐酸中不含氧元素,选项推理不正确;
B、分子和原子都是不带电的微粒,不带电的微粒不一定是分子和原子,也可能是中子,选项推理不正确;
C、复合肥料中含有两种或两种以上的营养元素,硝酸钾中含有N、P、K中的氮元素和钾元素,属于复合肥料,选项推理正确;
D、二氧化碳排放过多会造成温室效应加剧,造成温室效应加剧的气体除了二氧化碳外,还有臭氧、甲烷等气体,选项推理不正确。
故选C。
7. 下列实验操作正确的是
A. 稀释浓硫酸 B. 氧气验满
C. 移走蒸发皿 D. 测溶液的pH
【答案】B
【解析】
详解】A、稀释浓硫酸应将浓硫酸沿着烧杯壁缓缓注入水中,不正确;
B、氧气验满是将带火星木条放到集气瓶口,正确;
C、移走蒸发皿用坩埚钳,不能用手,不正确;
D、测溶液PH,应用玻璃棒蘸取溶液滴到PH试纸上,这样会污染试剂,不正确。
故选B。
8. 在催化剂作用下,二氧化碳与氢气能高效转化为甲醇(CH3OH),下列说法正确的是
A 反应前后原子、分子种类没有发生改变
B. 反应前后氢元素的化合价未改变
C. 该反应的四种物质中有两种氧化物
D. 参加反应的甲和乙的个数比为1:1
【答案】C
【解析】
【分析】由图可知,A为CO2、乙为H2、丙为CH3OH、丁为H2O,反应的化学方程式为。
【详解】A、化学反应的实质为分子分成原子,原子重新组合成新的分子,即反应前后原子种类没有改变,分子种类发生改变,该选项说法不正确;
B、反应前氢气中氢元素的化合价为0价,反应后氢元素的化合价为+1价,则反应前后氢元素的化合价发生改变,该选项说法不正确;
C、氧化物中含有两种元素,且一种元素属于氧元素,该反应中属于氧化物的为CO2和H2O,该选项说法正确;
D、由化学式可知,参加反应的甲和乙的个数比为1:3,该选项说法不正确。
故选C。
9. 碳及含碳物质有如图所示转化关系,下列说法不正确的是
A. 物质Y不可以选择稀硫酸
B. X可以是酒精,也可以是石墨烯
C. 反应①一定是化合反应
D. 反应②可以是吸热反应
【答案】C
【解析】
【详解】A、碳酸钙和稀硫酸反应生成的硫酸钙微溶于水,会覆盖在碳酸钙的表面,阻碍反应的进一步进行,故物质Y不能选择稀硫酸,选项正确;
B、酒精燃烧生成二氧化碳和水,石墨烯碳单质,碳单质燃烧生成二氧化碳,故X可以是酒精,也可以是石墨烯,选项正确;
C、反应①可以是碳燃烧生成二氧化碳,该反应符合“多变一”特点,属于化合反应,也可以是碳和氧化铜在加热的条件下反应生成铜和二氧化碳,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应,选项错误;
D、反应②可以是二氧化碳和碳在高温下反应生成一氧化碳,该反应是吸热反应,选项正确。
故选C。
10. 分类是一种重要的学习方法,下列各组按混合物、氧化物、单质顺序排列的是
A. 冰水混合物、二氧化氮、稀有气体B. 氯酸钾、氢氧化钙、液氧
C. 石灰石、过氧化氢、金刚石D. 硬水、碳酸钠、臭氧
【答案】C
【解析】
【分析】混合物中含有多种物质,氧化物是指含有两种元素,且一种元素为氧元素的化合物;单质是指只含一种元素的纯净物。
【详解】A、冰水混合物中只含水一种物质,属于纯净物;二氧化氮是由氮、氧两种元素组成,属于氧化物;稀有气体中含有氦气、氖气等,属于混合物,该选项不符合题意。
B、氯酸钾中只含一种物质,属于纯净物;氢氧化钙中含有钙、氢、氧三种元素,不属于氧化物;液氧中只含氧一种元素,属于单质,该选项不符合题意。
C、石灰石的主要成分为碳酸钙,属于混合物;过氧化氢是由氢、氧两种元素组成,属于氧化物;金刚石为碳单质,该选项符合题意。
D、硬水中含有钙、镁化合物和水,属于混合物;碳酸钠是由钠、碳、氧三种元素组成,不属于氧化物;臭氧中只含一种元素,属于单质,该选项不符合题意。
故选C。
11. 黑火药是中国古代四大发明之一,其燃烧时发生的反应是S+2KNO3+3CK2S+3X↑+N2↑,其中X的化学式是
A. O2B. COC. CO2D. K2CO3
【答案】C
【解析】
【分析】
【详解】化学反应前后,原子的种类和个数均不变,方程式等号右侧和左侧相比少了3个碳原子和6个氧原子,所以3个X分子中应该含有3个碳原子和6个氧原子,因此1个X分子中含1个碳原子和2个氧原子,所以X化学式为CO2,故选C。
12. 下图能正确反映对应关系的是
A. 利用红磷燃烧测定空气中氧气的含量(打开止水夹前)
B. 在少量二氧化锰中加入一定量双氧水
C. 加热氯酸钾制取氧气
D. 甲烷和过量的氧气在密闭容器中完全反应
【答案】B
【解析】
【详解】A、红磷燃烧放热,气压增大,完全反应后温度降低,氧气消耗,气压减小,该选项对应关系不正确;
B、双氧水在二氧化锰的催化作用下生成水和氧气,随着反应进行,氧气质量增加,双氧水分解完全之后,氧气质量不再改变,该选项对应关系正确;
C、一定条件下氯酸钾分解生成氯化钾和氧气,随着反应进行,氯化钾和氧气质量增大,氯化钾和氧气质量不再变化的时间应该是同一时间,该选项对应关系不正确;
D、甲烷燃烧生成水和二氧化碳,反应前后分子总数不变,该选项对应关系不正确。
故选:B。
二、综合题(本题包括5个大题。共28分)
13. 近年来,我国航空、航天、高铁等得到长足发展,跻身世界前列。大飞机C919试飞成功,标志着我国的航空强国梦又迈出了一大步。大飞机使用的化学材料如甲图。请回答:
(1)钛合金属于_______(填“金属”或“合成”)材料。
(2)乙图是钛原子结构示意图,则x=_______;画出第三周期与钛原子化学性质相似原子的原子结构示意图_______。
(3)铝制品有较好的耐腐蚀性,曾被用作各种炊具,但铝制饮具不能用酸性溶液浸泡,写出稀盐酸破坏铝制品表面氧化膜的化学方程式:_______。
【答案】(1)金属 (2) ①. 8 ②.
(3)
【解析】
【分析】
【小问1详解】
合金是由金属与金属或金属与非金属组成的混合物,属于金属材料。
【小问2详解】
在原子中,原子核外的电子总数等于核内的质子数,故x=22-2-10-2=8,第三周期原子核外有3个电子层,与钛原子化学性质相似,即最外层电子数为2,故该原子的原子结构示意图为:。
【小问3详解】
铝易与空气中的氧气反应生成氧化铝薄膜,稀盐酸与氧化铝反应生成氯化铝和水,反应的化学方程式为:。
14. 我国制碱工业的先驱一一侯德榜先生发明了“侯氏制碱法”,提高了食盐利用率,降低了纯碱的成本,为世界制碱技术谱写了新的篇章。“侯氏制碱法”的主要原理是以氯化钠、二氧化碳、氨气(NH3)为原料制备碳酸钠,其主要流程如图:
回答下列问题:
(1)溶解池中用搅拌器搅拌的目的是_________________。
(2)分离器中分离出NaHCO3固体的实验基本操作名称是_________________。
(3)煅烧炉中发生反应的化学方程式为_________________。
(4)为提高生产效率,在炭化塔中应综合考虑该生产的条件是________________(填字母序号)。
a.高温 b.低温 c.常温 d.高压 e.低压 f.常压
(5)为了使碳化塔中的反应能顺利进行,工业生产过程中是先通入氨气,形成氨的氯化钠饱和溶液之后,再通入二氧化碳气体的。这样做的原因是_________________。
【答案】(1)加快溶解速率
(2)过滤 (3)
(4)ad##da (5)先通入NH3使食盐水显碱性,能够吸收大量CO2气体
【解析】
【小问1详解】
溶解池中加装搅拌器的目的是加快溶解速率;
【小问2详解】
分离器中,是将固体与液体分离,分离出 NaHCO3固体的操作是过滤;
【小问3详解】
煅烧炉中,加热时碳酸氢钠分解生成碳酸钠、水和二氧化碳,发生反应的化学方程式为:;
【小问4详解】
碳化塔中发生的反应是氨气、二氧化碳、氯化钠溶液反应生成碳酸氢钠沉淀和氯化铵,气体的溶解度随温度降低而减小,压强增大而增大,碳酸氢钠在水中的溶解度随着温度的降低而减少,较高的温度有利于碳酸氢钠晶体的生长。为提高生产效率,在炭化塔中应综合考虑该生产的条件是高温、高压,故填:ad;
【小问5详解】
为了使碳化塔中的反应能顺利进行,工业生产过程中是先通入氨气,形成氨的氯化钠饱和溶液之后,再通入二氧化碳气体的。这样做的原因是先通入NH3使食盐水显碱性,能够吸收大量CO2气体。
15. 通过学习,你已经掌握了实验室制取气体的一些规律,以下是老师提供的一些实验装置,请你结合下图回答问题:
(1)写出实验室常温下制备氧气的化学方程式___________。
(2)选择___________装置组合来制备和收集氧气(填字母编号)。
(3)已知氨气是一种密度比空气小且极易溶于水的气体。将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是___________、___________。
(4)加热氯化铵与氢氧化钠的固体混合物制取氨气(同时生成氯化钠和水),应选择的反应发生装置是___________,收集装置为___________,此反应的化学方程式为___________。
【答案】(1)
(2)AC或AD或AF或BC或BD或BF
(3) ①. 集气瓶内液面上升 ②. 水由无色变为红色
(4) ①. A ②. E ③.
【解析】
【小问1详解】
实验室常温下制氧气选用过氧化氢溶液在二氧化锰作催化剂的条件下生成水和氧气,化学方程式为:
【小问2详解】
制氧气的药品可选用高锰酸钾或氯酸钾与二氧化锰混合加热,可选固体加热型发生装置即A,或选用过氧化氢溶液和二氧化锰混合,适用于固液常温型即B,由于氧气密度比空气略大故选用向上排空气法即D,氧气不易溶于水故可选用排水法收集即C,也可用万用瓶代替收集即装置F,故填:AC或AD或AF或BC或BD或BF
【小问3详解】
氨气极易溶于水形成氨水,使集气瓶内气体减少气压降低,大气压把水会压入集气瓶内,氨水显碱性可以使无色酚酞变红,故填:集气瓶内液面上升;水由无色变为红色。
【小问4详解】
加热氯化铵与氢氧化钠的固体混合物生成氨气,同时生成氯化钠和水,化学方程式为:。
16. 某小组选用鸡蛋壳(主要成分为CaCO3,其它成分不与水、稀盐酸反应)、稀盐酸、带过滤网的透明太空杯和电子秤等用品探究质量守恒定律。
取足量的稀盐酸加入太空杯中,再取1.1g鸡蛋壳放入过滤网内,按以下步骤进行实验并记录所称的质量(图中电子秤已省略)。
(1)实验前,需检查太空杯的___________。
(2)步骤Ⅱ中观察到鸡蛋壳表面___________(填现象)。
(3)比较步骤I与步骤___________所称物质量可知,参加化学反应的各物质的质量总和等于反应后生成物各物质的质量总和。
(4)充分反应后,生成物CO2的质量是___________g。
(5)根据化学方程式计算1.1g鸡蛋壳中CaCO3的质量。(写出计算过程)
【答案】(1)气密性 (2)产生大量气泡
(3)Ⅱ(或“Ⅲ”或“Ⅱ、Ⅲ”)
(4)0.44 (5)解:设1.1g鸡蛋壳中CaCO3的质量为x
x=1g
答:1.1g鸡蛋壳中CaCO3的质量为1g
【解析】
【分析】
【小问1详解】
碳酸钙能与稀盐酸反应生成氯化钙、二氧化碳和水,有气体生成,故实验前,需检查太空杯的气密性;
【小问2详解】
步骤Ⅱ中,倒置,鸡蛋壳和稀盐酸接触,碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,故观察到鸡蛋壳表面产生大量气泡;
【小问3详解】
比较步骤I与步骤Ⅱ、Ⅲ所称物质量可知,参加化学反应的各物质的质量总和等于反应后生成物各物质的质量总和;
【小问4详解】
根据质量守恒定律,化学反应前后,物质的总质量不变,可得生成二氧化碳的质量是:240.00g-239.56=0.44g;
【小问5详解】
见答案。
17. NaOH潮解后极易与空气中的CO2反应生成Na2CO3而变质。为测定实验室一瓶放置已久的烧碱中Na2CO3含量,某同学取适量的烧碱样品,溶于一定量的水得到200g溶液;再加入200g稀硫酸(足量)充分搅拌到不再放出气泡为止,称量溶液为395.6g。
(1)反应产生的CO2的质量为 g。
(2)若所取烧碱样品为50.0g,则样品中Na2CO3的质量分数是多少?
【答案】(1)4.4 (2)解:设样品中Na2CO3的质量分数是x
x=21.2%
答:则样品中Na2CO3的质量分数是21.2%。
【解析】
【小问1详解】
依据质量守恒定律反应产生的CO2的质量=200g+200g-395.6g=4.4g;
【小问2详解】
详解见答案。A.物质类别的认识
B.对安全的认识
①稀有气体属于纯净物。
②MnO2和KC1O3都属于氧化物。
①使用氢气之前先验纯
②家中液化气泄漏赶紧打火检查漏气管。
C.对微观解释的认识
D.对人物贡献的认识
①煤气泄漏时闻到一股怪味:分子在不
断的运动。
②Mg和Al化学性质不同的主要原因:
原子核外电子数不同。
①门捷列夫——元素周期表。
②张青莲——测定相对原子质量。
物质
甲
乙
丙
丁
反应前质量/g
3
17
15
4
反应后质量/g
m
26
0
10
Ⅰ
Ⅱ
Ⅲ
IV
实验步骤
拧紧杯盖,称量反应前总质量
倒置,称量反应过程中总质量
充分反应后正放,称量总质量
打开杯盖片刻后称量总质量
所称的质量/g
240.00
240.00
240.00
239.56
安徽省滁州市定远县育才学校2023-2024学年九年级下学期开学考化学试题: 这是一份安徽省滁州市定远县育才学校2023-2024学年九年级下学期开学考化学试题,共14页。试卷主要包含了请将答案正确填写在答题卡上,6时才是酸雨,此选项错误;, 钪是一种“工业的维生素”等内容,欢迎下载使用。
安徽省滁州市定远县八一学校2023-2024学年九年级下学期开学模拟化学试题: 这是一份安徽省滁州市定远县八一学校2023-2024学年九年级下学期开学模拟化学试题,共13页。试卷主要包含了选择题,综合题等内容,欢迎下载使用。
安徽省滁州市定远县八一学校2023-2024学年九年级下学期开学检测化学试题: 这是一份安徽省滁州市定远县八一学校2023-2024学年九年级下学期开学检测化学试题,共8页。试卷主要包含了选择题,综合题等内容,欢迎下载使用。












