

2022年江苏淮安中考化学真题及答案
展开一、单选题
1.下列变化中,属于物理变化的是
A.滴水成冰B.花生霉变C.蜡烛燃烧D.葡萄酿酒
2.储存易燃物和易爆物的厂房需要有明显的安全标志。下列图标不属于消防安全标志的是
A.B.
C.D.
3.下列常见物品所用材料属于无机非金属材料的是
A.塑料脸盆B.陶瓷花瓶C.不锈钢刀叉D.机动车轮胎
4.“端午到,粽香飘”。对闻到粽子香气的解释合理的是
A.分子的数目变多B.分子的体积变大
C.分子在不断运动D.分子发生了分解
5.在探究“铜绿”性质的实验中,下列操作错误的是
A.添加“铜绿”B.倾倒盐酸
C.点燃酒精灯D.洗涤试管
6.下列关于空气及其成分的说法错误的是
A.空气中各成分含量相对稳定B.CO2含量过高影响人体健康
C.N2用作粮食、瓜果的保护气D.O2可以支持所有的物质燃烧
7.胰蛋白酶是我国自主研发新冠疫苗的原料之一,其中一种胰蛋白酶的化学式为C6H15O12P3。下列关于这种胰蛋白酶的说法正确的是
A.该物质由四种元素组成B.该物质由碳、氢、氧、磷原子构成
C.该物质的相对分子质量为372gD.该物质中碳、氧元素的质量比为2:1
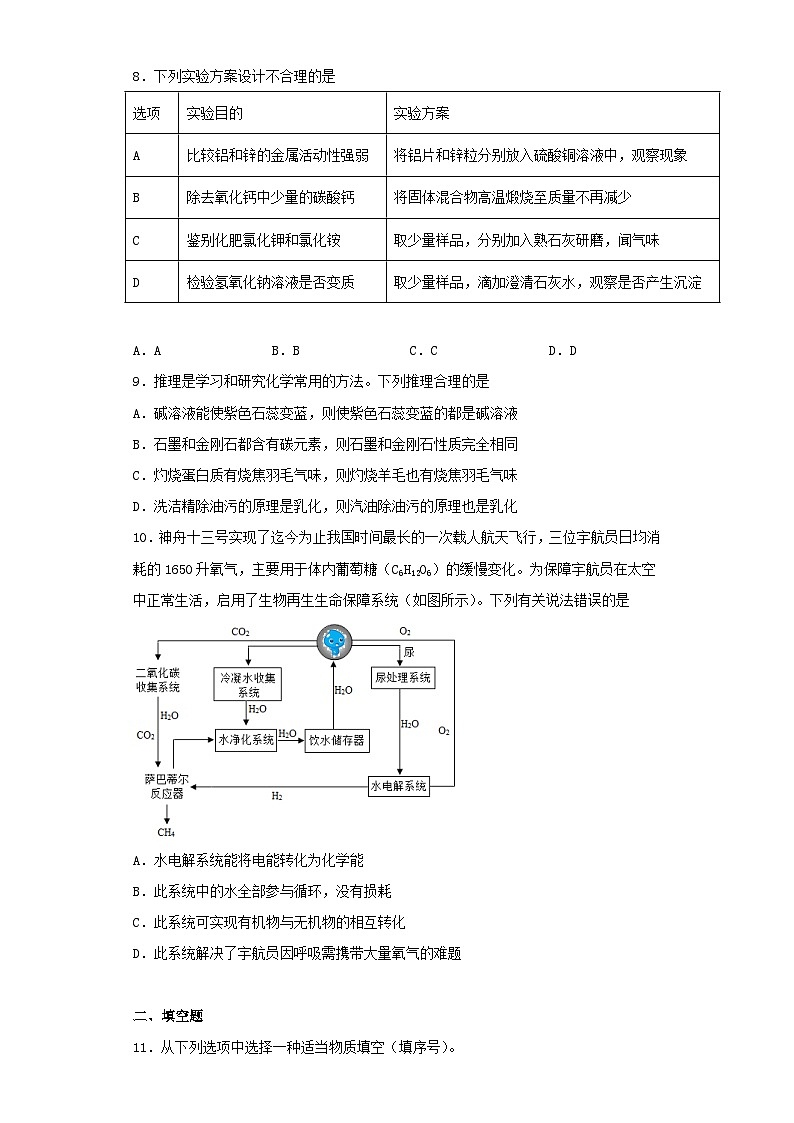
8.下列实验方案设计不合理的是
A.AB.BC.CD.D
9.推理是学习和研究化学常用的方法。下列推理合理的是
A.碱溶液能使紫色石蕊变蓝,则使紫色石蕊变蓝的都是碱溶液
B.石墨和金刚石都含有碳元素,则石墨和金刚石性质完全相同
C.灼烧蛋白质有烧焦羽毛气味,则灼烧羊毛也有烧焦羽毛气味
D.洗洁精除油污的原理是乳化,则汽油除油污的原理也是乳化
10.神舟十三号实现了迄今为止我国时间最长的一次载人航天飞行,三位宇航员日均消耗的1650升氧气,主要用于体内葡萄糖(C6H12O6)的缓慢变化。为保障宇航员在太空中正常生活,启用了生物再生生命保障系统(如图所示)。下列有关说法错误的是
A.水电解系统能将电能转化为化学能
B.此系统中的水全部参与循环,没有损耗
C.此系统可实现有机物与无机物的相互转化
D.此系统解决了宇航员因呼吸需携带大量氧气的难题
二、填空题
11.从下列选项中选择一种适当物质填空(填序号)。
A.淀粉 B.干冰 C.小苏打
(1)生活中可用于治疗胃酸过多的物质是____________。
(2)用于人工降雨、制造舞台云雾的物质是_____________。
(3)在面条上滴1滴碘水,观察到表面呈蓝色,说明面条中含有____________。
12.“绿水青山就是金山银山”是建设生态文明的重要理念。
(1)保护洪泽湖水资源,建设优美的生态环境。下列措施可行的是 。
A.清理水中废弃物B.游船使用清洁能源C.随意捕捞水产品
(2)二氧化氯(ClO2)是一种常用的消毒剂,可用X与SO2反应制备。该反应的化学方程式为 ,其中X的化学式是____________。
(3)请你列举一条生活中节水的具体措施____________。
13.硝酸钾、硝酸钠、氯化钠的溶解度曲线如图所示。回答下列问题:
(1)氯化钠以离子形式分散在水中,氯化钠中带正电荷的离子是____________(填离子符号)。
(2)60℃时,硝酸钾的溶解度是____________g。
(3)20℃时,将40g硝酸钠加入50g水中,形成____________溶液(填“饱和”或“不饱和”)。
(4)60℃时,将等质量的硝酸钾和氯化钠的饱和溶液分别降温至20℃。下列判断正确的是 。
A.析出晶体质量:硝酸钾>氯化钠
B.所得溶液中溶剂质量:硝酸钾>氯化钠
C.所得溶液中溶质质量分数:硝酸钾>氯化钠
14.根据如图所示气体制取装置,回答下列问题:
(1)组装A时,依据酒精灯____________(填“外焰”或“内焰”)的高度调节试管位置。
(2)实验室用双氧水和二氧化锰制备氧气,应选择的发生装置是____________(填序号),该反应的化学方程式是____________。
(3)通常情况下,二氧化碳能溶于水。实验室若采用排水法收集二氧化碳气体,为减少其损耗,应选择的装置是____________(填序号)。
三、实验题
15.淮安有丰富的盐矿资源,化学兴趣小组同学称取一定质量粗盐样品(含有泥沙),用如图所示装置进行初步提纯。回答下列问题:
(1)操作①中,发现天平指针向右偏,接下来的操作是____________。
(2)操作④中,滤液仍然浑浊,可能的原因是 。
A.滤纸破损B.滤纸未紧贴漏斗内壁C.漏斗内液面高于滤纸边缘
(3)操作⑤中,待蒸发皿内出现____________时,停止加热。
四、流程题
16.某氮肥厂用煤、空气和水为原料合成氨气(NH3),同时可得到副产品碳酸氢铵。其工艺流程如图所示:
回答下列有关问题:
(1)煤加入煤气发生炉前需经过粉碎处理,其目的是____________。
(2)“合成塔”中发生反应的化学方程式是____________。
(3)部分氨气通入“碳化塔”的目的是____________。
(4)氨气被广泛认为是未来理想的零碳燃料,其燃烧的微观示意图如图所示。
①参加反应的甲、乙分子个数比是____________。
②该反应属于____________(填基本反应类型)反应。
五、科普阅读题
17.阅读下面短文,回答问题。
铁是生活中使用最广泛的金属,活泼性较强,铁元素属于人体必需微量元素之一。
我国在春秋时期就开始了铁的冶炼,汉代出现了最早的炼铁高炉。
“苟利国家生死以,岂因祸福避趋之。”林则徐修筑洪泽湖大堤,所展现出的勤政爱民、甘于奉献是其一生赤子情怀的缩影。林则徐用生铁铸成铁锅(如图1),放在条石的齿槽之间,再浇上由糯米汁与熟石灰搅拌而成的砂浆,使得条石与条石牢牢地黏合在一起,不留丝毫缝隙,做到了针插不进、水泼不进。他还在每一块铁锔上刻上自己的名字,以表示对其修筑的工程终身负责。如今一百九十多年过去了,洪泽湖大堤依然固若金汤。
(1)人体缺乏铁元素,会影响健康,易得____________(填序号)。
A.佝偻病 B.贫血症 C.甲状腺疾病
(2)工业上用赤铁矿石(主要成分:Fe2O3)冶炼生铁,Fe2O3与CO反应的化学方程式是____________。
(3)利用铁锔和砂浆将条石与条石牢牢黏合在一起,使大堤固若金汤。
①说明铸造铁锔的生铁具有的物理性质是_____________。
②砂浆中的熟石灰与空气接触,发生反应的化学方程式是____________。
(4)从条石中取出的铁锔暴露在空气中一段时间后,表面因生锈而腐蚀。导致铁腐蚀的因素有多种,化学兴趣小组同学对此开展以下探究:取四份质量均为0.15g的生铁粉末,分别放入如图2所示装置中进行四次实验。内容记录如下表所示:
①由实验Ⅱ、Ⅲ可知,加速铁生锈的物质是____________。
②能说明铁生锈需要水的证据是____________。
③实验Ⅳ中氧气含量下降的原因可能是____________。
六、综合应用题
18.硫酸是世界上产量最大、用途最广的酸,被称为“化学工业之母”。化学兴趣小组同学对硫酸进行了多角度的研究。
【物质制备】
(1)工业上采用接触法制硫酸:先煅烧黄铁矿得到SO2,再将SO2经过一系列变化得到硫酸。SO2中硫元素的化合价是_______________。
【物质性质】
(2)用温度计的水银球一端蘸取浓硫酸,取出后在空气中放置一段时间,观察到温度计示数上升,是因为浓硫酸能吸收____________,并放出热量。
(3)请利用下图提供的仪器与药品,探究稀硫酸与氢氧化钠溶液的反应。
①取____________(填“A”或“B”)中的氢氧化钠溶液5mL加入烧杯中,并插入pH计。
②从另一试剂瓶中取出稀硫酸逐滴加入①的溶液中,并用____________(填仪器名称)不断搅拌。反应过程中溶液pH变化的部分数据如下表所示:
③在pH=12.8时,溶液中的溶质是____________(填化学式)。
④滴加稀硫酸过程中,溶液pH不断减小的原因有:
a.硫酸与氢氧化钠发生了反应;
b.______
⑤为证明溶液pH从13.1减小到10.4的过程中,④中原因a起主要作用,需设计的实验方案是____________。
【定量研究】
(4)某工厂现有含碳酸钠的废水需要处理。为测定废水中碳酸钠的质量分数,化学兴趣小组同学取废水样品100g,加入溶质质量分数为10%的硫酸溶液9.8g,恰好完全反应,反应的化学方程式: (此废水中其他物质不与硫酸反应)。计算废水中碳酸钠的质量分数(写出计算过程)。
选项
实验目的
实验方案
A
比较铝和锌的金属活动性强弱
将铝片和锌粒分别放入硫酸铜溶液中,观察现象
B
除去氧化钙中少量的碳酸钙
将固体混合物高温煅烧至质量不再减少
C
鉴别化肥氯化钾和氯化铵
取少量样品,分别加入熟石灰研磨,闻气味
D
检验氢氧化钠溶液是否变质
取少量样品,滴加澄清石灰水,观察是否产生沉淀
序号
实验操作
3分钟时氧气的含量
Ⅰ
/
21%
Ⅱ
打开分液漏斗活塞,滴加2mL蒸馏水,关闭活塞
15%
Ⅲ
打开分液漏斗活塞,滴加2mL食盐水,关闭活塞
8%
Ⅳ
打开分液漏斗活塞,滴加2mL溶质质量分数为10%的稀盐酸,关闭活塞
13%
稀硫酸体积/mL
0
2
4
6
8
……
溶液pH
13.1
12.8
12.3
11.5
10.4
……
2022年江苏淮安中考化学真题参考答案
1.A
2.D
3.B
4.C
5.B
6.D
7.A
8.A
9.C
10.B
11.(1)C
(2)B
(3)A
12.(1)AB
(2)KClO3
(3)淘米水浇花等(合理即可)
13.(1)Na+
(2)110
(3)不饱和
(4)A
14.(1)外焰
(2) B
(3)D
15.(1)向左盘加入粗盐直到天平平衡
(2)AC
(3)较多固体
16.(1)使反应更快更充分
(2)
(3)除去气体中的CO2
(4) 4:3 置换反应
17.(1)B
(2)
(3) 硬度大
(4) 食盐水 实验Ⅰ不加水,氧气含量不减少,实验Ⅱ加水后,氧气含量减少 铁与盐酸反应生成氯化亚铁和氢气,气体体积增加,氧气含量下降。
18.(1)+4
(2)水蒸气
(3) A 玻璃棒 NaOH、Na2SO4 水稀释氢氧化钠溶液 取等质量的pH=13.1的两烧杯氢氧化钠溶液,一杯加入稀硫酸直至pH=10.4,记录加入稀硫酸的质量。另一杯加入蒸馏水直至pH=10.4,记录加入蒸馏水的质量
(4)解:加入硫酸的质量为9.8g×10%=0.98g
设废水中碳酸钠的质量为x
碳酸钠的质量分数为。
答:废水中碳酸钠的质量分数是1.06%。
2023年江苏省淮安市中考化学真题(无答案): 这是一份2023年江苏省淮安市中考化学真题(无答案),共6页。试卷主要包含了做其次局部时,用0,5 K39,5gD,物质世界丰富多彩,金属是一类重要的材料等内容,欢迎下载使用。
2023年江苏省淮安市中化学考真题(无答案): 这是一份2023年江苏省淮安市中化学考真题(无答案),共4页。
_2018年江苏淮安中考化学真题及答案: 这是一份_2018年江苏淮安中考化学真题及答案,共7页。试卷主要包含了选择题,填空与简答题,实验与探究题,计算题等内容,欢迎下载使用。












