






沪科技版(2020)必修第一册分散系教案配套课件ppt
展开溶液:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
溶剂:能溶解其他物质的物质。
例如:医用酒精、浓硫酸、盐酸、盐水
乳浊液:不溶于水的且由许多分子集合而成的小液滴分散到液体里形成的混合物。
例如:振荡水和植物油得到乳状浑浊液体
悬浊液:液体里悬浊着很多不溶于水的固体小颗粒,使液体呈现浑浊状态。即固体小颗粒分散到液体里形成的混合物。
三者共同点:由一种或几种物质分散到另一种物质中形成的混合物。
1、定义:化学上把一种(或多种)物质粒子形式分散到另一种(或多种)物质中所形成的混合物,叫做分散系。
分散质:分散系中被分散成粒子的物质(少)
分散剂:另一种物质即粒子分散在其中的物质(多)
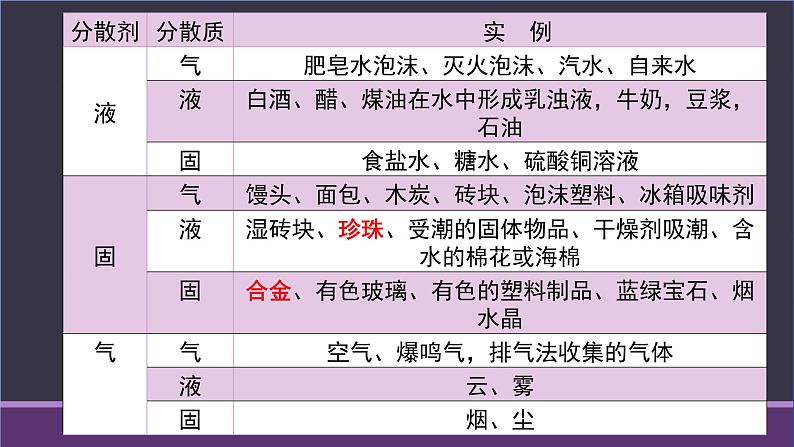
a.依据:分散剂和分散质的状态
b.依据:分散质粒子大小
1、定义:分散质微粒的直径在1-100nm的分散系
依据:(1)分散剂的状态
注:胶体不是一类物质,而是几乎任何物质都可能形成的一种分散状态
粒子胶体,例如:Fe(OH)3 胶体
分子胶体,例如:淀粉胶体、蛋白质胶体等
实验1-1:Fe(OH)3胶体的制备
实验1-2:用激光笔照射硫酸铜溶液和氢氧化铁胶体,观察实验现象。
方法:向40mL沸水中逐滴滴加5~6滴饱和FeCl3溶液,至液体呈红褐色,停上加热。
1. 用蒸馏水,不可用自来水,自来水中的离子会使胶体沉淀;
2. 用饱和氯化铁溶液,浓度太小,不易形成胶体;
3. 溶液呈红褐色时停止加热,加热过度易形成沉淀;
4. 不能搅拌,易使胶体粒子相互碰撞形成沉淀;
1. 丁达尔效应——特性
区分胶体与溶液的一种常用物理方法
定义:光束通过胶体时,在垂直入射光方向可以看到一条明亮的“通路”。原因:由于胶体粒子(分散质微粒)对光线散射(光波偏离原来方向而分散传播)形成的
当丁达尔效应出现的时候,光就有了形状
丁达尔效应是区分胶体与溶液的一种物理方法
没有光亮的“通路”,没有丁达尔效应
光亮的“通路”,具有丁达尔效应
为什么会出现丁达尔效应?
胶体的聚沉:1.加入电解质溶液 2.加入带相反电荷的胶体粒子 3.过度加热或剧烈搅拌
原因:①胶体粒子由于吸附而带电,同种胶体粒子带相同电荷,他们之间互相排斥阻止了胶体粒子变大,使得不易聚集; ②胶体粒子做布朗运动,也就是无规则运动,使得不易聚集。
胶体属于介稳体系,在一定条件下可以稳定存在。
(2) 河口三角洲的形成
(3)FeCl3溶液可用于止血
(4) 墨水混用容易堵塞
胶粒具有很大的表面积,故其具有很强的吸附性。
明矾(KAl(SO4)2·12H2O
利用胶体粒子直径>半透膜孔径>离子和小分子粒径,是提纯胶体的方法。
思考1:如果向氢氧化铁胶体中逐滴滴加稀硫酸溶液,可能出现什么情况?
生成红褐色沉淀,继续滴加沉淀溶解
思考2:有哪些方法可以辨别无色透明的胶体与食盐溶液?
能产生丁达尔现象的是胶体;不能透过半透膜的是胶体。
1、胶体和其他分散系〔溶液、浊液〕的本质区别是
A、分散质粒子的大小B、是不是一种稳定的体系C、会不会产生丁达尔效应D、粒子有没有带电荷
2.下列物质中,不能产生丁达尔现象的是
①烟雾 ②溴水 ③蒸馏水 ④沸水中加几滴FeCl3饱和溶液 ⑤淀粉溶液 ⑥有色玻璃 ⑦鸡蛋清溶液⑧乙醇水溶液
A.②⑧B.②③⑧C.②③⑤⑥⑦D.⑤④⑥⑦
高中化学沪科技版(2020)必修第一册分散系教学ppt课件: 这是一份高中化学沪科技版(2020)必修第一册分散系教学ppt课件,共22页。PPT课件主要包含了自然界的丁达尔现象,小油滴,小土粒,Na+和Cl-,分散系的分类,1nm,100nm,nm~100nm,胶体的分类,胶体的性质等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第一节 物质的分类及转化教学课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第一节 物质的分类及转化教学课件ppt,共27页。PPT课件主要包含了发现大自然的美,学习目标等内容,欢迎下载使用。
苏教版 (2019)第三单元 物质的分散系教课内容ppt课件: 这是一份苏教版 (2019)第三单元 物质的分散系教课内容ppt课件,共18页。PPT课件主要包含了分散系的概述,分散系的分类,胶体的性质等内容,欢迎下载使用。













