
四川省蓬溪中学校2023-2024学年高二上学期开学考试化学试题
展开可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23Fe-56Ni-59
Cu-64
一、选择题:本题共 14 小题,每小题 3 分,共 42 分。在每小题只有一项是符合题目要求。
1.日常生活中的下列做法不是为了加快化学反应速率的是
A.清洗水壶垢用较浓白醋B.将煤块粉碎后燃烧
C.发馒头加酵母粉D.月饼盒内放置还原性铁粉
2.在测定中和反应反应热的实验中,下列说法正确的是
A.测量酸溶液的温度后,未冲洗温度计就测碱溶液的温度,会使求得的中和热的数值偏大
B.0.1ml/L盐酸与某强碱稀溶液中和放出的热量随反应物的用量改变而改变,但中和反应反应热不变
C.分多次把NaOH溶液倒入盛有稀盐酸的量热计的内筒中
D.玻璃搅拌器沿内筒壁顺时针移动,使酸碱溶液混合
3.下列有关热化学方程式的表示及说法正确的是
A.已知2H2(g)+O2(g)=2H2O(g) ∆H=-483.6 kJ∙ml-1,则氢气的燃烧热∆H=-241.8 kJ∙ml-1
B.25℃、101kPa时,C的燃烧热燃烧时生成稳定的CO2,S的燃烧热燃烧时生成稳定的SO3
C.含20gNaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+H2O(l) ∆H=-57.4kJ∙ml-1
D.已知 H2(g)+I2(g)=2HI(g) ∆H1,H2(g)+I2(s)=2HI(g) ∆H2,则△H1>△H2
4.在一定条件下,已知:C(s)+O2(g)═CO2(g)ΔH1
2C(s)+O2(g)═2CO(g)ΔH2 C(s)+CO2(g)═2CO(g)ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是( )
A.ΔH3=ΔH1+2ΔH2B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2D.ΔH3=ΔH2-ΔH1
5.NF3是一种温室气体,其存储能量的能力是CO2的12 000~20 000倍,在大气中的寿命可长达740年,如表所示是几种化学键的键能,下列说法中正确的是
A.过程N2(g)→2N(g)放出能量
B.过程N(g)+3F(g)→NF3(g)放出能量
C.反应N2(g)+3F2(g)=2NF3(g)为吸热反应
D.NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应
6.在密闭容器中进行A与B反应生成C的可逆反应,反应速率v(A)、v(B)、v(C)之间存在以下关系:v(C)=2v(A),3v(C)=2v(B),则该反应可以表示为
A.A(g)+B(g)⇌C(g)B.2A(g)+2B(g)⇌3C(g)
C.A(g)+3B(g)⇌2C(g)D.3A(g)+B(g)⇌2C(g)
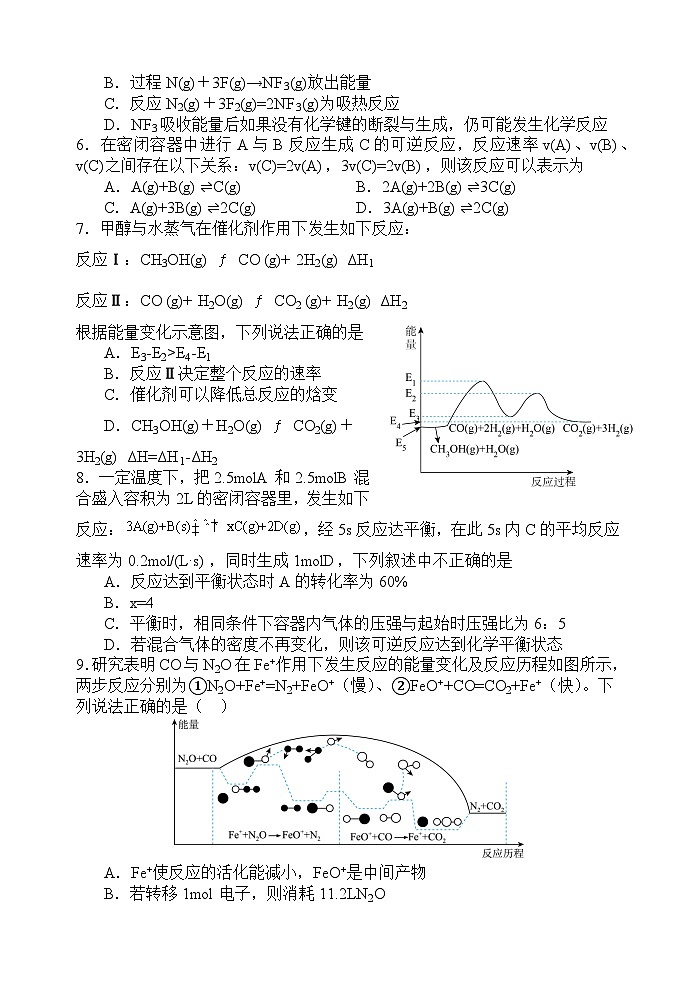
7.甲醇与水蒸气在催化剂作用下发生如下反应:
反应Ⅰ:CH3OH(g) CO (g)+ 2H2(g) ΔH1
反应Ⅱ:CO (g)+ H2O(g) CO2 (g)+ H2(g) ΔH2
根据能量变化示意图,下列说法正确的是
A.E3-E2>E4-E1
B.反应Ⅱ决定整个反应的速率
C.催化剂可以降低总反应的焓变
D.CH3OH(g)+H2O(g) CO2(g)+3H2(g) ΔH=ΔH1-ΔH2
8.一定温度下,把2.5mlA和2.5mlB混合盛入容积为2L的密闭容器里,发生如下反应:,经5s反应达平衡,在此5s内C的平均反应速率为0.2ml/(L·s),同时生成1mlD,下列叙述中不正确的是
A.反应达到平衡状态时A的转化率为60%
B.x=4
C.平衡时,相同条件下容器内气体的压强与起始时压强比为6:5
D.若混合气体的密度不再变化,则该可逆反应达到化学平衡状态
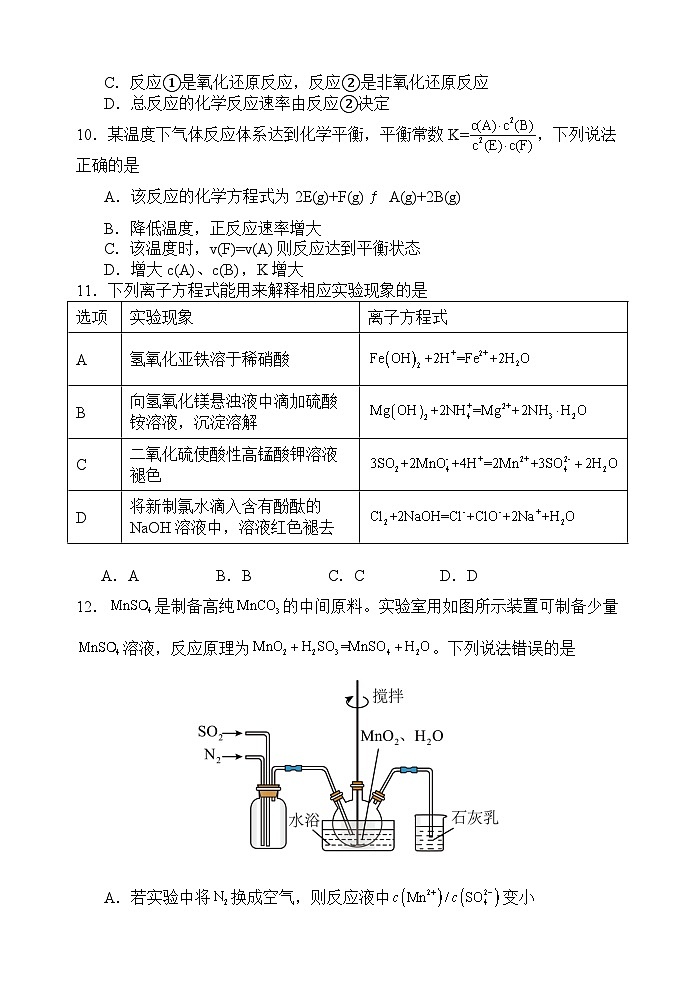
9.研究表明CO与N2O在Fe+作用下发生反应的能量变化及反应历程如图所示,两步反应分别为①N2O+Fe+=N2+FeO+(慢)、②FeO++CO=CO2+Fe+(快)。下列说法正确的是( )
A.Fe+使反应的活化能减小,FeO+是中间产物
B.若转移1ml电子,则消耗11.2LN2O
C.反应①是氧化还原反应,反应②是非氧化还原反应
D.总反应的化学反应速率由反应②决定
10.某温度下气体反应体系达到化学平衡,平衡常数K=,下列说法正确的是
A.该反应的化学方程式为2E(g)+F(g)A(g)+2B(g)
B.降低温度,正反应速率增大
C.该温度时,v(F)=v(A)则反应达到平衡状态
D.增大c(A)、c(B),K增大
11.下列离子方程式能用来解释相应实验现象的是
A.AB.BC.CD.D
12.是制备高纯的中间原料。实验室用如图所示装置可制备少量溶液,反应原理为。下列说法错误的是
A.若实验中将换成空气,则反应液中变小
B.在该反应中作催化剂
C.若不通,则烧瓶中的进气管口容易被堵塞
D.石灰乳对尾气的吸收效果比澄清石灰水更好
13.某有机物的结构简式如图所示,则该有机物不可能具有的性质是
①可以燃烧 ②能使酸性溶液褪色 ③能与溶液反应 ④能发生酯化反应 ⑤能发生加成反应 ⑥能发生水解反应
A.只有①②B.只有①④C.只有⑤D.只有⑥
14.T ℃时,向某恒温恒容密闭容器中充入等物质的量的CH4(g)和CO2(g),发生二氧化碳重整甲烷反应:CH4(g)+CO2(g) 2CO(g)+2H2(g),测得体系中CH4(g)和CO(g)的物质的量浓度随时间变化如图所示,下列说法错误的是
A.点B的坐标为(5,)
B.反应进行到5 min时,2v正(CH4)<v逆(CO)
C.CO2(g)的平衡转化率约为33.3%
D.T ℃时,该反应的平衡常数为
二、非选择题(本题共 4 个大题,每空2分,标注除外,共 58 分)
15.(14分)回答下列问题:
(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、 、 。
(2)量取反应物时,取50 mL 0.50 ml·L-1的盐酸,还需加入的试剂是 (1分) (填序号)。
A.50 mL 0.50 ml·L-1NaOH溶液 B.50 mL 0.55 ml·L-1NaOH溶液 C.1.0 g NaOH固体
(3)倒入 NaOH 溶液的正确操作是 (1分)(填序号)。
A.沿玻璃棒缓慢倒入B.分三次少量倒入C.一次迅速倒入
(4)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如下表所示。
①甲在实验之前预计ΔH1=ΔH2.他的根据是 ;乙在实验之前预计ΔH1≠ΔH2,他的根据是 。
②实验测得的温度是:A的起始温度为13.0℃、终了温度为19.8℃;设充分反应后溶液的比热容c=4.184 J·(g·℃)-1,忽略实验仪器的比热容及溶液体积的变化,则ΔH1= ;(已知溶液密度均为1 g·cm-3)
(5)若用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,测得的中和反应热数值会_______(填“偏大”、“偏小”或“无影响”)。
16.(14 分)利用化学原理对废气、废水进行脱硝、脱碳处理,可实现绿色环保、废物利用,对构建生态文明有重要意义。
Ⅰ.脱硝:(1)H2还原法消除氮氧化物
已知:N2(g)+2O2(g)=2NO2(g) ΔH1=+133kJ/ml
H2O(g)=H2O(l) ΔH2=-44kJ/ml H2的燃烧热ΔH3=-285.8kJ/ml
在催化剂存在下,H2还原NO2生成水蒸气和氮气的热化学方程式为 。
(2)用NH3催化还原法消除氮氧化物,发生反应:
4NH3(g)+6NO(g)5N2(g)+6H2O(l) ΔH<0
相同条件下,在2L恒容密闭容器中,选用不同催化剂,产生N2的量随时间变化如图所示。
①计算0~4分钟在A催化剂作用下,反应速率v(NO)= 。
②下列说法正确的是 。
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已达到平衡
D.若反应在恒容绝热的密闭容器中进行,当K值不变时,说明已达到平衡
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3=7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH (填“增大”“减小”或“不变”),负极的电极反应式为 。
(4)汽车尾气里含有的 NO 气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
,已知该反应在 T ℃时,平衡常数 K=9.0。请回答: 该反应的平衡常数表达式为:K= ;
下列为 4 种不同情况下测得的反应速率中,表明该反应进行最快的是 ;
17.(15分)碳达峰是指我国承诺2030年前,二氧化碳的排放不再增长。因此,诸多科学家都在大力研合理利用和CO以减少碳的排放。
(1)可通过以下4种方式转化成有机物,从而有效实现碳循环。
a.
b.
c.
已知:
以上反应中,最环保节能的是 (1分),原子利用率最高的是 (1分)。(填编号)
(2)我国科学家设计出一条仅11步的工业合成路线,实现了到淀粉的合成。其第一步是把还原为甲醇(),该方法的化学方程式是: 。回答下列问题:
①能说明该反应已达平衡状态的是 (填字母)。
A.单位时间内生成的同时消耗了
B.在恒温恒容的容器中,混合气体的平均摩尔质量保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,混合气体的密度不再变化
②该反应正逆反应的活化能大小为:Ea(正) Ea(逆)(填“>”、“=”或“<”)
(3)利用CO高温时与磷石膏()反应,可减少CO的排放,又可以实现硫酸盐资源的再利用。已知该反应的产物与温度有关。
①在700℃时,主要的还原产物是一种硫的最低价盐,该物质为 (填化学式)。
②在1150℃时,向盛有足量的真空恒容密闭容器中充入一定量CO,反应体系起始压强为,主要发生反应:。该反应达到平衡时,,CO的转化率为50%,则初始时 _____ml/L,该反应的压强平衡常数 MPa(3分)(忽略副反应;气体分压=总压×气体物质的量分数)。
工业上也可用炭粉还原磷石膏,该反应的产物与C/S值(炭粉与的物质的量之比)有关。向密闭容器中加入几组不同C/S值的炭粉与磷石膏的混合物,1100℃煅烧至无气体产生,结果如图所示。当C/S值为0.5时,反应产物主要为CaO、和;当C/S值大于0.7时,反应所得气体中的体积分数下降,可能的原因是 。
18.(15分)锗是一种重要的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。下图为工业上利用湿法炼锌渣(主要含有GeO2、ZnO、FeO、Fe2O3、SiO2)制备高纯锗的工艺流程:
已知:①GeO2为两性化合物。
②常温下,部分金属阳离子转化为氢氧化物沉淀的pH见下表。
③有机试剂丹宁沉淀金属离子的沉淀率见下表。
(1)“浸出”时加热的目的是 ;浸出渣的主要成分是 (填化学式)。
(2)浸出后加入NaClO溶液的作用是 。
(3)“滤液2”中主要含有的金属阳离子是 (填离子符号)。
(4)GeCl4与高纯水反应的化学方程式为 (3分)。
(5)I2的一种制备方法如下图所示:
加入Fe粉进行转化反应的离子方程式为 ,生成的沉淀与硝酸反应,生成 后可循环使用。化学键
N≡N
F-F
N-F
键能/kJ·ml-1
946
154.8
283.0
选项
实验现象
离子方程式
A
氢氧化亚铁溶于稀硝酸
B
向氢氧化镁悬浊液中滴加硫酸铵溶液,沉淀溶解
C
二氧化硫使酸性高锰酸钾溶液褪色
D
将新制氯水滴入含有酚酞的NaOH溶液中,溶液红色褪去
反应物
起始温度
t1/℃
终了温度
t2/℃
中和热
/kJ·ml-1
A.1.0 ml·L-1HCl溶液50 mL、1.1 ml·L-1NaOH溶液50 mL
13.0
ΔH1
B.1.0 ml·L-1HCl溶液50 mL、1.1 ml·L-1NH3·H2O溶液50 mL
13.0
ΔH2
离子
Fe2+
Fe3+
Zn2+
Ge4+
开始沉淀pH
7.5
2.2
6.2
8.2
完全沉淀pH
9.0
3.2
8.2
11.2
离子
Fe2+
Fe3+
Zn2+
Ge4+
沉淀率(%)
0
99
0
97~98.5
四川省蓬溪中学校2023-2024学年高二上学期10月月考化学试题含答案: 这是一份四川省蓬溪中学校2023-2024学年高二上学期10月月考化学试题含答案,共24页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
四川省蓬溪中学2023-2024学年高二上学期10月月考化学试题(Word版附解析): 这是一份四川省蓬溪中学2023-2024学年高二上学期10月月考化学试题(Word版附解析),共19页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
四川省蓬溪中学2023-2024学年高二化学上学期开学考试试题(Word版附解析): 这是一份四川省蓬溪中学2023-2024学年高二化学上学期开学考试试题(Word版附解析),共17页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。












