许昌市高二下学期第四次月考化学试卷及答案
展开许昌市三校联考高二下学期第四次考试
化学试卷
(时间90分钟,分值100分)
本试卷分为第I卷(选择题)和第II卷(非选择题)两部分。请将答案答在答题卡上,在本试卷上答题无效。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Al 27
第I卷 选择题
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要
求)
1.化学与生产、生活、社会密切相关,下列说法错误的是
A.绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物
B.加工后具有吸水性的植物纤维可用作食品干燥剂
C.臭氧、高锰酸钾溶液、次氯酸钠溶液、乙醇溶液均可用于消毒杀菌,且原理相同
D.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生相关
2.下列物质分类正确的是
A.SO2、SiO2、CO均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体[来源:Zxxk.Com]
C.烧碱、冰醋酸、四氯化碳均为电解质
D.福尔马林、水玻璃、氨水均为混合物
3.用NA表示阿状加德罗常数,下列说法正确的是
A.78g Na2O2与足量水反应中电子转移了0.2NA
B.60g丙醇中存在的共价键总数为10NA
C.分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有(不含立体异构)4种
D.1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
4.下列推断正确的是
A.SiO2、NO2都能与NaOH溶液反应,都是酸性氧化物,
B.Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C.为增大氯水中c(HClO),应采取的措施是加入CaCO3固体
D.铁、铝容器常温下可盛放浓硫酸,是因为常温下铁、铝与浓硫酸不反应
5.下列离子方程式不正确的是
A.向硫酸氢钠溶液中滴加Ba(OH)2溶液恰好至中性:
2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.等物质的量浓度的FeI2溶液与溴水等体积混合:
2Fe2++2I-+2Br2=2Fe3++I2+4Br-
C.用惰性电极电解CuSO4溶液:2Cu2++2H2O2Cu+O2↑+4H+
D.硫氢化钠水解:HS-+H2O H2S+OH-
6.改变反应物用量,下列反应能用同一个反应方程式表示的是
①NaAlO2溶液与CO2反应; ②Si与烧碱溶液反应; ③H2S与NaOH溶液反应;
④Fe与稀硝酸反应; ⑤S在O2中燃烧; ⑥NH3与O2的反应
A.②⑤⑥ B.①②③⑤ C.①③④⑥ D.①③④⑤⑥
7.下列说法正确的是
A.将15.6 g Na2O2和5.4 g Al同时放入一定量的水中可以产生标况下气体6.72 L
B.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该气体能使品红溶液褪色,
则该溶液可能既含有SO32-又含有CO32-
C.大多数碳的化合物都是共价化合物,其原因是碳元素有三种同位素
D.石油分馏可获得乙烯、丙烯和丁二烯
8.常温下,在pH值为4的FeCl3溶液、pH值为10的Na2CO3溶液和pH值为2的盐酸溶液
中,水的电离度分别为α1、α2和α3,则它们的关系为
A. α1=α2>α3 B. α1<α2<α3 C. α1>α2>α3 D. 无法判断
9.在500℃时,把0.3mol SO2和0.2mol O2充入一个体积为10L并盛有V2O5(催化剂)的
真空密闭容器中,保持温度不变,经2min后,容器内的压强不再变化,此时容器内
压强减小20%。下列说法正确的是
A.该温度下此反应的平衡常数K=400
B.其他条件不变,再充入0.3mol SO2和0.2mol O2平衡时,SO2的体积分数增大
C.平衡时,SO2的转化率为95%
D.前2min SO2的平均反应速率0.02mol/(L·s)
10.将铂电极置于KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流,下列叙述
正确的是
A.通入CH4的电极为正极
B.正极的电极反应式为O2+4H++4e-=2H2O
C.通入CH4的一极的电极反应式为CH4+2O2+4e-=CO2+2H2O
D.负极的电极反应式为CH4+10OH--8e-=CO32-+7H2O
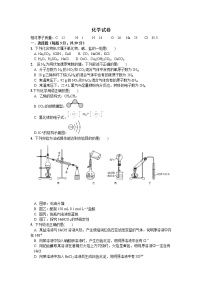
11.利用右图所示装置进行下列实验,能得出相应实验结论的是
选项 | ①[来源:Z。xx。k.Com] | ② | ③ | 实验结论 | [来源:学科网ZXXK] |
A | 稀硝酸 | Na2S | AgNO3与[来源:学#科#网] AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
B | 浓硫酸 | 无水 乙醇 | 溴水 | 有乙烯生成 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
D | 稀硫酸 | Na2CO3 | Na2SiO3 溶液 | 酸性: 稀硫酸>碳酸>硅酸 |
12.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),相关数据如下
表:
实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
下列判断不正确的是
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= mol·L—1
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)
13.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到2mol乙酸和1mol醇,该醇的
分子式为
A.C14H18O5 B.C14H22O3 C.C14H22O5 D.C14H10O5
14.下列化合物中同分异构体数目最少的是
A.乙酸乙酯 B.戊醇 C.戊烷 D.戊烯
第II卷 非选择题
二、非选择题:本题共5小题,共58分,分为必做题和选做题。其中15-17为必做题;
18-19为选做题,请考生根据要求作答。
15.(8分)X、Y、Z、W、H为原子序数依次增大的五种短周期元素,它们满足以下条件:
元素周期表中,Z与Y相邻,Z与W也相邻; Y、Z和W三种元素的原子最外层电子数
之和为17;H的单质常温下为黄绿色气体。请填空:
(1)Z、W、H简单阴离子的半径由大到小的顺序是____________(用离子符号表示)
(2)H的单质通入W的氢化物的水溶液中,可观察到有淡黄色沉淀生成,该现象说明
H与W单质的氧化性强弱顺序为____________(用化学式表示)
(3)写出实验室制取H的单质的化学反应方程式________________
(4)X、Y、Z和W可组成一化合物,其原子个数之比为8︰2︰4︰1。其水溶液中各
种离子的浓度由大到小的顺序为____________
16.(10分)现有A、B、C、D、E五种中学教材中常见的金属单质,其单质和最高价氧化物
对应的水化物的有关信息如下表所示:
单质 | A | B | C | D | E |
最高价氧化物 对应水化物的稳定性 | 难分解 | 能分解 | 能分解 | 能分解 | 能分解 |
单质性质 | 与水剧烈反应 | 缓慢溶于热水 | 溶于强碱性溶液 | 难溶于冷的浓硝酸 | 溶于浓、稀硝酸 |
已知A、B、C的组成元素位于同一短周期,D和E的组成元素位于同一周期,D的低
价氢氧化物在空气中会发生颜色变化,E在空气中生锈呈绿色。
根据要求,回答下列问题:
(1)C元素最高价氧化物对应的水化物既能与酸反应,又能与碱反应,原因分别是:
__________________;________________(用电离方程式表示)
(2)以B、C为电极,A的氢氧化物的水溶液为电解质溶液,构成原电池。写出C极
的电极反应式:________________________。
(3)用离子方程式表示D的单质能与D的化合物在水溶液中发生化合反应:______________________
(4)E的单质在加热条件下能与浓硫酸反应,其反应的化学方程式为
____________________________
17.(10分)(1)(4分)甲醇是重要的化工原料,又可做燃料。利用合成气(主要成
分为CO、CO2和H2)在催化剂的作用下合成甲醇,主要反应如下:
①CO(g)+2H2(g)CH3OH(g) △H1
②CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H2= -58 kJ/mol
③CO2(g)+H2(g)CO(g)+H2O(g) △H3
已知反应①中的相关的化学键键能数据如下:
化学键 | H-H | C-O | CO (CO中的化学键) | H-O | C-H |
E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
回答下列问题:
①△H3=_____kJ/mol
②25℃,101 kPa条件下,测得16g甲醇完全燃烧释放出Q kJ的热量,请写出表示
甲醇燃烧热的热化学方程式_______________
(2)(3分)25℃,将a mol·L-1氨水与b mol·L-1盐酸等体积混合后溶液呈中性,
则此时溶液中c(NH4+)__________c(Cl-)(填“>”、“<”或“﹦”);用含a、b
的代数式表示该温度下NH3·H2O的电离平衡常数Kb = _________
(3)(3分)800℃时,在2L密闭容器中发生反应2NO(g)+O2(g) 2NO2(g),在反
应体系中,n(NO)随时间的变化如下表所示:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①下图中表示NO2变化的曲线是___________
用O2表示从0~2s内该反应的平均速率v=____
②能说明该反应已经达到平衡状态的是_______
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内的密度保持不变
以下为选做题。请考生从A、B两组中选一组作答,在答题卡中做好标记,若两组都做,则按第一组评分。
选做题 A组 选修3 物质结构与性质
18.(10分)A、B、C、D四种元素的原子序数依次递增,A、B的基态原子中L层未成对
电子数分别为3、2,C在短周期主族元素中电负性最小,D元素被称为继铁、铝之后
的第三金属,其合金多用于航天工业,被誉为“21世纪的金属” ,其基态原子外围
电子占据两个能级且各能级电子数相等。请回答下列问题:
(1)A、B、C三种元素的第一电离能由小到大的顺序是_______(填元素符号)。
(2)D元素基态原子的核外电子排布式为____________________。
(3)白色晶体C3AB4中阴离子的空间立体构型是_______,中心原子的杂化方式是_____
(4)中学化学常见微粒中与A2B互为等电子体的分子有__________(任写一种即可)。
(5)已知D3+可形成配位数为6的配合物。现有组成皆为DCl3·6H2O的两种晶体,一
种为绿色,另一种为紫色。为测定两种晶体的结构,分别取等量样品进行如下
实验:①将晶体配成水溶液,②滴加足量AgNO3溶液,③过滤出AgCl沉淀并进
行洗涤、干燥、称量;经实验测得产生的沉淀质量:绿色晶体是紫色晶体的2/3。
依据测定结果可知绿色晶体的化学式为_______________,该晶体中含有的化学
键有__________
a.离子键 b.极性键 c.非极性键 d.配位键
19.(20分)A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、 D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最小的是________(填元素符号),其中C原子的外围电子排
布图为________。
(2)A和B的氢化物所属的晶体类型分别为_________和_________。
(3)B、C均可以与D形成化合物,其中熔点较高的是____(用化学式表示)
(4)A和B可形成1:1型的化合物E,E的电子式为_____
(5)化合物D2A的立体构型为_________,中心原子的孤电子对数为_________,单质
D与湿润的Na2CO3反应可制备D2A,其化学方程式为_______________。
(6)A和B能够形成化合物F,其晶胞结构如右图所示,
晶胞边长为0.566nm, F 的化学式为______;晶胞
中A 原子的配位数为______;晶体F的密度
=______g.cm-3(只列式,不计算)
选做题 B组 选修5 有机化学基础
18.(14分)煤的“气化”是使煤变成洁净能源的有效途径之一,其主要反应为:
C + H2OCO + H2,甲酸苯异丙酯(F)是生产香料和药物的重要原料。下图是用煤为原料合成甲酸苯异丙酯的路线图(部分反应条件和生成物已略去),其中D的分子式为C9H10O,且能发生银镜反应。
根据上述转化关系回答下列问题:
(1)写出B、D的结构简式:B:_______________ D:________________
(2)D→E的反应类型为:_________________
(3)B与新制Cu(OH)2悬浊液反应也能生成C,写出其化学方程式________________
(4)写出C与E反应生成F的化学方程式:_______________________
(5)F有多种同分异构体,写出满足下列条件的两种同分异构体的结构简式
_________________、 _______________________。
①属于酯类, 且能发生银镜反应
②苯环上的一氯代物只有两种
③分子中只有两个甲基
19.(16分)有机化合物G是合成维生素类药物的中间体,其合成路线如下:
其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去
已知G为:
请回答下列问题:
(1)G的分子式_____________;D中官能团的名称是_________。
(2)第②步反应的化学方程式为__________________________。
(3)第③步反应的化学方程式为__________________________。
(4)写出F的结构简式_____________。
(5)第①~⑥步反应中属于加成反应的有___________________;属于取代反应的有
__________________________。(填步骤编号)
(6)同时满足下列条件的E的同分异构体有_____________种。
①只含一种官能团;
②链状结构且无—O—O—;
③核磁共振氢谱只有2组峰。
许昌市三校联考高二下学期第四次考试 化学答案
第I卷 选择题
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 |
答案 | C | D | C | C | B | A | B | A | A | D | D | B | B | C |
第II卷 非选择题
15.(8分)(每空2分)
(1)S2->Cl->O2-
(2)Cl2>S
(3)MnO2+4HCl (浓)MnCl2+Cl2↑+2H2O
(4)c(NH4+)>c(SO42-)>c(H+)>c(OH-)
16.(10分)(每空2分)
(1)Al(OH)3Al3++3OH-;Al(OH)3H++AlO2-+H2O
(2)Al-3e-+4OH-= AlO2-+2H2O
(3)Fe+2Fe3+=3Fe2+
(4)Cu+2H2SO4 (浓)CuSO4+SO2↑+H2O
17.(10分)
(1)①+41(2分)
②CH3OH(l)+3/2 O2(g)=CO2+2H2O △H=-2QkJ/mol(2分)
(2) =(1分) ; b×10-7/(a-b)(2分)
(3))①b (1分); 1.5×10-3mol/(L·s) (1分) (2)bc (1分)
选做题 A组 选修3 物质结构与性质
18.(10分)
(1)Na<O<N(1分)
(2)[Ar]3d24s2(1分)
(3)正四面体(1分) sp3(1分)
(4)CO2 或CS2 (2分)
(5)[Ti(H2O)5Cl]Cl2·H2O(2分); abd(2分)多选少选漏选均不得分
19. (20分)
(1)Na(1分); (1分)
(2)分子晶体(1分) 离子晶体(1分)
(3)NaCl(2分)
(4)(2分)
(5)V形(2分);2(2分);
2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl(2分)
(6)Na2O(2分);8(2分);
(用NA表示也可)(2分)
选做题 B组 选修5 有机化学基础
18.(14分)(1)HCHO (2分) (2分)
(2)加成反应(2分)
(3)HCHO + 2Cu(OH)2HCOOH +Cu2O↓+ 2H2O (2分)
(4)(2分)
(5)写出其中的两种即可(4分,写对一个得2分)
19.(16分)(1)C6H10O3(2分)酯基、醛基、羟基(2分)多写、漏写、写错均不得分
(2)(2分)
(3)(2分)
(4)(2分)
(5)①④(2分)、②⑤(2分) (漏写得一分,写错不得分)
(6)3(2分)
不用注册,免费下载!
邢台一中高二第四次月考化学试题及答案: 这是一份邢台一中高二第四次月考化学试题及答案,共6页。试卷主要包含了5NA,585,4a3d) B等内容,欢迎下载使用。
全国高中学生化学竞赛(决赛)理论试题14版: 这是一份全国高中学生化学竞赛(决赛)理论试题14版,共7页。
安徽省宣城市泾县重点中学2022-2023学年高一下学期竞赛选拔化学试题含解析: 这是一份安徽省宣城市泾县重点中学2022-2023学年高一下学期竞赛选拔化学试题含解析,共19页。试卷主要包含了单选题等内容,欢迎下载使用。