


高考化学一轮复习跟踪检测5原子结构化学键 含解析
展开![]() 原子结构 化学键
原子结构 化学键
1.具有广泛用途的 Co放射源首次实现了国内批量生产。另外,钴还有多种原子,如 Co、Co、Co和 Co。下列关于钴原子的说法正确的是( )
A.Co、Co、Co、Co和 Co是摩尔质量不同的五种同素异形体
B.Co放射源可以用来治疗癌症,其中子数与电子数之差等于6
C.Co、Co、Co、Co和 Co互为同位素,物理性质几乎相同,化学性质不同
D.Co、Co、Co、Co和 Co互为同分异构体
解析:选B Co、Co、Co、Co和 Co互为同位素,物理性质不同,化学性质几乎完全相同,A、C、D错误;Co 的中子数为60-27=33,与电子数之差为33-27=6,B正确。
2.下列化学用语的表述正确的是( )

C.CO2的分子示意图:![]()
D.次氯酸的结构式:H—Cl—O
解析:选A B项,NaClO的电子式应为![]() C项,碳原子半径应大于氧原子半径;D项,HClO的结构式应为H—O—Cl。
C项,碳原子半径应大于氧原子半径;D项,HClO的结构式应为H—O—Cl。
3.由德国重离子研究中心人工合成的第112号元素的正式名称为“Copemicium”,相应的元素符号为“Cn”,该元素的名称是为了纪念天文学家哥白尼而得名。该中心人工合成Cn的过程可表示为 Zn+Pb === Cn+n。下列叙述中正确的是( )
A.上述合成过程属于化学变化
B.Cn元素的相对原子质量为277
C.Cn 的原子核内中子数比质子数多53
D.Cn元素位于元素周期表的第六周期,是副族元素
解析:选C A项,化学变化的最小粒子为原子,该反应中原子类型发生了变化,不属于化学变化,错误;B项,该Cn原子的相对原子质量为277,元素的相对原子量与该元素不同核素的相对原子量和在自然界中的含量有关,错误;C项,该原子的中子数=277-112,中子数比质子数多的数目为277-112-112=53,正确;D项,第118号元素位于周期表中第七周期0族,则112号元素位于第七周期第ⅡB 族,错误。
4.下列说法中正确的是( )
A.Na2S2、NaClO中所含化学键类型完全相同
B.只有活泼金属元素与活泼非金属元素之间才能形成离子键
C.等物质的量的CN-和N2含有的共用电子对数相等
D.氯气与NaOH反应的过程中,同时有离子键、极性键和非极性键的断裂和形成
解析:选C A项,Na2S2中含有离子键和非极性键,NaClO中含有离子键和极性键,错误;B项,NH4Cl中含有离子键,但它是由非金属元素形成的,错误;C项,CN-电子式为![]() N2电子式为
N2电子式为![]() 当物质的量相等时,两者含有的共用电子对数相等,正确;D项,根据反应:2NaOH+Cl2===NaCl+NaClO+H2O,反应过程中有离子键、极性键的断裂和形成,但只有非极性键的断裂,没有非极性键的形成,错误。
当物质的量相等时,两者含有的共用电子对数相等,正确;D项,根据反应:2NaOH+Cl2===NaCl+NaClO+H2O,反应过程中有离子键、极性键的断裂和形成,但只有非极性键的断裂,没有非极性键的形成,错误。
5.固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体的最外电子层结构,则下列有关说法不正确的是( )
A.1 mol NH5中含有5NA个N—H键(NA表示阿伏加德罗常数)
B.NH5中既有共价键又有离子键

D.它与水反应的离子方程式为NH+H-+H2O===NH3·H2O+H2↑
解析:选A NH5的所有原子的最外层都符合相应稀有气体的最外电子层结构,则NH5属于铵盐,电子式为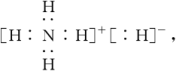 1 mol NH5中含有4NA个N—H键,既含有共价键又含有离子键,A错误,B、C正确;D项,NH5和H2O发生氧化还原反应生成NH3·H2O和H2,离子方程式为NH+H-+H2O===NH3·H2O+H2↑,D正确。
1 mol NH5中含有4NA个N—H键,既含有共价键又含有离子键,A错误,B、C正确;D项,NH5和H2O发生氧化还原反应生成NH3·H2O和H2,离子方程式为NH+H-+H2O===NH3·H2O+H2↑,D正确。
6.已知X、Y、Z三种元素的原子序数依次增大,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态化合物,则下列说法错误的是( )
A.Y和Z可以组成一种Y和Z的质量比为7∶8的化合物
B.X、Y、Z组成的盐中既含离子键又含共价键
C.X和Z可以组成原子个数比分别为1∶1和2∶1,常温下为液态的两种化合物
D.由X、Y、Z三种元素中的任意两种组成的具有10电子的粒子仅有2种
解析:选D 由X原子的电子层数与它的核外电子总数相等知,X为氢元素;Z原子的最外层电子数是次外层的3倍,则Z为氧元素;与氧可形成两种以上气态化合物的Y为氮元素。N、O可形成化合物NO,A项正确;H、N、O组成的盐有NH4NO3、NH4NO2等,既含离子键又含共价键,B项正确;H、O两元素可形成H2O、H2O2两种液态化合物,C项正确;H、N、O组成的10电子微粒有多种,如NH、NH3、H2O、H3O+、OH-等,D项不正确。
7.X是第三周期非金属元素,该原子如果要达到8电子稳定结构,需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是( )
A.X最高价氧化物对应的水化物一定是强酸
B.X元素的氢化物化学式一定为H2X
C.X的单质一定是良好的半导体材料
D.X元素的氧化物一定能与烧碱反应
解析:选D A项,根据已知位、构、性方面的信息推断,X为Si或S,最高价氧化物对应的水化物为H2SiO3或H2SO4,前者是弱酸,后者是强酸,错误;B项,气态氢化物为SiH4或H2S,错误;C项,单质为Si或S,前者是半导体材料,后者是绝缘体材料,错误;D项,氧化物为SiO2或SO2、SO3,都是酸性氧化物,正确。
8.X、Y、Z均为短周期主族元素,其核电荷数依次增大,且它们的原子最外层电子数之比为1∶4∶2。下列叙述中正确的是( )
A.X一定是碱金属元素
B.Y元素能形成化合物NaHYO3,且其水溶液呈碱性
C.Z元素形成的最高价氧化物熔点较低
D.X的单质一定能通过电解Z的盐酸盐溶液制备
解析:选B X、Y、Z均为短周期主族元素,其核电荷数依次增大,且它们的原子最外层电子数之比为1∶4∶2,应分别是第ⅠA族、第ⅣA族、第ⅡA族,其可能是H或Li、C和Mg元素。A项,X不一定是碱金属元素,错误;C项,氧化镁的熔点较高,错误;D项,H2可以通过电解MgCl2溶液制取,但Li不可以,错误。
9.设X、Y、Z代表元素周期表中前四周期的三种元素,已知X+和Y-具有相同的电子层结构;Z元素的原子核内质子数比Y元素的原子核内质子数少9;Y和Z两种元素可形成含4个原子核、42个电子的负一价阴离子。下列说法不正确的是( )
A.元素Z的气态氢化物分子中含有10个电子
B.元素Y的气态氢化物分子中含有18个电子
C.元素Z与元素X形成的化合物X2Z中离子都达到稳定结构
D.元素Y、Z组成的化合物属于离子化合物
解析:选D 由“X+和Y-具有相同的电子层结构”知X+和Y-的最外层都是8电子,推知X为第ⅠA族元素、Y为第ⅦA族元素;又因“Z元素的原子核内质子数比Y元素的原子核内质子数少9”,故Y为Cl、Z为O、X为K。水分子中含有10个电子,氯化氢分子中含有18个电子,K2O中的K+、O2-均达到最外层8电子稳定结构。氯、氧组成的化合物为共价化合物。
10.A、B、C、D、E是原子序数依次增大的五种短周期元素且B、C相邻,A元素可以与B、C、E元素分别形成甲、乙、丙三种物质,且甲、乙均为10电子化合物,丙为18电子化合物。D元素的最外层电子数与核外电子层数相等。已知:甲+E2===丙+B2,甲+丙===丁,下列说法正确的是( )
A.离子半径:D>C>B
B.A与C两种元素共同形成的10电子粒子有3种
C.D元素在周期表中的位置可以是第二周期第ⅡA族
D.丁物质均由非金属元素构成,只含共价键
解析:选B 由题目信息可判断出A为氢元素;10电子化合物可能为甲烷、氨气、水、HF,已知甲+E2===丙+B2,甲+丙===丁,则E为氯元素,B为氮元素;由B、C相邻知C为氧元素,故甲为NH3、乙为H2O、丙为HCl、丁为NH4Cl;D元素的最外层电子数与核外电子层数相等,原子序数大于氧元素,处于第三周期,最外层电子数为3,故D为铝元素。A项,N3-、O2-、Al3+电子层结构相同,核电荷数越大离子半径越小,故离子半径:N3->O2->Al3+,错误;B项,H与O两种元素可形成的10电子粒子有H2O、H3O+、OH-三种,正确;C项,Al元素位于第三周期第ⅢA 族,错误;D项,NH4Cl含有离子键、共价键,错误。
11.现有部分短周期主族元素的性质或原子结构如下表所示:
元素编号 | 元素性质或原子结构 |
X | 周期序数=主族序数=原子序数 |
Y | 原子最外层电子数为a,次外层电子数为b |
Z | 原子L层电子数为a+b,M层电子数为a-b |
M | 单质在自然界中的硬度最大 |
N | 位于第三周期,最外层电子数是电子层数的2倍 |
(1)写出X、Y、Z、N四种元素的名称:
X________,Y________,Z________,N________。
(2)由X、Y、Z、M、N五种元素两两组成的分子中,许多分子含有的电子数相等,写出符合下列要求的分子式:
①含10e-且呈正四面体结构的分子________;
②含14e-的双原子分子________;
③含16e-且能使溴水褪色的分子________;
④含18e-且常温下呈液态的分子________。
解析:(1)根据周期序数=主族序数=原子序数,推知X为氢元素;根据电子数L层=a+b,M层=a-b,最外层为a,次外层为b,得出b=2,a=6,从而推得Y、Z分别为氧元素、硅元素;金刚石在自然界中的硬度最大,故M为碳元素,N的最外层电子数是电子层数的2倍,则推得N为硫元素。(2)①CH4为正四面体分子,②CO为双原子14e-分子,③乙烯能和溴水发生加成反应,使溴水褪色,④H2O2 在常温下为18e-的液态分子。
答案:(1)氢 氧 硅 硫
(2)①CH4 ②CO ③C2H4 ④H2O2
12.现有部分元素的原子结构特点如表:
X | L层电子数是K层电子数的3倍 |
Y | 核外电子层数等于原子序数 |
Z | L层电子数是K层和M层电子数之和 |
W | 最外层电子数是次外层电子数的2.5倍 |
(1)画出W原子结构示意图________________________。
(2)元素X与元素Z相比,非金属性较强的是________(填元素名称),写出一个能表示X、Z非金属性强弱关系的化学反应方程式:_____________________________________。
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为____________________。
(4)元素X和元素Y以原子个数比1∶1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的、且在自然界中稳定存在的物质,写出该反应的化学方程式:________________________________________________________________________。
解析:X元素原子的L层电子数是K层电子数的3倍可知,L层为6个电子,X为氧元素;Y元素原子的核外电子层数等于原子序数,Y只能是氢元素;Z元素原子的L层电子数是K层和M层电子数之和,L层有8个电子,则其M层电子数为6,Z是硫元素;W元素原子的最外层电子数是次外层电子数的2.5倍,其次外层只能是K层,有2个电子,W为氮元素。(1)W(N)原子结构示意图为![]() 。(2)O2可置换H2S中的S,能说明氧元素比硫元素非金属性强。(3)H、N、O、S四种非金属元素形成离子化合物只能是铵盐,其水溶液显强酸性应是强酸的酸式盐,因为铵盐水解酸性不如其酸式盐溶液酸性强,故应为NH4HSO4。(4)H和O按原子个数比1∶1化合形成的化合物为H2O2,共有18个电子,则H和N形成的18电子微粒只能是N2H4,H2O2与N2H4反应生成无毒且在自然界中稳定存在的物质为N2和H2O,反应的化学方程式为N2H4+2H2O2N2+4H2O。
。(2)O2可置换H2S中的S,能说明氧元素比硫元素非金属性强。(3)H、N、O、S四种非金属元素形成离子化合物只能是铵盐,其水溶液显强酸性应是强酸的酸式盐,因为铵盐水解酸性不如其酸式盐溶液酸性强,故应为NH4HSO4。(4)H和O按原子个数比1∶1化合形成的化合物为H2O2,共有18个电子,则H和N形成的18电子微粒只能是N2H4,H2O2与N2H4反应生成无毒且在自然界中稳定存在的物质为N2和H2O,反应的化学方程式为N2H4+2H2O2N2+4H2O。
答案:(1)![]()
(2)氧 2H2S+O2===2H2O+2S↓(其他合理答案亦可)
(3)NH4HSO4
(4)N2H4+2H2O2N2+4H2O
13.原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2离子化合物。
(1)写出Y2O2的电子式:______________________________________________________,
其含有的化学键是____________。
(2)用电子式表示Y2O的形成过程:_____________________________________________。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶液氧化性最强的是________(填化学式)。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是________________(填化学式)。
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式:__________________________________。
解析:根据短周期元素Y可形成Y2O和Y2O2两种离子化合物可判断,Y为Na,由分子式XH3、H2Z和HW可知,X、Z、W分别属于ⅤA、ⅥA、ⅦA三个主族,再由原子序数的关系判断,X、Z、W分别为N、S、Cl。
答案:(1) ![]() 离子键、共价键
离子键、共价键
(2)![]()
(3)HNO3 (4)NH3
(5)NCl3+3H2O===3HClO+NH3
高考化学一轮复习讲练 第5章 第17讲 原子结构 化学键 (含解析): 这是一份高考化学一轮复习讲练 第5章 第17讲 原子结构 化学键 (含解析),共21页。试卷主要包含了了解元素、核素和同位素的含义,电子式的书写方法,5倍,推出W为N等内容,欢迎下载使用。
2022年高考化学一轮复习讲义第5章第27讲 原子结构 化学键 (含解析): 这是一份2022年高考化学一轮复习讲义第5章第27讲 原子结构 化学键 (含解析),共18页。试卷主要包含了了解元素、核素和同位素的含义,“等电子”微粒的判断与应用等内容,欢迎下载使用。
2022高考化学一轮复习专练23原子结构与化学键含解析: 这是一份2022高考化学一轮复习专练23原子结构与化学键含解析,共9页。试卷主要包含了单项选择题,不定项选择题,非选择题等内容,欢迎下载使用。












