


高考化学一轮复习跟踪检测4氧化还原反应 含解析
展开![]() 氧化还原反应
氧化还原反应
1.分析生产生活中的下列过程,不涉及氧化还原反应的是( )
A.煤液化制得清洁能源
B.用酒精测试仪检测酒驾
C.将氯气通入冷的消石灰中制漂白粉
D.从海水中提取氯化镁
解析:选D A项,煤的液化是指将煤与H2在催化剂作用下转化为液体燃料(直接)或利用煤产生的H2和CO通过化学合成产生液体燃料或其他液体化工产品(间接)的过程,涉及氧化还原反应,错误;B项,交警常用“酒精检测仪”检查司机是否酒后驾车,其反应原理为C2H5OH+4CrO3+6H2SO4===2Cr2(SO4)3+2CO2↑+9H2O,涉及氧化还原反应,错误;C项,将氯气通入冷的消石灰中制漂白粉的原理:2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O,涉及氧化还原反应,错误;D项,从海水中提取氯化镁时,经历了氯化镁—氢氧化镁—氯化镁的转化过程,不涉及氧化还原反应,正确。
2.下列说法正确的是( )
A.HClO中氯元素化合价比HClO4中氯元素化合价低,所以HClO4的氧化性强
B.已知①Fe + Cu2+===Fe2++Cu;②2Fe3++Cu===2Fe2++Cu2+,则氧化性强弱顺序为Fe3+>Cu2+>Fe2+
C.已知还原性:B->C->D-,反应2C-+ D2===2D-+C2和反应2C-+B2===2B-+C2都能发生
D.具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应
解析:选B HClO的氧化性强,A错误;氧化性Fe3+>Cu2+>Fe2+,B正确;根据反应2C-+B2===2B-+C2可知,还原性C-> B-,与已知矛盾,C错误;如浓硫酸和SO2之间不能反应,D错误。
3.SO2通入足量的Fe(NO3)3稀溶液中,溶液由棕黄色变为浅绿色,但立即又变成棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。针对上述一系列变化,下列说法不正确的是( )
A.上述过程中,最终被还原的是NO
B.从上述反应可以得出结论,氧化性:HNO3>Fe3+>稀硫酸
C.上述过程中,会产生一种无色难溶于水的气体
D.假设通SO2完全反应,同温同压下,SO2和逸出气体的体积比为1∶1
解析:选D 溶液由黄色变为浅绿色,但立即又变为黄色,Fe3+变为Fe2+,后又被氧化为Fe3+,所以最终被还原的是NO,A正确;根据溶液由棕黄色变为浅绿色,说明Fe3+的氧化性强于稀硫酸,但在硝酸存在的条件下溶液立即又变成棕黄色,说明Fe2+迅速被氧化成Fe3+,故硝酸的氧化性比Fe3+强,综上所述氧化性:HNO3>Fe3+>稀硫酸,B正确;SO2被氧化后产生的H+和NO构成强氧化体系,氧化Fe2+时生成无色难溶于水的NO气体,C正确;由A知最终被还原的是NO,故相当于SO2与NO之间的氧化还原反应,有3SO2~2NO,则通入SO2与逸出气体的体积比为3∶2,故D错误。
4.高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。湿法制备的离子反应方程式:2Fe(OH)3+3ClO-+4OH-===2FeO+3Cl-+5H2O;干法制备的化学反应方程式:2FeSO4+4Na2O2===2Na2FeO4+2Na2SO4。有关分析错误的是( )
A.等物质的量时,Na2FeO4氧化能力优于NaClO
B.湿法中氢氧化铁被氧化
C.干法中每生成1 mol Na2FeO4转移3 mol电子
D.次氯酸钠的氧化性强于高铁酸钠
解析:选C A项,1 mol Na2FeO4作氧化剂得3 mol电子,而1 mol NaClO作氧化剂得2 mol电子,所以等物质的量时,氧化能力Na2FeO4>NaClO;C项,干法中每生成1 mol Na2FeO4,应转移4 mol电子;D项,湿法制备中可以看出氧化性NaClO>Na2FeO4。
5.石英与焦炭在高温的氮气流中,通过以下反应可制得新型陶瓷材料氮化硅(Si3N4):3SiO2+6C+2N2Si3N4+6CO。下列叙述正确的是( )
A.Si3N4中Si元素显-4价,N元素显+3价
B.上述反应中每生成1 mol Si3N4,N2得到12 mol电子
C.在氮化硅的合成反应中,N2是氧化剂,SiO2是还原剂
D.由上述反应可知还原性:SiO2>Si3N4
解析:选B Si3N4中N为-3价,Si为+4价,A项错误;该反应中N2是氧化剂,C是还原剂,C项错误;该反应中SiO2既不是氧化剂也不是还原剂,无法比较与Si3N4的还原性谁大谁小,D项错误。
6.已知二氯化二硫(S2Cl2)的结构式为Cl—S—S—Cl,它易与水反应:2S2Cl2+2H2O===4HCl+SO2↑+3S↓。对该反应的说法正确的是( )
A.S2Cl2既作氧化剂又作还原剂
B.H2O作还原剂
C.每生成1 mol SO2转移4 mol电子
D.氧化产物与还原产物的物质的量之比为3∶1
解析:选A 因Cl的非金属性比S强,故S2Cl2中S、Cl的化合价分别为+1、-1价,则在反应中只有硫的化合价发生变化,氧化产物与还原产物的物质的量之比为1∶3,A项正确,B、D项错误;SO2中硫的化合价为+4价,故每生成1 mol SO2转移3 mol电子,C项错误。
7.根据表中信息判断,下列选项不正确的是( )
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4…… |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO…… | Cl2、Mn2+…… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱的顺序为MnO>Cl2>Fe3+>Br2
解析:选D A项,酸性高锰酸钾溶液具有强氧化性,过氧化氢在反应中表现还原性,H2O2被氧化成O2,反应过程中氢原子和氧原子构成水分子,正确;B项,根据产物,氯气先氧化Fe2+,还原性Fe2+>Br-,发生的反应是6FeBr2+3Cl2===2FeCl3+4FeBr3,正确;C项,生成1 mol Cl2,转移电子的物质的量为[0-(-1)]×2×1 mol=2 mol,正确;D项,根据反应中氧化剂的氧化性强于氧化产物的氧化性,②中氧化性Cl2>Br2>Fe3+,③中氧化性MnO>Cl2,氧化性由强到弱的顺序是MnO>Cl2>Br2>Fe3+,错误。
8.已知下列实验事实:①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;②向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液;③将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是( )
A.化合物KCrO2中Cr元素为+3价
B.实验①证明Cr2O3是两性氧化物
C.实验②证明H2O2既有氧化性又有还原性
D.实验③证明氧化性:Cr2O>I2
解析:选C KCrO2和Cr2(SO4)3中Cr元素均为+3价,A项正确;由①知Cr2O3既能溶于强酸,又能溶于强碱,且均生成盐和水,故Cr2O3为两性氧化物,B项正确;由②可知H2O2将KCrO2氧化为K2Cr2O7,说明H2O2具有氧化性,C项错误;由③中溶液变蓝知,生成了碘单质,则反应中Cr2O是氧化剂,I2是氧化产物,由氧化剂的氧化性大于氧化产物的氧化性知,氧化性:Cr2O>I2,D项正确。
9.已知NH4CuSO3与足量的10 mol·L-1硫酸溶液混合微热,产生下列现象:①有红色金属生成;②产生刺激性气味的气体;③溶液呈现蓝色;据此判断下列说法正确的是( )
A.反应中硫酸作氧化剂
B.NH4CuSO3中硫元素被氧化
C.刺激性气味的气体是氨气
D.1 mol NH4CuSO3完全反应转移0.5 mol电子
解析:选D NH4CuSO3与足量的10 mol·L-1H2SO4混合微热,生成Cu、CuSO4、SO2、(NH4)2SO4,可知NH4CuSO3中Cu元素的化合价一部分由+1价升高为 +2价,一部分由 +1价降低为0价,故NH4CuSO3既作氧化剂又作还原剂。A项,H2SO4中各元素的化合价不变,错误;B项,NH4CuSO3中只有Cu元素的化合价发生变化,错误;C项,刺激性气味的气体为SO2,错误;D项,1 mol NH4CuSO3完全反应转移电子为0.5 mol×(1-0)=0.5 mol,正确。
10.把图2中的物质补充到图1中,可得到一个完整的氧化还原型离子方程式(未配平):
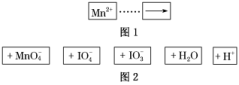
对于该离子方程式的说法不正确的是( )
A.IO作氧化剂
B.氧化性:Mn2+>IO
C.氧化剂与还原剂的物质的量之比为5∶2
D.若有2 mol Mn2+参加反应时,则转移10 mol电子
解析:选B 由Mn2+―→MnO知,锰元素的化合价升高,Mn2+作还原剂,氧化产物为MnO,由IO―→IO知,碘元素的化合价降低,则IO作氧化剂,IO为还原产物,选项A正确;根据配平后的方程式2Mn2++5IO+3H2O===5IO+2MnO+6H+,可知选项C和D均正确;根据氧化性:氧化剂>氧化产物;还原性:还原剂>还原产物可知选项B错。
11.U常见化合价有+4和+6。硝酸铀酰[UO2(NO3)2]加热可发生如下分解:
[UO2(NO3)2]―→UxOy+NO2↑+O2↑(未配平)
将气体产物收集于试管中并倒扣于盛水的水槽中,气体全部被吸收,水充满试管。则生成的铀的氧化物化学式是( )
A.UO2 B.2UO2·UO3
C.UO3 D.UO2·2UO3
解析:选C 由题意知气体产物全部被吸收,即二者与水完全反应生成HNO3,依据化合价升降守恒,判断出4NO2+O2+2H2O===4HNO3,则说明硝酸铀酰在分解前后铀元素的化合价未发生变化,故需保持+6价。
12.某含铬(Cr2O)废水用硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]处理,反应中铁元素和铬元素(+3价)完全转化为沉淀。该沉淀干燥后得到n mol FeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是( )
A.消耗硫酸亚铁铵的物质的量为n(2-x)mol
B.处理废水中Cr2O的物质的量为 mol
C.反应中发生转移的电子的物质的量为3nx mol
D.在FeO·FeyCrxO3中3x=y
解析:选A 根据铁原子守恒可知,消耗硫酸亚铁铵的物质的量为n(1+y)mol,又由FeO·FeyCrxO3呈电中性可知3x+3y=6,代入前式得,消耗硫酸亚铁铵的物质的量为n(3-x)mol,故A错误;根据Cr原子守恒,产物中Cr原子为xn mol,故Cr2O的物质的量为 mol,故B正确;生成n mol FeO·FeyCrxO3,则一共有nx mol Cr原子参加反应,1 mol Cr原子转移3 mol电子,故转移的电子数为3nx mol,故C正确;该反应中铁元素的化合价部分由+2价升高到+3价,铬元素的化合价由+6价降低为+3价,根据得失电子守恒有3x=y,故D正确。
13.某小组同学为探究H2O2、H2SO3、Br2的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
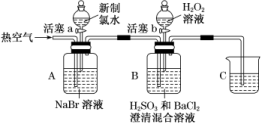
实验记录如下:
| 实验操作 | 实验现象 |
Ⅰ | 打开活塞a,滴加少量新制氯水,关闭活塞a | A中溶液变为浅红棕色 |
Ⅱ | 吹入热空气 | A中红棕色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | B中开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
请回答下列问题:
(1)实验操作Ⅰ时,A中反应的离子方程式为___________________________________________________________________。
(2)实验操作Ⅱ吹入热空气的目的是___________________________________________。
(3)装置C的作用是________________________________________________;
C中盛放的药品是______________________。
(4)实验操作Ⅲ中混合液逐渐变成红棕色,其对应的离子方程式为________________________________________________________________________。
(5)由上述实验得出的结论是______________________________________________。
(6)①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否有干扰,理由是_____________________________________________________________________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是____________________________________________________(写出一条即可)。
解析:(1)实验操作Ⅰ是Cl2置换出NaBr中的Br2,发生的反应为Cl2+2Br-===2Cl-+Br2。(2)溴易挥发,利用热空气吹出溴蒸气。(3)溴有毒,易造成空气污染,不能直接排到空气中,应利用强碱溶液进行尾气吸收。(4)操作Ⅱ中,产生大量白色沉淀,且溶液颜色没有明显变化,说明Br2将H2SO3氧化为H2SO4(产生BaSO4沉淀),自身被还原为Br-。加入H2O2,混合溶液变成红棕色,说明有Br2生成,即H2O2将Br-氧化成Br2,注意溶液呈酸性。(5)H2O2将Br-氧化成Br2,Br2将H2SO3氧化成H2SO4,故氧化性:H2O2>Br2>H2SO3。(6)①热空气会氧化H2SO3,但可以通过颜色变化来判断Br2被H2SO3还原。②开始时颜色无明显变化,可能是因为H2SO3过量、H2O2浓度小、H2O2与Br-反应慢等。
答案:(1)2Br-+Cl2===Br2+2Cl-
(2)吹出单质Br2
(3)吸收多余的Br2,以免污染环境 NaOH溶液
(4)H2O2+2Br-+2H+===Br2+2H2O
(5)氧化性:H2O2>Br2>H2SO3
(6)①不干扰,无论热空气是否参加氧化H2SO3,只要观察到B中产生白色沉淀的同时颜色无明显变化,即能证明Br2氧化了H2SO3 ②H2SO3有剩余(或H2O2浓度小或Br-与H2O2反应慢等合理答案均可)
14.(1)次磷酸钠(NaH2PO2)可用于化学镀镍,即通过化学反应在塑料镀件表面沉积镍磷合金。
化学镀镍的溶液中含有Ni2+和H2PO,在酸性条件下发生以下镀镍反应:
Ni2++__H2PO+______===__Ni+__H2PO+______
①请配平上述化学方程式。
②上述反应中,若生成1 mol H2PO,反应中转移电子的物质的量为________。
(2)①高铁酸盐也是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:
2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑
若生成2 mol Na2FeO4,则反应中电子转移的物质的量为________mol。
②高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含Mn2+1 mg的水体样本,需要1.2 mg·L-1高铁酸钾________ L。
(3)S2O具有强氧化性,其还原产物为SO,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液。请写出此反应的化学方程式:________________________________________________________________________。
(4)①在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:
FeSO4+____KNO3+____H2SO4
K2SO4+____Fe2(SO4)3+____NO↑+____H2O;其中氧化剂为__________。
②铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160 mL 5 mol·L-1盐酸中,再加入一定量铁粉恰好溶解,收集到2.24 L(标准状况)气体,经检测,溶液中无Fe3+,则参加反应的铁粉的质量为__________。
解析:(1)②H2PO中P显+1价,H2PO中P显+3价,所以若生成1 mol H2PO,应转移电子2 mol。
(2)①在该反应中,Fe由+2价升到+6价,Na2O2中的一部分O由-1价升到0价。所以当生成2 mol Na2FeO4时,应转移电子10 mol。
②根据电子守恒得:
×2=×3
x=2 L。
(3)根据信息,Mn2+被氧化成MnO,而S2O被还原生成稳定的SO,则可写出相应的化学方程式。
(4)②Fe2O3+6H+===2Fe3++3H2O
x 6x 2x
2Fe3++Fe===3Fe2+
2x x
Fe + 2H+=== H2↑+Fe2+
0.1 mol 0.2 mol 0.1 mol
由题意得:0.2 mol+6x=0.16 L×5 mol·L-1
解得x=0.1 mol
参加反应的铁粉质量为(0.1 mol+x)×56 g·mol-1=11.2 g。
答案:(1)①1 1H2O 1 1 2H+ ②2 mol
(2)①10 ②2
(3)5K2S2O8+2MnSO4+8H2O4K2SO4+2KMnO4+8H2SO4
(4)①6 2 4 1 3 2 4 KNO3 ②11.2 g
15.硫的多种化合物在工业中有重要的应用。
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为________。
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为1∶2时,产物为________(填化学式)。
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2。该反应的化学方程式为___________________________________________。
(2)铬会造成环境污染。某酸性废水中含有Cr2O,处理时可用焦亚硫酸钠(Na2S2O5)将Cr2O转化为毒性较低的Cr3+,再调节pH至8,使铬元素沉降,分离出污泥后测得废水中Cr3+浓度为0.52 mg·L-1,达到排放标准。
①Na2S2O5参加反应的离子方程式为________________________________________。
②处理后的废水中Cr3+的物质的量浓度为________________________________________________________ mol·L-1。
解析:(1)②根据题中信息可知,氧化剂是O2,还原剂是Na2S2O4,又知氧化剂和还原剂的物质的量之比为1∶2,若设Na2S2O4被氧化后硫的化合价为+x价,则根据得失电子守恒有1×4=(x-3)×2×2,解得x=4,又有水蒸气参与反应,所以产物为NaHSO3。
(2)①2O将Cr2O还原为Cr3+,则S2O被氧化为SO,由电荷守恒可知反应物中还应有H+,据此可写出反应的离子方程式。②处理后的废水中Cr3+的浓度已知是0.52 mg·
L-1,只需将其转化为物质的量浓度即可,即c(Cr 3+)==1×10-5 mol·L-1。
答案:(1)①+3 ②NaHSO3
③HCOOH+2SO2+2NaOH===Na2S2O4+CO2+2H2O
(2)①3S2O+2Cr2O+10H+===6SO+4Cr3++5H2O ②1×10-5
2024届高考化学一轮复习 课时跟踪检测(四) 氧化还原反应(含答案): 这是一份2024届高考化学一轮复习 课时跟踪检测(四) 氧化还原反应(含答案),共12页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
高考化学一轮复习跟踪检测2物质的量 含解析: 这是一份高考化学一轮复习跟踪检测2物质的量 含解析,共6页。试卷主要包含了NA表示阿伏加德罗常数的数值,设NA表示阿伏加德罗常数的值,NA代表阿伏加德罗常数的数值,下列有关溶液配制的说法正确的是等内容,欢迎下载使用。
2022届高考化学一轮复习跟踪检测10追根知反应3__氧化还原反应的配平与计算含解析: 这是一份2022届高考化学一轮复习跟踪检测10追根知反应3__氧化还原反应的配平与计算含解析,共10页。试卷主要包含了硫代硫酸钠溶液与氯气能发生反应等内容,欢迎下载使用。












