


2022年高中化学必修2暑假同步测试卷(七)生活中两种常见的有机物 Word版含答案
展开 www.ks5u.com高中同步测试卷(七)
www.ks5u.com高中同步测试卷(七)
生活中两种常见的有机物
(时间:90分钟,满分:100分)
一、选择题(本题包括16小题,每小题只有一个选项符合题意,共48分)
1.“绿色能源”是目前研究的新能源之一,高粱、玉米等绿色植物的种子经发酵、蒸馏就可以得到一种“绿色能源”。这种物质是( )
A.氢气 B.甲烷
C.酒精 D.木炭
2.下列物质都能与金属钠反应放出H2,产生H2的速率排序正确的是( )
①C2H5OH ②NaOH溶液 ③醋酸溶液
A.①>②>③ B.②>①>③
C.③>②>① D.③>①>②
3.下列有机物中,不属于烃的衍生物的是( )
A.氯丁烷 B.甲苯
C.硝基苯 D.乙醇
4.下列物质不能用于从碘水中提取碘的是( )
A.乙醇 B.苯
C.四氯化碳 D.汽油
5.下列除杂方法不正确的是( )
A.除去乙烷中混有的少量乙烯:通入稀溴水中,干燥
B.除去溴苯中混有的少量单质溴:加入足量的NaOH溶液,振荡、静置、分液
C.除去96%的乙醇中的少量水制无水乙醇:加入生石灰,振荡、静置、蒸馏
D.除去乙醇中混有的少量苯,可通过分液的方法实现
6.若要检验酒精中是否含有少量水,可选用的试剂是( )
A.石灰石 B.金属钠
C.浓硫酸 D.无水硫酸铜
7.向装有乙醇的烧杯中投入一小块金属钠,下列对实验现象的描述中正确的是( )
A.钠块浮在乙醇液面的上面 B.钠熔化成小球
C.钠块在乙醇的液面上游动 D.钠块表面有气泡放出
8.如图所示的某有机反应,其反应类型为( )
![]()
A.取代反应 B.加成反应
C.水解反应 D.氧化反应
9.把质量为m g的Cu丝灼烧变黑,趁热立即放入下列物质中,Cu丝变红且质量小于m g的是( )
A.C2H5OH B.稀H2SO4
C.水 D.CO
10.下列物质中,在一定条件下既能进行加成反应,也能进行取代反应,并且不能使KMnO4酸性溶液褪色的是( )
A.乙烷 B.乙烯
C.乙醇 D.苯
11.CH3COOH分别与CH3CH2OH和CH3 CHOH反应,生成的酯的相对分子质量关系为( )
A.前者大于后者 B.前者小于后者
C.前者等于后者 D.无法判断
12.肉桂醇,白色针状或块状结晶,有温和、持久而舒适的香气,可用作定香剂和除臭剂,其结构简式如图所示,下列有关肉桂醇的叙述正确的是( )
![]()
A.肉桂醇的摩尔质量为134 g
B.肉桂醇能使酸性高锰酸钾溶液褪色
C.肉桂醇能与溴水发生取代反应
D.1 mol肉桂醇完全燃烧消耗11.5 mol O2
13.巴豆酸的结构简式为CH2—CH===CH—COOH。现有①氯化氢、②溴水、③纯碱溶液、④乙醇、⑤酸性高锰酸钾溶液,在一定条件下能与巴豆酸反应的物质是( )
A.②④⑤ B.①③④
C.①②③④ D.①②③④⑤
14.在下图实验装置中,持续通入X气体,可以看到a处有红色物质生成,b处固体变蓝,c处得到具有刺激性气味的液体,则X气体可能是 ( )
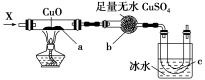
A.H2 B.CO和H2
C.NH3 D.CH3CH2OH(g)
15.下列说法不正确的是( )
A.体积分数为75%的乙醇水溶液,可用于杀菌、消毒
B.1 mol乙醇与足量Na反应生成 mol H2
C.苯中含有少量乙醇,加水后分液可除去乙醇
D.用乙醇作萃取剂可以将溴从溴水中萃取出来
16.某有机物X(C4H6O5)广泛存在于许多水果内。该化合物具有如下性质:
①在有浓H2SO4存在和加热条件下,X与醇或羧酸均反应生成有香味的产物;
②1 mol X与足量的NaHCO3溶液反应,可生成44.8 L(标准状况下)CO2。
根据上述信息,对X的结构判断正确的是( )
A.含有碳碳双键
B.含有两个羧基和一个羟基
C.含有一个羧基和两个羟基
D.含有三个羟基和一个—COOR
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
答案 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
二、非选择题(本题包括4小题,共52分)
17.(12分)已知A是一种相对分子质量为28的气态烃,现以A为主要原料合成一种具有酸味的物质D,其合成路线如图所示。
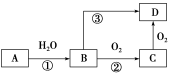
请回答下列问题:
(1)写出A的结构简式:__________________。
(2)A、B分子中的官能团名称分别是__________________、__________________。
(3)物质B可以被直接氧化为D,需要加入的试剂是__________________。
(4)写出下列反应的化学方程式:
①__________________________________________________________;反应类型:__________________。
②__________________________________________________________;反应类型:__________________。
18.(12分)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
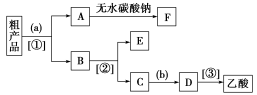
(1)试剂a是________,试剂b是________;分离方法①是________,分离方法②是________,分离方法③是________。
(2)在得到的A中加入无水碳酸钠粉末,目的是
________________________________________________________________________。
19.(12分)为了探究乙醇和金属钠反应的原理,做了如下四个实验:
实验一:向小烧杯中加入无水乙醇,再放入一小块金属钠,观察现象,并收集产生的气体。
实验二:设法检验实验一收集到的气体。
实验三:向试管中加入3 mL水,并加入一小块金属钠,观察现象。
实验四:向试管中加入3 mL乙醚(CH3CH2OCH2CH3),并加入一小块金属钠,发现无任何现象发生。
回答以下问题:
(1)简述实验二中检验气体的实验方法及作出判断的依据:
________________________________________________________________________
________________________________________________________________________。
(2)从结构上分析,该实验选取水和乙醚做参照物的原因是
________________________________________________________________________
________________________________________________________________________。
(3)实验三的目的是欲证明________________________;实验四的目的是欲证明________________________________;根据实验三和实验四的结果,可以证明乙醇和金属钠反应的化学方程式应为
________________________________________________________________________。
20.(16分)下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
[实验目的]制取乙酸乙酯
[实验原理]甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯。
[装置设计]甲、乙、丙三位同学分别设计了下列三套实验装置:
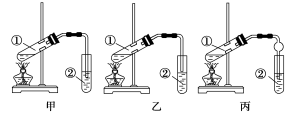
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,较合理的是________(选填“甲”或“乙”)。丙同学将甲装置进行了改进,将其中的玻璃管改成了球形干燥管,除起冷凝作用外,另一重要作用是____________________________。
[实验步骤]
(1)按丙同学选择的装置组装仪器,在试管中先加入3 mL乙醇,并在摇动下缓缓加入2 mL浓硫酸充分摇匀,冷却后再加入2 mL冰醋酸;
(2)将试管固定在铁架台上;
(3)在试管②中加入适量的饱和Na2CO3溶液;
(4)用酒精灯对试管①加热;
(5)当观察到试管②中有明显现象时停止实验。
[问题讨论]
a.步骤(1)安装好实验装置,加入样品前还应检查____________;
b.写出试管①发生反应的化学方程式(注明反应条件):
________________________________________________________________________;
c.试管②中饱和Na2CO3溶液的作用是____________________________________。______________(填“能”或“不能”)换成NaOH溶液,原因为
________________________________________________________________________。
d.从试管②中分离出乙酸乙酯的实验操作是____________________。
参考答案与解析
1. C
2. 解析:选C。Na与CH3COOH反应比与C2H5OH反应剧烈,故反应速率③>①,可排除A、B项;NaOH溶液中含有H2O,故Na与NaOH溶液反应比与C2H5OH反应快,比与CH3COOH反应慢。
3. 解析:选B。B项,甲苯为烃而不是烃的衍生物。
4. 解析:选A。作为萃取剂的条件之一就是和原来的溶液互不相溶,能分层,而乙醇和水互溶,故它不能用于从碘水中提取碘。
5. 解析:选D。乙醇和苯互溶,可通过蒸馏的方法除去乙醇中的少量苯。
6.解析:选D。无水硫酸铜遇水生成CuSO4·5H2O,由白色粉末变成蓝色晶体,符合题意;B项,钠不但能与水反应,也能与乙醇反应,故不能检验酒精中是否含有水的存在。
7. 解析:选D。因钠的密度大于乙醇,故钠能沉到烧杯的底部,且在钠的表面能看到有气泡放出。
8. 解析:选A。根据图示可知,此反应为乙酸和乙醇反应生成乙酸乙酯和水的反应,属于酯化反应,而由于反应的机理可以看做是乙醇中的—OCH2CH3取代乙酸中的—OH,故又属于取代反应,故选A。
9.解析:选B。铜丝灼烧变黑生成CuO,在加热条件下,CuO被C2H5OH、CO还原生成Cu,质量与灼烧前相同,CuO与水不反应,也不会再变红,CuO与稀H2SO4反应后剩余未反应的铜使Cu丝变红且质量减小。
10.解析:选D。A项,乙烷不能发生加成反应;B项,乙烯能使KMnO4酸性溶液褪色;C项,乙醇不能发生加成反应。
11.解析:选B。CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O,CH3COOH+CH3CHOHCH3CO18OCH2CH3+H2O,生成酯的相对分子质量分别为88和90。
12. 解析:选B。肉桂醇的分子式为C9H10O,其摩尔质量为134 g·mol-1,A选项错误;肉桂醇中含有碳碳双键,可使酸性高锰酸钾溶液褪色,B选项正确;肉桂醇分子中含有碳碳双键,碳碳双键可与溴水发生加成反应,C选项错误;根据肉桂醇的分子式可知1 mol肉桂醇完全燃烧消耗的O2为11 mol,D选项错误。
13. 解析:选D。①氯化氢能与巴豆酸发生加成反应,②溴水能与巴豆酸发生加成反应,③纯碱溶液能与巴豆酸反应生成盐、CO2和水,④乙醇能与巴豆酸发生酯化反应,⑤酸性高锰酸钾溶液能与巴豆酸发生氧化反应。
14. 解析:选D。选项中的物质都能与氧化铜反应,生成物中含有铜和水,因此a处有红色物质生成,b处固体变蓝。但由于干燥管中有足量的无水硫酸铜,能将生成的水全部吸收,所以c处得到的液体不是水。选项D中,CH3CH2OH(g)与CuO反应:CH3CH2OH+CuOCH3CHO+Cu+H2O,a处有红色物质生成,b处固体变蓝,c处得到具有刺激性气味的液体,D正确。
15.解析:选D。乙醇和水互溶,不能将溴从溴水中萃取出来。
16. 解析:选B。由①可知该有机物结构中必存在—OH和—COOH,由②可知该有机物结构中必存在两个—COOH,再结合X的分子式为C4H6O5可知,其结构中只能含有两个—COOH和一个—OH。
17. 解析:由烃的相对分子质量为28可推知该烃为乙烯,即CH2===CH2。乙烯与水加成制取乙醇,乙醇氧化制取乙醛,同时乙醇能直接氧化生成乙酸。
答案:(1)CH2===CH2
(2)碳碳双键 羟基
(3)酸性KMnO4溶液(或酸性K2Cr2O7溶液)
(4)①CH2===CH2+H2OCH3CH2OH 加成反应 ②2CH3CH2OH+O22CH3CHO+2H2O 氧化反应
18.解析:粗产品中有乙酸乙酯、乙酸、乙醇三种物质,用饱和碳酸钠溶液进行萃取、分液可把混合物分离成两种半成品,其中一份是乙酸乙酯(即A)、另一份是乙酸钠和乙醇的水溶液(即B)。蒸馏B可得到乙醇(即E),留下的残液是乙酸钠溶液(即C)。再在C中加稀H2SO4,经蒸馏可得到乙酸溶液。
答案:(1)饱和Na2CO3溶液 稀硫酸 分液 蒸馏 蒸馏
(2)除去乙酸乙酯中的水分
19. 解析:乙醇与钠反应产生的气体有两种可能:H2或O2,若检验该气体可收集后靠近明火,若能燃烧或发出爆鸣声,则该气体是氢气,否则是氧气。根据乙醇的结构分析知,选取水和CH3CH2OCH2CH3做参照物的原因是它们分别含有—OH和CH3CH2—;然后再证明羟基上的氢和钠能反应,乙基上的氢与Na不能反应。
答案:(1)将收集到的气体点燃,若能燃烧或发出爆鸣声则证明该气体是氢气
(2)乙醇分子中含有乙基和羟基,而水分子中含羟基,乙醚分子中含有乙基
(3)羟基氢可和钠发生反应 乙基上的氢不能和钠发生反应 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑
20.解析:根据甲、乙装置的差别及丙的改进装置便知应选择乙装置,这样可防止倒吸,这也是改进后干燥管的作用之一。由于乙醇与乙酸均易挥发,因此制取的乙酸乙酯中会混有这两种物质,可用饱和Na2CO3溶液除去乙醇和乙酸,同时还降低了乙酸乙酯的溶解度,并可用分液的方法分离,但若用NaOH溶液,则NaOH会使乙酸乙酯水解,故不能用NaOH溶液。
答案:[装置设计]乙 能防止倒吸
[问题讨论]a.装置的气密性
b.CH3COOH+C2H5OHCH3COOC2H5+H2O
c.吸收乙醇、除去乙酸、降低乙酸乙酯的溶解度,使其分层析出 不能 若用NaOH溶液,则NaOH会使生成的乙酸乙酯水解,导致实验失败
d.分液
2022年高中化学必修2暑假同步测试卷(十五)综合检测卷C Word版含答案: 这是一份2022年高中化学必修2暑假同步测试卷(十五)综合检测卷C Word版含答案,共8页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
2022年高中化学必修2暑假同步测试卷(十四)综合检测卷B Word版含答案: 这是一份2022年高中化学必修2暑假同步测试卷(十四)综合检测卷B Word版含答案,共8页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
2022年高中化学必修2暑假同步测试卷(十三)综合检测卷A Word版含答案: 这是一份2022年高中化学必修2暑假同步测试卷(十三)综合检测卷A Word版含答案,共8页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。












