

十年(23-22)高考化学真题分项汇编专题29 反应热计算 盖斯定律(2份打包,原卷版+教师版)
展开专题29 反应热计算——盖斯定律
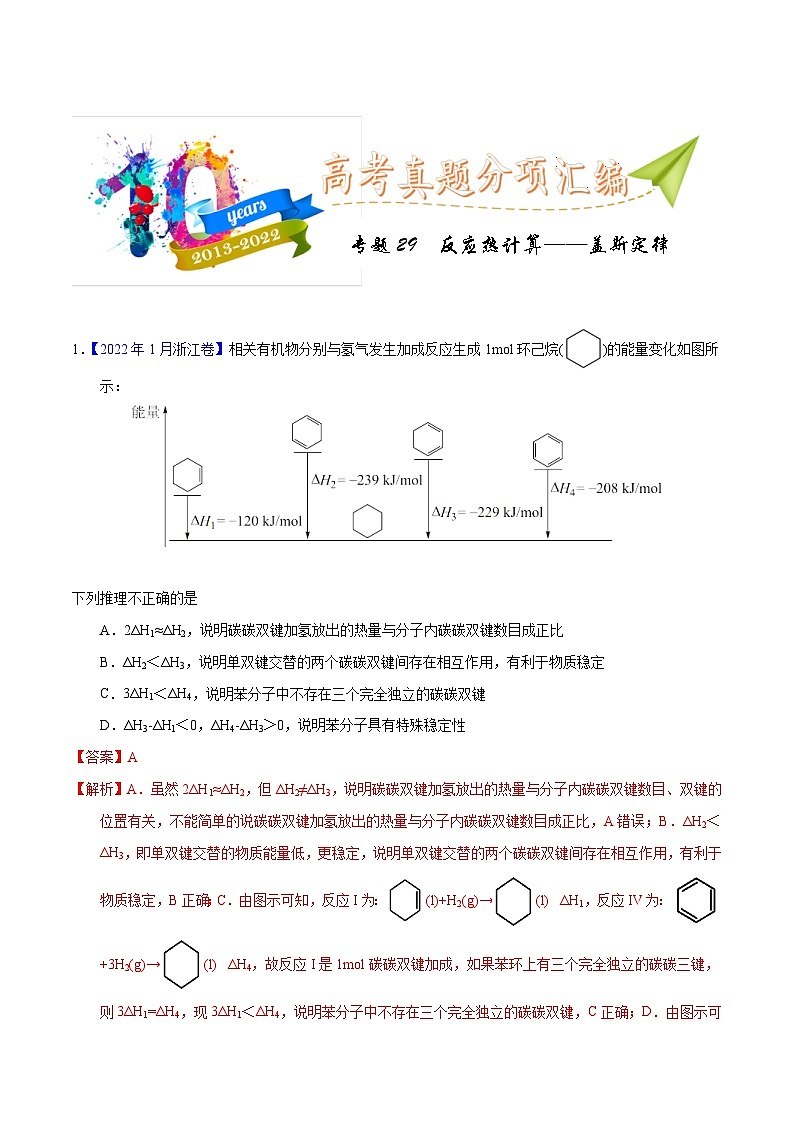
1.【2022年1月浙江卷】相关有机物分别与氢气发生加成反应生成1mol环己烷()的能量变化如图所示:
下列推理不正确的是
A.2ΔH1≈ΔH2,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
B.ΔH2<ΔH3,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
C.3ΔH1<ΔH4,说明苯分子中不存在三个完全独立的碳碳双键
D.ΔH3-ΔH1<0,ΔH4-ΔH3>0,说明苯分子具有特殊稳定性
【答案】A
【解析】A.虽然2ΔH1≈ΔH2,但ΔH2≠ΔH3,说明碳碳双键加氢放出的热量与分子内碳碳双键数目、双键的位置有关,不能简单的说碳碳双键加氢放出的热量与分子内碳碳双键数目成正比,A错误;B.ΔH2<ΔH3,即单双键交替的物质能量低,更稳定,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定,B正确;C.由图示可知,反应I为:(l)+H2(g)→(l) ΔH1,反应IV为:+3H2(g)→(l) ΔH4,故反应I是1mol碳碳双键加成,如果苯环上有三个完全独立的碳碳三键,则3ΔH1=ΔH4,现3ΔH1<ΔH4,说明苯分子中不存在三个完全独立的碳碳双键,C正确;D.由图示可知,反应I为:(l)+H2(g)→(l) ΔH1,反应III为:(l)+2H2(g) →(l) ΔH3,反应IV为:+3H2(g)→(l) ΔH4,ΔH3-ΔH1<0即(l)+H2(g) →(l) ΔH<0,ΔH4-ΔH3>0即+H2(g)→(l) ΔH>0,则说明具有的总能量小于,能量越低越稳定,则说明苯分子具有特殊稳定性,D正确;故答案为:A。
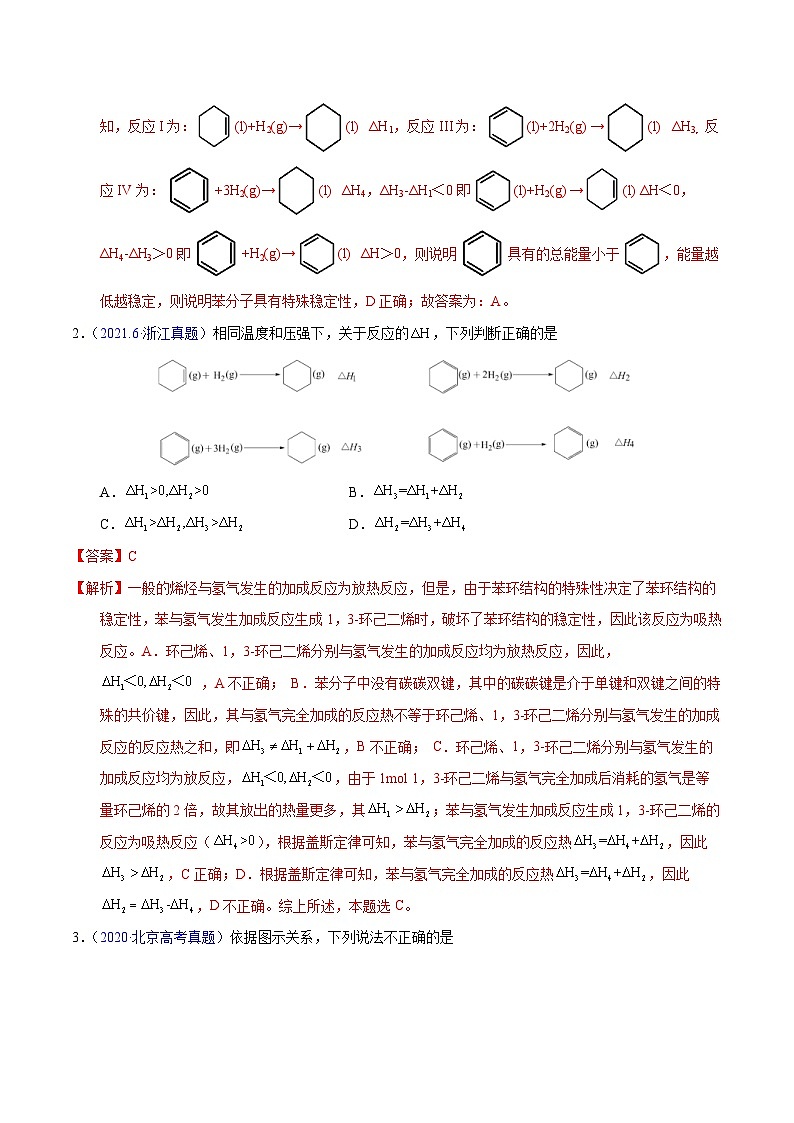
2.(2021.6·浙江真题)相同温度和压强下,关于反应的,下列判断正确的是
A. B.
C. D.
【答案】C
【解析】一般的烯烃与氢气发生的加成反应为放热反应,但是,由于苯环结构的特殊性决定了苯环结构的稳定性,苯与氢气发生加成反应生成1,3-环己二烯时,破坏了苯环结构的稳定性,因此该反应为吸热反应。A.环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放热反应,因此, ,A不正确; B.苯分子中没有碳碳双键,其中的碳碳键是介于单键和双键之间的特殊的共价键,因此,其与氢气完全加成的反应热不等于环己烯、1,3-环己二烯分别与氢气发生的加成反应的反应热之和,即,B不正确; C.环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放反应,,由于1mol 1,3-环己二烯与氢气完全加成后消耗的氢气是等量环己烯的2倍,故其放出的热量更多,其;苯与氢气发生加成反应生成1,3-环己二烯的反应为吸热反应(),根据盖斯定律可知,苯与氢气完全加成的反应热,因此,C正确;D.根据盖斯定律可知,苯与氢气完全加成的反应热,因此,D不正确。综上所述,本题选C。
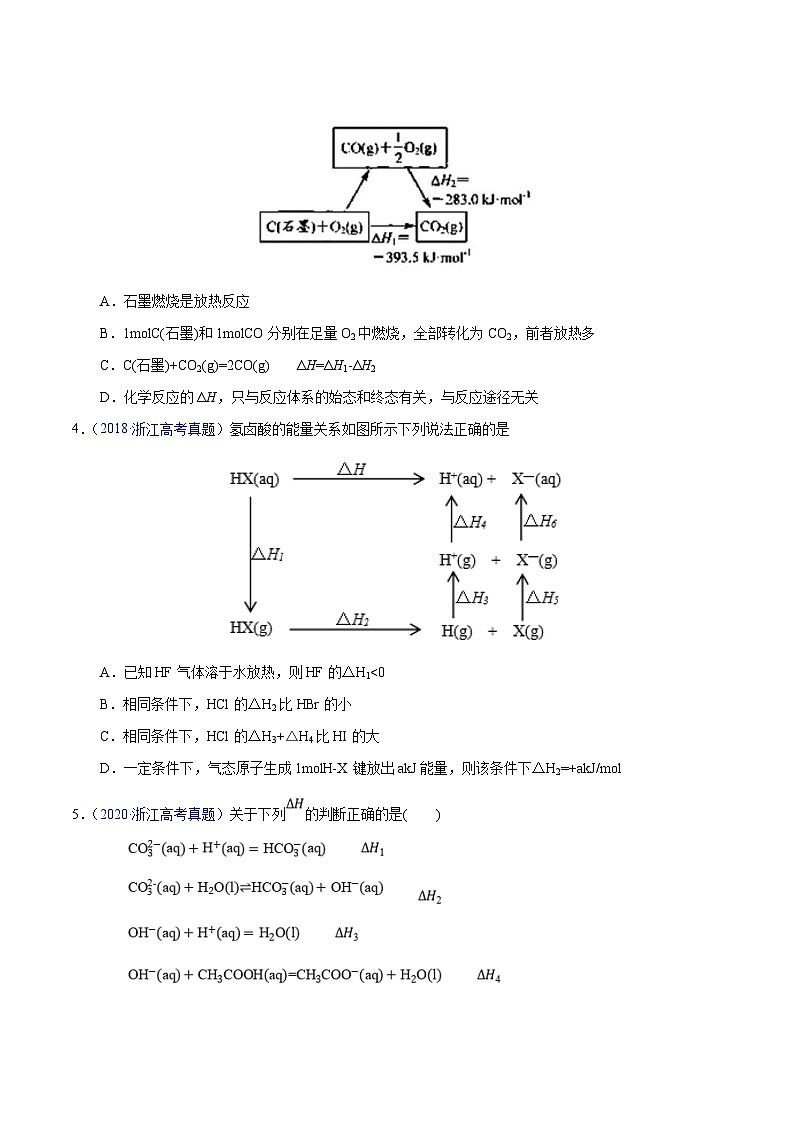
3.(2020·北京高考真题)依据图示关系,下列说法不正确的是
A.石墨燃烧是放热反应
B.1molC(石墨)和1molCO分别在足量O2中燃烧,全部转化为CO2,前者放热多
C.C(石墨)+CO2(g)=2CO(g) ΔH=ΔH1-ΔH2
D.化学反应的ΔH,只与反应体系的始态和终态有关,与反应途径无关
【答案】C
【解析】A.所有的燃烧都是放热反应,根据图示,C(石墨)+O2(g)= CO2(g) ΔH1=-393.5kJ/mol,ΔH1<0,则石墨燃烧是放热反应,正确;B.根据图示,C(石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol,CO(g)+O2(g)=CO2(g) ΔH2=-283.0kJ/mol,根据反应可知都是放热反应,1molC(石墨)和1molCO分别在足量O2中燃烧,全部转化为CO2,1molC(石墨)放热多,正确;C.根据分析,①C(石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol,②CO(g)+O2(g)=CO2(g) ΔH2=-283.0kJ/mol,根据盖斯定律①-②x2可得:C(石墨)+CO2(g)=2CO(g) ΔH=ΔH1-2ΔH2,错误;D.根据盖斯定律可知,化学反应的焓变只与反应体系的始态和终态有关,与反应途径无关,正确;答案选C。
4.(2018·浙江高考真题)氢卤酸的能量关系如图所示下列说法正确的是
A.已知HF气体溶于水放热,则HF的△H1<0
B.相同条件下,HCl的△H2比HBr的小
C.相同条件下,HCl的△H3+△H4比HI的大
D.一定条件下,气态原子生成1molH-X键放出akJ能量,则该条件下△H2=+akJ/mol
【答案】D
【解析】A.△H1代表的是HX气体从溶液中逸出的过程,因为HF气体溶于水放热,则HF气体溶于水的逆过程吸热,即HF的△H1>0,错误;B.由于HCl比HBr稳定,所以相同条件下HCl的△H2比HBr的大,错误;C.△H3+△H4代表H(g)→H(aq)的焓变,与是HCl的还是HI的无关,错误;D.一定条件下,气态原子生成1molH-X键放出akJ能量,则断开1molH-X键形成气态原子吸收akJ的能量,即为△H2=+akJ/mol,正确;答案选D。
5.(2020·浙江高考真题)关于下列的判断正确的是( )
A. B. C. D.
【答案】B
【解析】碳酸氢根的电离属于吸热过程,则CO(aq)+H+(aq)=HCO(aq)为放热反应,所以△H1<0;
CO(aq)+H2O(l)HCO(aq)+OHˉ(aq)为碳酸根的水解离子方程式,CO的水解反应为吸热反应,所以△H2>0;
OHˉ(aq)+H+(aq)=H2O(l)表示强酸和强碱的中和反应,为放热反应,所以△H3<0;
醋酸与强碱的中和反应为放热反应,所以△H4<0;
但由于醋酸是弱酸,电离过程中会吸收部分热量,所以醋酸与强碱反应过程放出的热量小于强酸和强碱反应放出的热量,则△H4>△H3;
综上所述,只有△H1<△H2正确,故答案为B。
6.(2015·重庆高考真题)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol-1
已知碳的燃烧热ΔH1=a kJ·mol-1
S(s)+2K(s)=K2S(s) ΔH2=b kJ·mol-1
2K(s)+N2(g)+3O2(g)=2KNO3(s) ΔH3=c kJ·mol-1
则x为
A.3a+b-c B.c+3a-b C.a+b-c D.c+a-b
【答案】A
【解析】已知碳的燃烧热为ΔH1=a kJ·mol-1,则碳燃烧的热化学方程式为:①C(s)+O2(g)=CO2(g) ΔH1=a kJ·mol-1,②S(s)+2K(s)=K2S(s) ΔH2=b kJ·mol-1,③2K(s)+N2(g)+3O2(g)=2KNO3(s) ΔH3=c kJ·mol-1,根据盖斯定律,可得ΔH=3ΔH1+ΔH2—ΔH3,即x=3a+b-c,答案选A。
7.(2017·浙江高考真题)根据体系的能量循环图:
下列说法正确的是:
A.>0 B.
C. D.
【答案】D
【解析】A.气态水转化为液态水放出热量,则△H5<0,错误;B.氢氧化钙生成氧化钙固体和水蒸气,与液态水和氧化钙反应生成氢氧化钙不是可逆的过程,水蒸气变成液态水会放出热量,△H1+△H2≠0,错误;C.②CaO(s)+H2O(l)=Ca(OH)2(s)、④CaO(s)=CaO(s),②+④不能得到510℃时Ca(OH)2(s),则△H3≠△H4+△H2,错误;D.由盖斯定律可知,①+②+④+⑤=-③,即△H1+△H2+△H4+△H5=-△H3,可知△H1+△H2+△H3+△H4+△H5=0,正确;故选:D。
8.(2014·江苏高考真题)已知:C(s)+O2(g)=CO2(g) △H1
CO2(g)+C(s)=2CO(g) △H2
2CO(g)+O2(g)=2CO2(g) △H3
4Fe(s)+3O3(g)=2Fe2O3(s) △H4
3 CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s) △H5
下列关于上述反应焓变的判断正确的是
A.△H1>0,△H3<0
B.△H2>0,△H4>0
C.△H1=△H2+△H3
D.△H3=△H4+△H5
【答案】C
【解析】A、碳和CO燃烧均是放热反应,△H1<0,错误;B、二氧化碳与碳反应是吸热反应,铁在氧气中燃烧是放热反应,△H4<0,错误;C、②CO2(g)+C(s)=2CO(g) △H2,③2CO(g)+O2(g)=2CO2(g) △H3,则根据盖斯定律可知②+③即得到C(s)+O2(g)=CO2(g) ,△H1=△H2+△H3,正确;D、已知④4Fe(s)+3O3(g)=2Fe2O3(s) △H4,⑤3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s) △H5,则根据盖斯定律可知(④+⑤×2)÷3得到2CO(g)+O2(g)=2CO2(g),则△H3=,错误;答案选C。
9.(2008·宁夏高考真题)已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A.-44.2kJ·mol-1 B.+44.2kJ·mlo-1
C.-330kJ·mol-1 D.+330kJ·mlo-1
【答案】A
【解析】由题干条件可知如下反应:
H2(g)+O2(g) H2O(l);ΔH=-285.8 kJ·mol-1 ①
C2H4(g)+3O2(g)2CO2(g)+2H2O(l);ΔH=-1 411.0 kJ·mol-1 ②
C2H5OH(l)+3O2(g)2CO2(g)+3H2O(l);ΔH=-1 366.8 kJ·mol-1 ③
根据盖斯定律则②-③可得:C2H4(g)+H2O(l)C2H5OH(l);ΔH=-44.2 kJ·mol-1。
答案选A。
10.(2013·全国高考真题)在1200℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+O2(g)=SO2(g)+H2O(g) △H1
②2H2S(g)+SO2(g)=S2(g)+2H2O(g) △H2
③H2S(g)+O2(g)=S(g)+H2O(g) △H3
④2S(g) =S2(g) △H4
则△H4的正确表达式为( )
A.△H4=2/3(△H1+△H2-3△H3)
B.△H4=2/3(3△H3-△H1-△H2)
C.△H4=3/2(△H1+△H2-3△H3)
D.△H4=3/2(△H1-△H2-3△H3)
【答案】A
【解析】根据盖斯定律,①×-③×得⑤:S(g)+O2(g)=SO2(g) △H5=(△H1-△H3);根据盖斯定律,②×-③×得⑥:SO2(g)+S(g)=O2(g) + S2(g) △H6=(△H2-2△H3);⑤+⑥得:2S(g) =S2(g) △H4=(△H1+△H2-3△H3),答案为A。
11.(2014·全国高考真题)室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为△H1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为△H2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是
A.△H2>△H3 B.△H1<△H3
C.△H1+△H3=△H2 D.△H1+△H2>△H3
【答案】B
【解析】根据题意知,CuSO4·5H2O(s)溶于水的热化学方程式为CuSO4·5H2O(s)Cu2+(aq)+SO42—(aq)+5H2O(l),△H1>0;CuSO4(s)溶于水的热化学方程式为CuSO4(s)Cu2+(aq)+SO42—(aq),△H2<0;根据盖斯定律知,CuSO4·5H2O受热分解的热化学方程式为:CuSO4·5H2O(s)CuSO4(s)+5H2O(l) △H3=△H1—△H2>0。A、根据上述分析知,△H2<△H3,A错误;B、根据上述分析知,△H1<△H3,B正确;C、根据上述分析知,△H3=△H1—△H2,C错误;D、根据上述分析知,△H1+△H2<△H3,D错误。答案选B。
12.(2013·海南高考真题)已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l);ΔH1
2 H2(g)+ O2(g)= 2H2O(g);ΔH2
C(s)+ O2(g)=CO2(g);ΔH3
则反应4C3H5(ONO2)3(l)= 12CO2(g)+10H2O(g) + O2(g) +6N2(g)的ΔH为
A.12ΔH3+5ΔH2-2ΔH1 B.2ΔH1-5ΔH2-12ΔH3
C.12ΔH3-5ΔH2-2ΔH1 D.ΔH1-5ΔH2-12ΔH3
【答案】A
【解析】已知:①6C(s)+5H2(g)+3N2(g)+9O2(g)═2C3H5(ONO2)3(l);△H1,
②H2(g)+O2(g)=H2O(g);△H2,③C(s)+O2(g)═CO2(g);△H3,
由盖斯定律:10×②+12×③-2×①得:
4C3H5(ONO2)3(l)═12CO2(g)+10H2O(g)+O2(g)+6N2(g);△H=12△H3+10△H2-2△H1;
故选A。
13.(2018·浙江高考真题)已知:
下列说法正确的是
A.∆H1<0,∆H2<0,∆H3<∆H4 B.6∆H1+∆H2+∆H3-∆H4=0
C.-6∆H1+∆H2+∆H3-∆H4=0 D.-6∆H1+∆H2-∆H3+∆H4=0
【答案】B
【解析】物质由气态转化为液态(液化)需要放热,物质由固态转化为气态需要吸热,比较反应3和反应4中 C6H12O6(s)→ C6H12O6(g)为吸热过程,6H2O(g)→ 6 H2O(l)为放热过程,所以反应4放出更多能量,△H更小,故△H3>△H4,选项A错误;由盖斯定律知,反应1的6倍与反应2与反应3的和可以得到反应4,即6△H1+△H2+△H3=△H4,经数学变形,可以得到6△H1+△H2+△H3-△H4=0,选项B正确;选项C、D均错误。答案选B。
14.(2019·浙江高考真题)MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg):
M2+(g)+CO32-(g) M2+(g)+O2−(g)+CO2(g)
已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是
A.ΔH1(MgCO3)>ΔH1(CaCO3)>0
B.ΔH2(MgCO3)=ΔH2(CaCO3)>0
C.ΔH1(CaCO3)-ΔH1(MgCO3)=ΔH3(CaO)-ΔH3(MgO)
D.对于MgCO3和CaCO3,ΔH1+ΔH2>ΔH3
【答案】C
【解析】根据盖斯定律,得ΔH=ΔH1+ΔH2+ΔH3,又易知Ca2+半径大于Mg2+半径,所以CaCO3的离子键强度弱于MgCO3,CaO的离子键强度弱于MgO。A.ΔH1表示断裂CO32-和M2+的离子键所吸收的能量,离子键强度越大,吸收的能量越大,因而ΔH1(MgCO3)>ΔH1(CaCO3)>0,正确;B.ΔH2表示断裂CO32-中共价键形成O2−和CO2吸收的能量,与M2+无关,因而ΔH2(MgCO3)=ΔH2(CaCO3)>0,正确;C.由上可知ΔH1(CaCO3)-ΔH1(MgCO3)<0,而ΔH3表示形成MO离子键所放出的能量,ΔH3为负值,CaO的离子键强度弱于MgO,因而ΔH3(CaO)>ΔH3(MgO),ΔH3(CaO)-ΔH3(MgO)>0,错误;D.由上分析可知ΔH1+ΔH2>0,ΔH3<0,故ΔH1+ΔH2>ΔH3,正确。故答案选C。
15.【2022年全国乙卷】油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
③
计算热分解反应④的________。
【答案】(1)170
【解析】
(1)已知:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1=-1036kJ/mol
②4H2S(g)+2SO2(g)=3S2(g)+4H2O(g) ΔH2=94kJ/mol
③2H2(g)+O2(g)=2H2O(g) ΔH3=-484kJ/mol
根据盖斯定律(①+②)×-③即得到2H2S(g)=S2(g)+2H2(g)的ΔH4=(-1036+94)kJ/mol×+484kJ/mol=170 kJ/mol;
16.【2022年湖北卷】自发热材料在生活中的应用日益广泛。某实验小组为探究“”体系的发热原理,在隔热装置中进行了下表中的五组实验,测得相应实验体系的温度升高值()随时间(t)的变化曲线,如图所示。
回答下列问题:
(1)已知:
①
②
③
则的___________。
【答案】(1)-911.9
【解析】
(1)根据盖斯定律可得,①+②+2´③可得反应CaO(s)+2Al(s)+7H2O(l)=Ca2+(aq)+2[Al(OH)4]-(aq)+3H2(g),则ΔH4=ΔH1+ΔH2+2ΔH3=(-65.17kJ⋅mol-1)+(-16.73kJ⋅mol-1)+2´(-415.0kJ⋅mol-1)=-911.9kJ⋅mol-1。
17.【2022年全国甲卷】金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石转化为,再进一步还原得到钛。回答下列问题:
(1)转化为有直接氯化法和碳氯化法。在时反应的热化学方程式及其平衡常数如下:
(ⅰ)直接氯化:
(ⅱ)碳氯化:
①反应的为_______,_______Pa。
【答案】(1) -223 1.2×1014
【解析】
(1)①根据盖斯定律,将“反应ⅱ-反应ⅰ”得到反应2C(s)+O2(g)=2CO(g),则∆H=-51kJ/mol-172kJ/mol=-223kJ/mol;则Kp===1.2×1014Pa;
18.(2012·江苏高考真题)铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原-氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g) △H=a kJ·mol-1
3AlCl(g)=2Al(l)+AlCl3(g) △H=b kJ·mol-1
①反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=________kJ·mol-1(用含a、b 的代数式表示)。
②Al4C3是反应过程中的中间产物。Al4C3与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为____________________________________________。
【答案】(1)①a+b ②Al4C3+12HCl=4AlCl3+3CH4↑
【解析】
(1)①根据盖斯定律,将题中所给两方程式相加得Al2O3(s)+3C(s)=2Al(l)+3CO(g),对应的△H=(a+b)kJ•mol﹣1,故答案为a+b;
②含氢量最高的烃为CH4,根据碳原子守恒,3个碳需要结合12个H原子形成3个CH4,再由铝原子守恒,4个铝需要结合12个Cl形成4个AlCl3,所以Al4C3与HCl之间为1:12参加反应,故该反应方程式为:Al4C3+12HCl=4AlCl3+3CH4↑;
19.(2020·山东高考真题)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.
Ⅱ.
Ⅲ.
回答下列问题:
(1)_________。
【答案】(1)+40.9
【解析】
(1).根据反应I-II=III,则△H3=△H1-△H2=-49.5kJ∙mol-1-(-90.4 kJ∙mol-1)=+40.9 kJ∙mol-1;
20.(2017·全国高考真题)[2017·新课标Ⅲ]砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(3)已知:As(s)+H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+O2(g)=H2O(l) ΔH2
2As(s)+O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
【答案】(3) 2△H1−3△H2−△H3
【解析】
(3)待求解反应可以由反应①×2-反应②×3-反应③,则△H=2△H1-3△H2-△H3 ;
21.(2009·山东高考真题)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(2)O2(g)= O+2(g)+e- H1=1175.7kJ·mol-1
PtF6(g)+ e-1PtF6-(g)H2= -771.1 kJ·mol-1
O2+PtF6-(s)=O2+(g)+PtF6- H3=482.2 kJ·mol-1
则反应O2(g)+ PtF6 (g) = O2+PtF6- (s)的H=_____________ kJ·mol-1。
(3)在25℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________
【答案】(2) -77.6
【解析】
(2)已知①O2(g)= O+2(g)+e- ΔH1=1175.7kJ·mol-1;
②PtF6(g)+ e-PtF6-(g) ΔH2= -771.1 kJ·mol-1;
③O2+PtF6-(s)=O2+(g)+PtF6- ΔH3=482.2 kJ·mol-1;
根据盖斯定律,将化学方程式①+②-③叠加得到:O2(g)+ PtF6 (g) = O2+PtF6- (s) ΔH=-77.6 kJ·mol-1
因此,本题正确答案为:-77.6 ;
22.(2016·全国高考真题)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(3)①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________________。
【答案】(3) △H4=2△H3-2△H2-△H1 反应放热量大、产生大量气体
【解析】
(3)根据盖斯定律,反应热效应之间的关系式为△H4=2△H3-2△H2-△H1。联胺有强还原性,N2O4有强氧化性,两者在一起易发生自发地氧化还原反应,反应放热量大、产生大量气体,所以联氨和N2O4可作为火箭推进剂。
23.(2018·江苏高考真题)NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)用水吸收NOx的相关热化学方程式如下:
2NO2(g)+H2O(l)HNO3(aq)+HNO2(aq) ΔH=−116.1 kJ·mol−1
3HNO2(aq)HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol−1
反应3NO2(g)+H2O(l)2HNO3(aq)+NO(g)的ΔH=___________kJ·mol−1。
【答案】(1)−136.2
【解析】
(1)将两个热化学方程式编号,
2NO2(g)+H2O(l)=HNO3(aq)+HNO2(aq) ΔH=−116.1 kJ·mol−1(①式)
3HNO2(aq)=HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol−1(②式)
应用盖斯定律,将(①式3+②式)2得,反应3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)ΔH=[(−116.1 kJ·mol−1)3+75.9 kJ·mol−1]2=-136.2kJ·mol−1。
24.(2013·江苏高考真题)磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)= 6CaO(s)+P4(s)+10CO(g) △H1="+3359.26" kJ·mol-1
CaO(s)+SiO2(s)= CaSiO3(s) △H2=-89.61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)= 6CaSiO3(s)+P4(s)+10CO(g) △H3
则△H3= kJ·mol-1。
【答案】(1)2821. 6
【解析】
应用化学反应原理分析相关问题,得出合理答案。
(1)2Ca3(PO4)2(s)+10C(s)=6CaO(s)+P4(s)+10CO(g) ΔH=+3359.26 kJ·mol-1①
CaO(s)+SiO2(s)=CaSiO3(s) ΔH2=-89.61 kJ·mol-1②根据盖斯定律,①+②×6得ΔH3=+2821.6 kJ·mol-1。
十年(23-22)高考化学真题分项汇编专题79 工艺流程 溶度积计算(2份打包,原卷版+教师版): 这是一份十年(23-22)高考化学真题分项汇编专题79 工艺流程 溶度积计算(2份打包,原卷版+教师版),文件包含十年23-22高考化学真题分项汇编专题79工艺流程溶度积计算原卷版doc、十年23-22高考化学真题分项汇编专题79工艺流程溶度积计算教师版doc等2份试卷配套教学资源,其中试卷共36页, 欢迎下载使用。
十年(23-22)高考化学真题分项汇编专题53 烃(2份打包,原卷版+教师版): 这是一份十年(23-22)高考化学真题分项汇编专题53 烃(2份打包,原卷版+教师版),文件包含十年23-22高考化学真题分项汇编专题53烃原卷版doc、十年23-22高考化学真题分项汇编专题53烃教师版doc等2份试卷配套教学资源,其中试卷共16页, 欢迎下载使用。
十年(23-22)高考化学真题分项汇编专题41 化学平衡常数及计算(2份打包,原卷版+教师版): 这是一份十年(23-22)高考化学真题分项汇编专题41 化学平衡常数及计算(2份打包,原卷版+教师版),文件包含十年23-22高考化学真题分项汇编专题41化学平衡常数及计算原卷版doc、十年23-22高考化学真题分项汇编专题41化学平衡常数及计算教师版doc等2份试卷配套教学资源,其中试卷共40页, 欢迎下载使用。












