

- 新教材2023高中化学第七章有机化合物质量评估新人教版必修第二册 试卷 试卷 0 次下载
- 新教材2023高中化学第八章化学与可持续发展第一节自然资源的开发利用课时1金属矿物的开发利用同步测试新人教版必修第二册 试卷 0 次下载
- 新教材2023高中化学第八章化学与可持续发展第一节自然资源的开发利用课时3煤石油和天然气的综合利用同步测试新人教版必修第二册 试卷 0 次下载
- 新教材2023高中化学第八章化学与可持续发展第三节环境保护与绿色化学同步测试新人教版必修第二册 试卷 0 次下载
- 新教材2023高中化学第八章化学与可持续发展第二节化学品的合理使用课时1化肥农药的合理施用合理用药同步测试新人教版必修第二册 试卷 0 次下载
高中化学人教版 (2019)必修 第二册第八章 化学与可持续发展第一节 自然资源的开发利用课时练习
展开第一节 自然资源的开发利用
课时2 海水资源的开发利用
【基础巩固】
1.(2022·广东汕头)所谓海水淡化是指除去海水中的盐分以获得淡水的工艺过程(又称海水脱盐),其方法较多,如反渗透法、水合物法、电渗析法和压渗析法等。下列方法中也可以用来进行海水淡化的是 ( )
A.过滤法 B.蒸馏法 C.分液法 D.冰冻法
答案:B
2.许多国家十分重视海水资源的综合利用,下列不需要经过化学变化就能从海水中获得的物质是 ( )
A.Cl2、Br2、I2 B.Na、Mg、Al
C.食盐、淡水 D.NaOH、H2
答案:C
3.(2022·广东广州)海水是巨大的化学资源库,下列有关海水综合利用的说法正确的是 ( )
A.从海水中获得淡水的过程发生了化学变化
B.海水中含有溴单质,通入空气和水蒸气可将溴单质吹出
C.海水晒盐可以得到NaCl,电解熔融NaCl可制备金属Na
D.利用海水、铝、空气制成航标灯的原理是将电能转化为化学能
解析:A项,从海水中获得淡水是利用蒸馏的方法,该过程属于物理变化,并未发生化学变化,错误;B项,海水中并不含有溴单质,而是含有大量的溴离子,需先通入氯气将溴离子氧化为溴单质,然后通入空气和水蒸气可将溴单质吹出,错误;C项,海水晒盐可以得到NaCl,电解熔融NaCl:2NaCl(熔融)![]() 2Na+Cl2↑,可制备金属Na,正确;D项,利用海水、铝、空气制成航标灯是利用原电池的原理,将化学能转化为电能,错误。
2Na+Cl2↑,可制备金属Na,正确;D项,利用海水、铝、空气制成航标灯是利用原电池的原理,将化学能转化为电能,错误。
答案:C
4.某课外小组将灼烧海带产生的灰烬浸泡后过滤,得到澄清的滤液。他们设计了如下的几个方案,你认为下列证明海带的灰烬中是否含有碘元素的操作中正确的是 ( )
A.取适量滤液,蒸干,观察是否有紫色固体生成
B.取适量滤液,加入苯,振荡,静置,苯层无色,证明不含碘元素
C.取适量滤液,向其中加入淀粉溶液,无明显现象,证明不含碘元素
D.取适量滤液,加入酸化的H2O2,再加入淀粉溶液,呈蓝色,证明含有碘元素
解析:海带的灰烬中含有的碘元素是以I-形式存在的,不是以单质形式存在的,所以A、B、C项均不正确;D项中发生了氧化还原反应:H2O2+2I-+2H+![]() I2+2H2O,产生了I2,使淀粉溶液呈蓝色。
I2+2H2O,产生了I2,使淀粉溶液呈蓝色。
答案:D
5.(2022·广东江门)浩瀚的海洋是一个巨大的资源宝库,工业上常用浓缩海水提取溴。
浓缩海水![]() 粗产品溴
粗产品溴![]() 溴蒸气
溴蒸气![]() 物质X
物质X![]()
![]() …
…![]() 产品溴
产品溴
下列说法错误的是 ( )
A.海水的淡化方法主要有蒸馏法、反渗透法和电渗析法等
B.步骤②中体现了溴易挥发的性质
C.①~④目的是富集溴元素
D.步骤③反应的离子方程式为Br2+SO2+2H2O![]() 2HBr+2H++S
2HBr+2H++S![]()
解析:A项,海水的淡化方法主要有蒸馏法、反渗透法和电渗析法等,正确;B项,步骤②中热空气能将溴吹出,体现了溴易挥发的性质,正确;C项,①~④过程溴的浓度逐渐增大,是溴元素的富集过程,正确;D项,溴化氢是强酸,所以步骤③反应的离子方程式应为Br2+SO2+2H2O![]() 2Br-+4H++S
2Br-+4H++S![]() ,错误。
,错误。
答案:D
6.溴有“海洋元素”之称,海水中溴含量为65 mg·L-1。在实验室模拟海水中溴的提取,
实验方法:将适量新制氯水加入20 mL富含溴离子的海水中(海水可以用0.1 mol·L-1的NaBr溶液代替),把溴置换出来。氯水中的氯气作
剂,涉及反应的离子方程式为 。
得到的单质溴可以用有机溶剂在 (填仪器名称)中实现萃取富集,萃取试剂用 、苯等,得到的有机层显 色。
答案:氧化 Cl2+2Br-![]() 2Cl-+Br2 分液漏斗 四氯化碳 橙
2Cl-+Br2 分液漏斗 四氯化碳 橙
【拓展提高】
7.(2022·广东东莞)利用海水提取溴和镁的过程如下图,下列说法错误的是 ( )
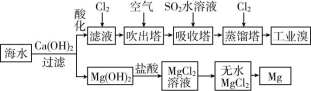
A.工业上常利用电解熔融MgCl2冶炼金属镁
B.工业溴中含有少量Cl2,可用NaOH溶液除去
C.富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D.若提取1 mol工业溴,至少需要标准状况下44.8 L的Cl2
解析:A项,Mg为活泼金属,工业上常利用电解熔融MgCl2冶炼金属Mg,正确;B项,溴、氯气均与NaOH溶液反应,不能除杂,错误;C项,溴易挥发,因此在富集溴元素过程中,可以用空气吹出法,正确;D项,由流程可知,若提取1 mol溴,需要通入两次氯气,则至少需要标准状况下氯气为2 mol×22.4 L·mol-1= 44.8 L,正确。
答案:B
8.(2022·广东深圳)海洋植物如海带、海藻中含有丰富的碘元素。下图为从海带中提取碘的工业生产流程,下列有关说法错误的是( )
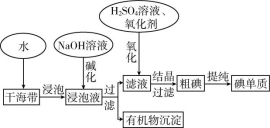
A.生产过程中通常将干海带粉碎的目的是增大海带与水的接触面积
B.干海带浸泡液中的碘离子可用淀粉溶液检验
C.工业上不直接从海水提取碘的原因是海水中碘的浓度很低
D.从海带中提取碘的过程利用了氧化还原反应原理
解析:A项,干海带粉碎的目的是增大海带与水的接触面积,有利于海带中的碘化物充分溶于水中,正确;B项,淀粉遇到碘单质变蓝,与碘离子不发生颜色反应,所以不能用淀粉检验碘离子,错误;C项,海水中的碘化物的浓度很低,不能直接提取,应浓缩后再提取,正确;D项,碘离子转化为碘单质的反应属于氧化还原反应,正确。
答案:B
9.海水中含有丰富的化学元素,某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr形式存在)及综合利用的生产流程简图如图所示。
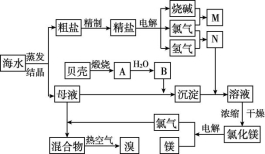
请回答下列问题。
(1)Mg(OH)2中加入盐酸后,要获得MgCl2·6H2O晶体,需要进行的实验操作依次为 (填字母)。
A.蒸馏 B.灼烧 C.过滤 D.蒸发 E.冷却结晶
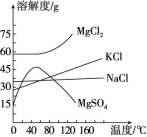 (2)母液中常含有MgCl2、NaCl、MgSO4、KCl等,可进一步加工制得一些重要的产品。下图是上述四种物质的溶解度曲线图,若将母液加热升温到60 ℃以上,随着水分的蒸发,会逐渐析出晶体,此晶体的主要成分是 。
(2)母液中常含有MgCl2、NaCl、MgSO4、KCl等,可进一步加工制得一些重要的产品。下图是上述四种物质的溶解度曲线图,若将母液加热升温到60 ℃以上,随着水分的蒸发,会逐渐析出晶体,此晶体的主要成分是 。
(3)过滤上述晶体后,将滤液降温到30 ℃以下,又逐渐析出晶体,用一定
量的冷水洗涤该晶体,最后可得到比较纯净的 晶体。
答案:(1)DEC (2)MgSO4、NaCl (3)KCl
【挑战创新】
10.空气吹出法工艺是目前“海水提溴”的最主要方法之一。其工艺流程如下:
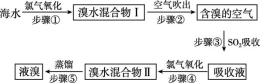
(1)步骤③的离子方程式: 。
(2)步骤⑤中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是 。
(3)溴水混合物Ⅱ中溶有一定量的氯气,因此在步骤⑤中可将蒸馏产生的气体通过 (填试剂名称)溶液,以除去氯气。
(4)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因: 。
(5)步骤①中用硫酸酸化可提高Cl2的利用率,理由是 。
(6)提取溴单质,采用蒸馏“溴水混合物Ⅱ”而不是蒸馏“溴水混合物Ⅰ”,请说明原因: 。
答案:(1)Br2+SO2+2H2O![]() 4H++2Br-+S
4H++2Br-+S![]() (2)分液漏斗
(2)分液漏斗
(3)溴化钾(或其他含Br-的盐类物质)
(4)温度过高,大量水蒸气随溴被蒸出,溴蒸气中水增加;温度过低,溴不能完全蒸出,产率低
(5)酸化可抑制Cl2、Br2与水反应
(6)将“溴水混合物Ⅰ”转变为“溴水混合物Ⅱ”是Br2的浓缩过程,可提高效率,减少能耗,降低成本
人教版 (2019)必修 第二册第一节 自然资源的开发利用第1课时练习题: 这是一份人教版 (2019)必修 第二册<a href="/hx/tb_c4000054_t7/?tag_id=28" target="_blank">第一节 自然资源的开发利用第1课时练习题</a>,共6页。试卷主要包含了下列有关金属冶炼的描述正确的是,海水蕴藏着丰富的化学资源,下列化工生产原理错误的是等内容,欢迎下载使用。
化学必修 第二册第一节 自然资源的开发利用第一课时巩固练习: 这是一份化学必修 第二册<a href="/hx/tb_c4000054_t7/?tag_id=28" target="_blank">第一节 自然资源的开发利用第一课时巩固练习</a>,共5页。试卷主要包含了下列有关金属冶炼的描述正确的是,海水蕴藏着丰富的化学资源,下列化工生产原理错误的是等内容,欢迎下载使用。
人教版 (2019)必修 第二册第一节 自然资源的开发利用第2课时当堂检测题: 这是一份人教版 (2019)必修 第二册<a href="/hx/tb_c4000054_t7/?tag_id=28" target="_blank">第一节 自然资源的开发利用第2课时当堂检测题</a>,共2页。试卷主要包含了下列方法中能将海水淡化的是,从淡化海水中提取溴的流程如下等内容,欢迎下载使用。














