所属成套资源:【期末复习】高一化学单元复习知识点梳理(人教版2019必修第二册)
第8章 化学与可持续发展——【期末复习】高一化学单元复习知识点梳理(人教版2019必修第二册)
展开
这是一份第8章 化学与可持续发展——【期末复习】高一化学单元复习知识点梳理(人教版2019必修第二册),共8页。
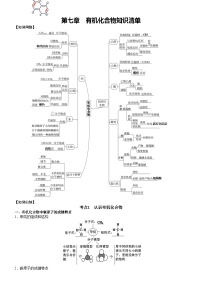
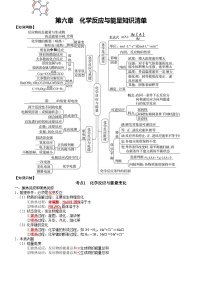
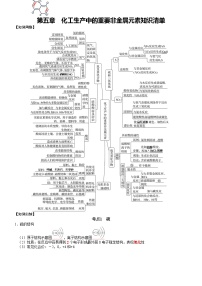
第八章 化学与可持续发展知识清单【知识网络】【知识归纳】考点1 自然资源的开发利用一、金属矿物的开发利用1.金属在自然界中存在的形态(1)游离态:少数金属,如金、铂(2)化合态:绝大多数金属2.金属冶炼的原理和实质(1)原理:采用加热、通电或使用还原剂等措施将金属从其化合物中还原出来(2)实质:用还原剂使化合态的金属得到电子变为金属单质3.金属冶炼的三个步骤及目的4.冶炼方法(1)根据金属活泼性选择冶炼方法(2)电解法①电解熔融的氯化钠:2NaCl2Na+Cl2↑②电解熔融的氯化镁:MgCl2Mg+Cl2↑③电解熔融的氧化铝:2Al2O34Al+3O2↑(3)热还原法①工业上炼铁:Fe2O3+3CO2Fe+3CO2②工业上炼钨:WO3+3H2W+3H2O③铝热法炼铬:Cr2O3+2Al2Cr+Al2O3④工业上炼铜:2CuO+C2Cu+CO2↑⑤工业上炼钛:4Na+TiCl44NaCl+Ti(4)热分解法①工业上炼汞:2HgO2Hg+O2↑②工业上炼银:2Ag2O4Ag+O2↑(5)湿法炼铜:Fe+CuSO4=FeSO4+Cu5.铝热反应实验(1)实验装置①镁的作用:燃烧放出的热量引燃铝热反应(引燃剂)②氯酸钾作用:对镁的燃烧起助燃作用(助燃剂)(2)注意事项①镁带要打磨干净表面的氧化膜,否则难以点燃;氧化铁粉末与铝粉要选择干燥的;铝粉要用没有被氧化的,否则反应难以进行。②氧化铁粉末与铝粉两者要混合均匀,以保证氧化铁与铝都完全反应。③内层滤纸要用水润湿,以防止纸漏斗燃烧。④蒸发皿中的细沙要适量,既要防止蒸发皿炸裂,又要防止熔融的液体溅出伤人。6.合理开发和利用金属资源(1)提高金属矿物的利用率(2)开发环保高效的金属冶炼方法(3)防止金属腐蚀(4)加强金属资源的回收和再利用(5)使用其他材料代替金属材料二、海水资源的开发利用1.海水水资源的利用类型(1)海水水资源的利用(2)海水蒸馏原理及装置①蒸馏烧瓶规格的选择:液体体积占烧瓶容积的1/3②冷却水的进出口:下进上出,采用逆流原理冷却效果好③蒸馏过程:开始时,先通冷凝水,再加热;结束时,先停热,再停通冷凝水④防暴沸方法:预先加入沸石或碎瓷片⑤忘记加沸石:先停热,再冷却,后补加2.海水化学资源的利用(1)制氯化钠及生产烧碱、纯碱、钠、氯气、盐酸等(2)制取镁、钾、溴及其他产品(3)从海水中获取化学物质的方法(4)海水提溴流程①流程②主要过程及反应原理(5)海水提镁流程①制石灰乳:CaCO3CaO+CO2↑、CaO+H2OCa(OH)2②沉淀Mg2+:Ca(OH)2+MgCl2Mg(OH)2↓+CaCl2③提取MgCl2:Mg(OH)2+2HClMgCl2+2H2O④制氯化镁晶体:MgCl2+6H2OMgCl2·6H2O⑤氯化镁晶体脱水:MgCl2·6H2OMgCl2+6H2O⑥制金属镁:MgCl2(熔融)Mg+Cl2↑【特别提醒】制氯化镁晶体的基本操作:加热浓缩、冷却结晶、过滤洗涤、干燥称量(6)海带提碘①流程②反应原理:Cl2+2I-I2+2Cl-③灼烧所用的仪器④萃取和分液操作3.海水能源资源的利用(1)从海水中提取铀和重水作核能的原料(2)开发潮汐能、波浪能等新型能源三、煤、石油和天然气的综合利用1.煤的组成与综合利用(1)煤的组成(2)煤的综合应用2.天然气的综合利用3.石油的综合利用(1)组成:多种碳氢化合物组成的混合物(2)利用方法【特别提醒】(1)煤的干馏、气化、液化以及石油的裂化、裂解和重整都是化学变化,只有石油的分馏属于物理变化。(2)煤、石油及其加工产品都是混合物。(3)从产品角度认识裂化和裂解的区别4.化学“六气”的主要成分 高炉煤气水煤气天然气液化石油气焦炉气裂解气主要成分CO、CO2H2、COCH4C3H8、C4H10C3H6、C4H8H2、CH4C2H4、COC2H4、C3H6C4H8、CH4考点2 化学品的合理使用一、化肥、农药的合理使用1.化学品的分类2.合理使用化肥(1)根据化肥本身的性质进行科学施用(2)过量施用化肥易造成水体富营养化化,产生水华等污染现象(3)不合理施用化肥会影响土壤的酸碱性和土壤结构3.合理使用农药(1)农药种类(2)农药发展的方向:高效、低毒、低残留(3)不合理施用农药的危害①会造成土壤和作物农药残留超标②会造成大气、地表水和地下水污染【特别提醒】不同化肥混合施用时可能会造成肥效的降低,如草木灰不能与铵态氮肥混合施用。二、合理用药1.药物分类2.药物在人体内的作用方式(1)改变机体细胞周围的物理及化学环境(2)药物分子和机体生物大分子的功能基团相结合3.阿司匹林(1)合成反应(2)化学名称:乙酰水杨酸(3)功效:解热镇痛(4)不良反应①在人体内产生的水杨酸会刺激胃肠粘膜②长期服用可能导致胃痛、头疼、眩晕、恶心等症状4.合理使用药物(1)遵循原则:安全、有效、经济和适当(2)防止滥用药物①长期服用安眠药或镇静剂②滥用抗生素③运动员服用兴奋剂(3)拒绝毒品【特别提醒】胃溃疡患者服用抗酸药的选择三、安全使用食品添加剂1.功能(1)改善食品品质和色、香、味(2)满足防腐、保鲜和加工工艺需要2.分类(1)按来源①天然食品添加剂②人工合成食品添加剂(2)按功能类别功能品种着色剂改善食品色泽 天然色素如红曲红等;合成色素如柠檬黄等 增味剂增加食品鲜味 味精(谷氨酸钠)膨松剂使食品膨松或酥脆碳酸氢铵、碳酸氢钠凝固剂改善食品形态 盐卤、葡萄糖酸-δ-内酯防腐剂防止食品腐败变质 苯甲酸及其钠盐、山梨酸及其钾盐抗氧化剂防止食品因氧化而变质 抗坏血酸(维生素C)营养强化剂 补充必要的营养成分 碘酸钾、维生素、碳酸钙、硫酸亚铁、硫酸锌 3.使用原则考点3 环境保护与绿色化学一、化学与环境保护1.环境问题2.工业“三废”:废气、废水、废渣(1)空气污染指数的项目:SO2、NO2、CO、O3和可吸入颗粒物等(2)污水处理(3)固体废弃物的处理(4)次生污染物的形成3.常见环境污染问题4.常见工业尾气的主要成分及处理方法尾气主要成分处理方法硫酸厂尾气SO2、O2、N2等用氨水吸收硝酸厂尾气NO、NO2、N2、O2等用NaOH溶液吸收高炉煤气CO、CO2、N2等回收利用炼钢烟气Fe2O3烟尘、CO等回收利用焦炉气H2、CH4、CO、CO2、C2H4、N2可用作燃料氯碱工业Cl2用NaOH溶液吸收二、绿色化学1.绿色化学的核心和最高目标(1)核心:利用化学原理从源头上减少和消除工业生产对环境的污染(2)最高目标:原子利用率为100%,即反应物中的原子全部转化为期望的最终产物(3)原子利用率100%的化学反应:化合反应、加成反应和加聚反应2.绿色化学核心理念3.绿色化学的研究对象(1)设计对人类健康和环境危害小的反应起始物,淘汰有毒的反应起始物。(2)选择最佳的反应条件,以实现最大限度的节能和零排放。(3)研究最佳的转换反应和良性试剂。(4)设计对人类健康和环境更安全的目标化合物4.绿色化学对化学反应的要求5.原子经济性(1)原子利用率=×100%(2)原子经济百分数=×100%6.开发和利用自然资源遵循的原则
相关试卷
这是一份第3章 简单的有机化合物——【期末复习】高一化学单元复习知识点梳理(鲁科版2019必修第二册),共19页。
这是一份第2章 化学键 化学反应规律——【期末复习】高一化学单元复习知识点梳理(鲁科版2019必修第二册),共10页。
这是一份专题9 金属与人类文明——【期末复习】高一化学单元复习知识点梳理(苏教版2019必修第二册),共4页。试卷主要包含了金属的存在,常见金属的存在,主要产品,其他铝热反应,应用等内容,欢迎下载使用。