

上海市杨浦区控江中学2022-2023学年高一下学期期中考试化学试卷(Word版含答案)
展开控江中学2022-2023学年高一下学期期中考试
化学试卷
可能用到的相对原子质量:H-1、N-14、O-16、S-32
一、自然界中的氮元素(本题共24分)
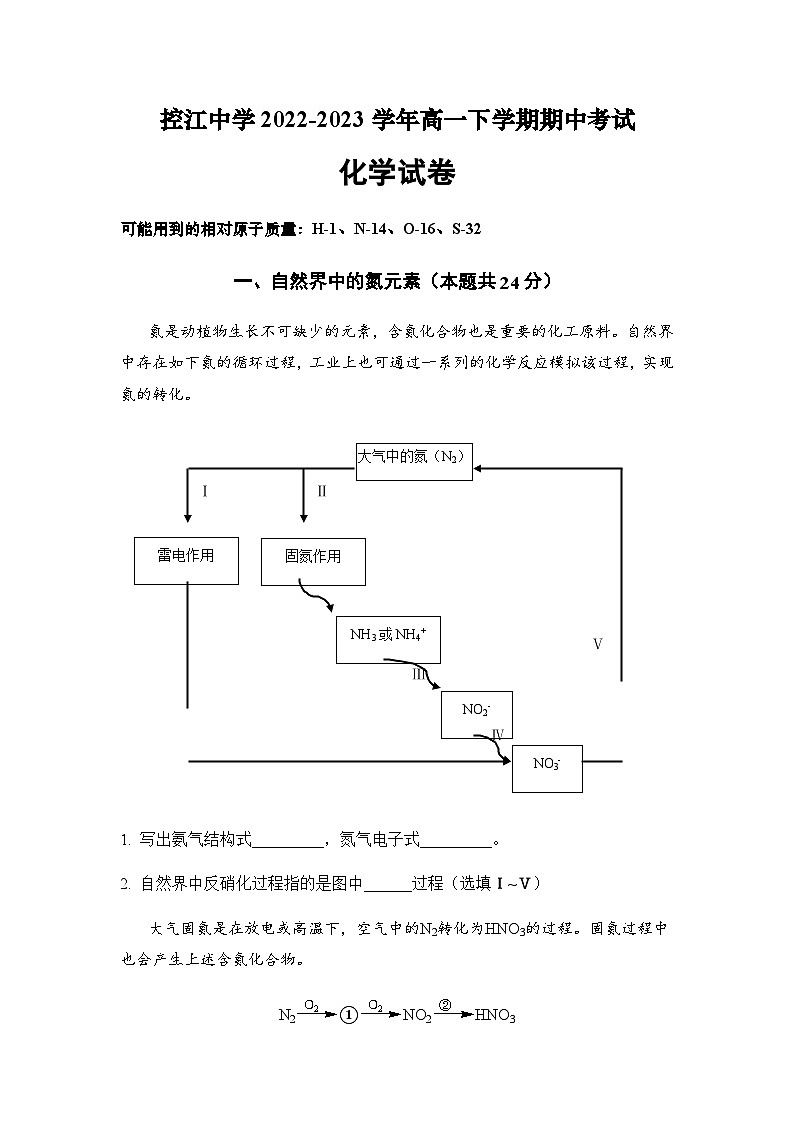
氮是动植物生长不可缺少的元素,含氮化合物也是重要的化工原料。自然界中存在如下氮的循环过程,工业上也可通过一系列的化学反应模拟该过程,实现氮的转化。
- 写出氨气结构式_________,氮气电子式_________。
- 自然界中反硝化过程指的是图中______过程(选填Ⅰ~Ⅴ)
大气固氮是在放电或高温下,空气中的N2转化为HNO3的过程。固氮过程中也会产生上述含氮化合物。
N2①NO2HNO3
- ①为___________(填写化学式)。
- 上述转化关系中四种含氮物质中,属于共价化合物的有_____种,含共价键的有_____种。
- 写出过程②的反应方程式___________,该反应中氧化剂与还原剂物质的量之比为______。
含氮量是衡量肥效的指标之一,常见氮肥:CO(NH2)2(尿素)、NH4NO3和(NH4)2SO4
- NH4NO3中含有的化学键包括_____________。
- 等物质的量NH4NO3和(NH4)2SO4的混合物,与足量氢氧化钠加热,产生气体10.08L(标准状况下),发生的离子方程式为__________________,固体混合物质量为________g。
- 设计实验检验上述化肥样品混合物中的硫酸根
___________________________________________________。
- 写出铵态氮肥保存或施用时注意事项(任写一点)
___________________________________________________。
土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:
___K2S+___KNO3+___H2O___N2↑+___K2SO4+___KOH
- 配平上述反应方程式,并标出电子转移的方向和数目。
- 被氧化的元素是______。
二、青年化学家元素周期表(本题共26分)
为纪念元素周期表诞生150周年,IUPAC等从世界范围征集优秀青年化学家提名,形成一张“青年化学家元素周期表”,向世界介绍118位优秀青年化学家,有8位中国青年化学家成为“N、S、Hg、U”等元素的代言人。
- 汞的原子结构示意图,汞在元素周期表中位于第________周期。
- 氮在周期表第______列,周期表中位置是____________________。
- 下列有关性质的比较,不能用元素周期律解释的是____________。
A.酸性:HCl>H2S | B.非金属性:O>S |
C.碱性:NaOH>Mg(OH)2 | D.热稳定性:HCl>H2S |
15. 非金属性:N>C,用一个化学方程式证明__________________________。
元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列数字①~⑨分别代表某种化学元素。请依据这9种元素回答下列问题。
① |
|
| |||||||||||||||
|
|
|
| ② | ③ |
|
|
| |||||||||
④ | ⑤ |
|
|
| ⑥ | ⑦ |
| ||||||||||
⑧ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ⑨ |
|
16. 非金属性最强的元素是_________。(填元素符号)
17 ⑨的最高价氧化物对应水化物的化学式是_______________。(填化学式)
18. 表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是_____________________(填离子符号)。
19. 任意例举一个实验事实说明金属性④>⑤:___________________。
20. 化合物M由9种元素中2种元素甲、乙组成,M电子式可表示为,则M化学式为____________。(填元素符号)
21. 1971年在星际空间发现一种由①、②、③三种元素组成的直线型分子X。X的摩尔质量为51g·mol-1,且X分子中共含5个原子(各原子均满足稀有气体原子的稳定结构),X分子式为_________,结构式为 。
科学家合成了一种新化合物(如图所示),其中X、Y、Na为同一短周期元素,且化合物中所有原子均达到8电子稳定结构。
22.原子半径:Na______Si(>、<或=)。
23.由题意可推知Y是Cl,推得此结论的依据是 。
X元素的简单氢化物电子式为___________。
三、葡萄酒中的二氧化硫(本题共28分)
土法酿造葡萄酒(只加糖的纯天然酿酒法)容易出问题,主要原因是发酵过程产生的菌种多达百种,难以控制而产生对神经有毒的甲醇等物质。科学酿酒需加SO2等辅料,我国国家标准(GB27602014)规定葡萄酒中SO2的残留量≤0.25 g·L-1。
24. 葡萄酒中添加SO2的作用可能是________。
A.氧化细菌 B.抗氧化 C.漂白 D.增酸作用
Ⅰ.实验方案一
利用SO2的漂白性检测干白葡萄酒(液体为无色)中的SO2或H2SO3。设计如图1的实验:
25. SO2水溶液显酸性,用离子方程式说明________________________。
26. 甲同学得出的实验结论是干白葡萄酒中不含SO2或H2SO3。这个结论______
______(填“成立”或“不成立”),理由是_________________。
Ⅱ.实验方案二
用如图实验装置探究二氧化硫的氧化性。按图2充入气体,连接装置,关闭旋塞1和2
- 打开旋塞1,可观察到的主要现象是
______________________。
28. 若A瓶和B瓶的体积相等,恢复到常温,关闭旋塞1,打开旋塞2,可观察到的现象是____________________________________________,此时B瓶中可能发生反应的化学方程式为_______________________________。
29. 若图2装置中充入H2S和SO2的混合气体共1mol,充分反应后,所得氧化产物比还原产物多0.25mol,则原混合气体中H2S和SO2的体积比可能是_______。
A. | B. | C. | D. |
30. 在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为__________mol/L。
在上述实验中,采用铜和浓硫酸制备SO2,应放置在下列____(填序号)中进行反应。
探究二氧化硫的还原性
31. 图2装置中将氢氧化钠溶液换为_______溶液,即可验证二氧化硫还原性。
32. 将SO2气体通入下列装置中,一定不可能产生沉淀的共_____项。(填写数字)
33. 将SO2气体通入CuCl2溶液中,生成CuCl沉淀的同时,还有产物HCl和H2SO4。请写出该反应的化学方程式______________________________。
Ⅲ.实验方案三
搭建图示装置为测定某葡萄酒中SO2的含量:
实验步骤如下:在B中加入300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应。除去C中剩余的H2O2后,用0.090 0 mol·L-1 NaOH溶液测定反应生成的酸,消耗NaOH溶液25.00 mL。
34. C中通入SO2发生反应的化学方程式为________。
35. 通过计算求出该葡萄酒中SO2的含量(以g·L-1为单位,即每升葡萄酒中含有SO2的质量)____________。
36. 该测定结果比实际值偏高,可能的原因是_____________________。
37 . 针对此原因提出一条改进措施:____________________________。
四、雾霾与脱硝(本题共22分)
中国科学院官方微信于2017年3月发表《灰霾专题》,提出灰霾中细颗粒物的成因,部分分析如下图所示。
- 根据上图信息可以看出,下列哪种气体污染物不是由机动车行驶造成的
A.SO2 B.NOx C.VOCs D.NH3
硫氧化率(SOR)和氮氧化率(NOR)通常用来分别表示气体污染物SO2和NO2向和的转化程度。SOR和NOR的计算公式为:
已知PM2.5中主要以(NH4)2SO4形式存在,主要以NH4NO3形式存在。(NH4)2SO4比NH4NO3更稳定;NH4NO3和HNO3加热或光照均易分解。
某地SOR和NOR的数据如下表所示:
季节 | 春季 | 夏季 | 秋季 | 冬季 | 平均 |
SOR | 0.29 | 0.42 | 0.28 | 0.26 | 0.31 |
NOR | 0.21 | 0.14 | 0.23 | 0.25 | 0.21 |
- 由上表数据可知,SOR和NOR差异最大的季节是______________。
A.春季
B.夏季
C.秋季
D.冬季
40. 结合相关化学原理推测该季节产生这种差异可能的原因。______________________。
41. 设r = c()/c(),r值可以较好地反映机动车等移动源污染与燃煤等固定源污染的相对大小。已知某地PM2.5浓度及r值随季节变化如右图所示。根据该图分析,造成秋冬季节PM2.5偏高的首要原因是_____。
A.移动源污染 B.固定源污染
42. 假如你是城市管理者,请你提出一条有针对性的措施,以缓解秋冬季节PM2.5污染较严重的问题。____________________________。
烟气脱硝(将NOx转化成无害物质)是工业废气处理中的重要工艺。相对传统的处理工艺,活性炭吸附脱硝法具有工艺过程无二次污染、氮资源和脱硝剂可循环利用等优点。回答下列问题。
Ⅰ.活性炭吸附脱硝法的工艺流程如图所示。
43. 该流程中活性炭的作用是 ,若入口烟气中NOx以NO形式参加反应,则相应的化学方程式为 。
Ⅱ.某同学选择如下装置(省略夹持仪器)对该方法进行模拟实验:
44. 实验前,按h→j,i→k的顺序连接仪器,检查装置 。按h→j而不是h→k连接仪器的原因是 。
45. 先通入空气,再打开A、B中分液漏斗的活塞,观察到B中出现红棕色气体,此时,所获得的氮氧化物中一定含有 气体。
46. 装置F除了能用于判断气体流速和脱硝效果外,还可用于 。
47. 为达到更好的脱硝效果,实验中应采取的措施有 (任写1种)。
48. 常温常压下,以一定流速和比例混合NO、NH3、空气等气体进行模拟实验,现测得NO入口体积分数为3×10-4,出口体积分数为6×10-5,则脱硝百分率为 %(因混合气体中NO所占比例很小,可忽略脱硝前后气体总体积的变化,计算结果保留小数点后1位)。
控江中学2022-2023学年高一下学期期中考试
化学
参考答案
一、自然界中的氮元素(本题共24分)
- (1分),(1分)
- Ⅴ(2分)
- NO(1分)
- 3种(1分),4种(1分)
- 3NO2+H2O===2HNO3+NO(1分),1:2(1分)
- 离子键和共价键(2分)
- NH4++OH-NH3↑+H2O(2分),31.8g(2分)
- 取化肥样品溶于水,加入足量稀盐酸后,无沉淀,再加入氯化钡,若产生白色沉淀,证明固体样品中含有硫酸根(2分)
- 保存:避光避热;施用:不与碱性物质一同使用,深施盖土(任意1点,2分)
- 5K2S+8KNO3+4H2O4N2↑+5K2SO4+8KOH(4分,配平2分,方向数目合计2分,方向和数目错其中之一即不给分)
- K2S中-2价的硫元素(1分)
二、青年化学家元素周期表(本题共26分)
- 六(1分)
- 第15列(2分),第二周期,第ⅤA族或第15族(2分,周期1分,族1分)
- A(2分)
15. CaCO3+2HNO3===Ca(NO3)2+H2O+CO2↑(2分)
16. Cl(1分)
17. HBrO4(1分)
18. S2->Cl->K+ (2分)
19. Na与冷水剧烈反应,镁与热水缓慢反应(2分)
20. S2Br2或S2Cl2(2分,写出其中一个即给分)
21. C3HN(2分,元素符号顺序颠倒均可),(2分)
22.>(1分)
23.Y在第三周期,且Y和Si间只有一根共价键(2分)
(2分)
三、葡萄酒中的二氧化硫(本题共28分)
24. B(1分)。
25. SO2+H2OH2SO3H++HSO3-(2分)
26. 不成立,实验对比说明浓度低的亚硫酸不能使品红溶液褪色,葡萄酒中的SO2含量很低,所以也不能使品红溶液褪色(2分)
27. B瓶内壁有黄色固体和小液滴生成(2分)
28. NaOH溶液倒吸到B瓶中(1分)
SO2+NaOH===NaHSO3或SO2+2NaOH===Na2SO3+H2O(1分)
29. A(2分)
30. 0.1mol/L(2分),A(2分)
31. KMnO4溶液(溴水、碘水等合理即可)(1分)
32. 1项(2分)
33. 2CuCl2+SO2+2H2O===2CuCl↓+2HCl+H2SO4(2分)
34. SO2+H2O2===H2SO4(2分)
35. 0.24g/L(2分)
36. 盐酸易挥发,挥发出的HCl消耗氢氧化钠,使消耗氢氧化钠的体积增大,测定结果偏高(2分)
37 . 用稀硫酸代替稀盐酸(2分)
四、雾霾与脱硝(本题共22分)
- A(1分)
- B(2分)
40. 由于夏季温度较高、光照强度较大,会促进SO2转化为SO,导致SO2浓度下降,SO浓度上升,SOR增大;而夏季HNO3和NH4NO3易分解,导致NO浓度下降,NO2浓度上升,NOR减小,因此SOR和NOR在夏季差异最大。(2分)
41. A (1分)
42. 秋季和冬季应该加大机动车污染整治力度或适当限制机动车的行驶或推广使用新能源汽车(2分)
43. 催化剂(2分),6NO + 4NH3 5N2 + 6H2O(2分,条件1分)
44. 气密性(2分);氨气密度较小,可使反应气体混合均匀(2分)
45. NO2(1分)
46. 尾气处理(1分)
47. 干燥气体、控制气体流速、控制各气体比例(任写1种,2分)。
48. 0.8或80%(2分)
上海市杨浦区控江中学2022-2023学年高一下学期期末考试化学试题(含解析): 这是一份上海市杨浦区控江中学2022-2023学年高一下学期期末考试化学试题(含解析),共26页。
2020-2021学年上海市控江中学高一(下)期中化学试卷: 这是一份2020-2021学年上海市控江中学高一(下)期中化学试卷,共23页。试卷主要包含了选择题,综合分析题,计算题等内容,欢迎下载使用。
2022-2023学年上海市杨浦区控江中学高三下学期3月测试化学试题含答案: 这是一份2022-2023学年上海市杨浦区控江中学高三下学期3月测试化学试题含答案,共12页。试卷主要包含了选择题,综合题等内容,欢迎下载使用。












