
- 中考化学易错点大全 试卷 试卷 0 次下载
- 2.专题二 常见气体的制备课件PPT 课件 1 次下载
- 4.专题四 物质的除杂(分离)课件PPT 课件 0 次下载
- 5.专题五 物质的推断课件PPT 课件 1 次下载
- 6.专题六 实验探究题课件PPT 课件 0 次下载
3.专题三 物质的检验、鉴别和共存课件PPT
展开类型一 物质的检验、鉴别(含无试剂鉴别)
物质的检验、鉴别既有区别又有联系。联系:它们都是根据特征反应现象判定物质。区别:检验是根据物质的特性,用物理或化学方法对物质的组成成分加以确定、证实(若待检验物质为酸、碱、盐的溶液,则对阴、阳离子都要加以鉴定);鉴别是对两种或两种以上的物质进行定性区分。
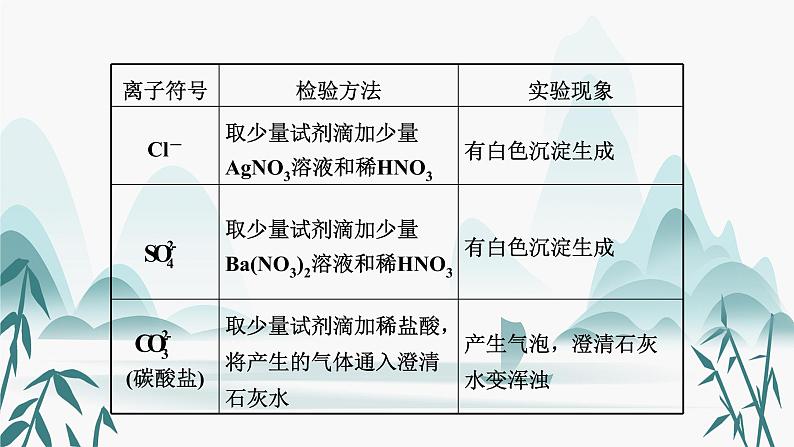
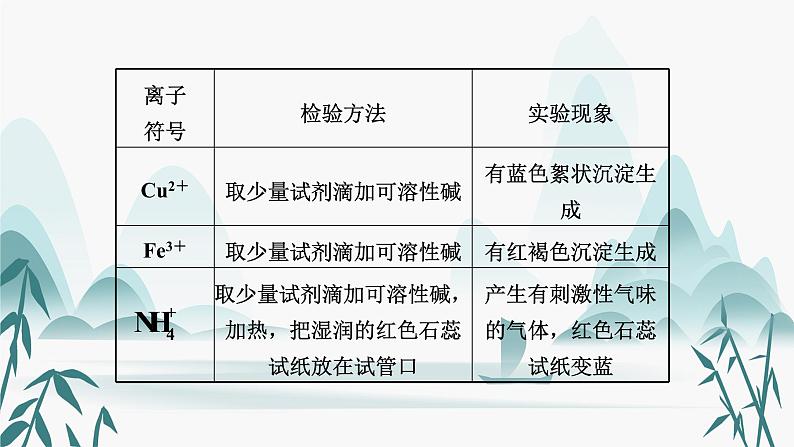
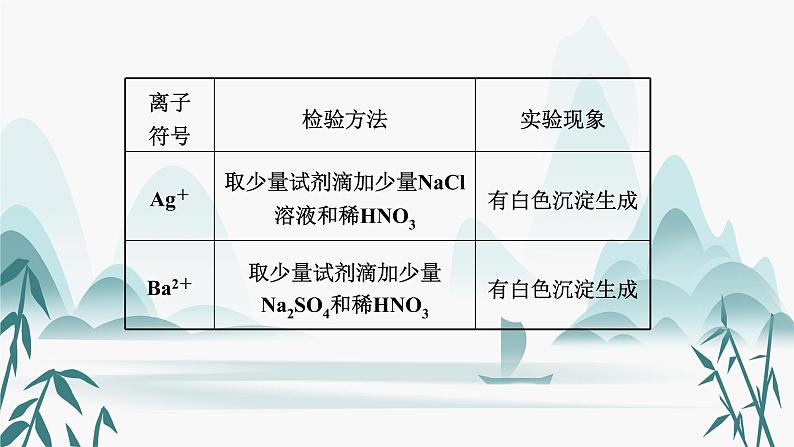
一、物质的检验(2015永州19,2014年2考)1. 常见气体的检验
二、物质的鉴别1. 物质鉴别(含无试剂鉴别)的方法(1)物理方法:依据特殊的物理性质(如颜色、气味、溶解性、溶解时的吸放热现象等)进行观察、分析、判断、得出结论。①依据颜色鉴别:含Cu2+溶液显蓝色,含Fe3+溶液显黄色,KMnO4溶液显紫红色。②依据气味鉴别:SO2、NH3均有刺激性气味。③依据溶解性鉴别:CaCO3不溶于水、Na2CO3溶于水。
④依据溶解时的吸放热现象鉴别:NaOH溶于水放热、NH4NO3溶于水吸热、NaCl溶于水无明显变化。⑤依据磁性鉴别:铁丝可以用磁铁来吸引,而铝丝不可以。(2)化学方法:分别取出少量待检验物质(一般为溶液),加入少量试剂充分反应,观察反应现象,根据现象分析、判断、得出结论。①若物质间有明显酸碱性差异,可使用酸碱指示剂和pH试纸(或pH计)来鉴别。
②鉴别一组溶液a.若溶液中有酸,可选用Na2CO3等可溶性碳酸盐来检验。b.若溶液中有碳酸盐,可用酸。c.若溶液中有Ag+,选用盐酸。d.若溶液中有Ba2+,选用硫酸
3. 鉴别的基本题型(1)无试剂鉴别:这类试题是利用待鉴别的物质之间的关系加以鉴别。①特征现象法:首先鉴别出有颜色或有气味的物质,然后再利用已经鉴别出来的物质去鉴别其他物质,以此类推,鉴别出全部物质。②两两混合法:当不存在具有特殊物理性质的物质时,将组内物质两两混合,根据与组内其他物质反应产生特殊现象鉴别出第一种物质,再利用该物质鉴别其他物质,从而将各物质一一鉴别开来。
(2)任选试剂的鉴别:一般先按照共性(气体按能否燃烧或助燃,溶液按照酸碱性等)分组,再根据各组物质的特殊性质分别鉴别。
例1 下表中各组物质的鉴别方法正确的是( )
【解析】紫色石蕊溶液遇酸变红,遇碱变蓝,向稀盐酸、碳酸钠溶液、氢氧化钠溶液中分别滴加石蕊溶液时,溶液依次为红色、蓝色和蓝色,A错误;碳酸钙和硫酸钡都不溶于水,因此不能用水鉴别,B错误;二氧化碳和氮气都不能燃烧,也不支持燃烧,氧气具有助燃性,所以将燃着的木条分别伸入气体中,无法鉴别氮气和二氧化碳,C错误;D中加入足量的稀硫酸,与铁粉反应会产生气泡,木炭粉没有明显变化,氧化铜粉末溶解,得到蓝色溶液,可以鉴别,D正确。
例 2 下列物质的溶液,不另加试剂就不能鉴别出来的一组是( )A. CuSO4 BaCl2 H2SO4B. Na2CO3 Ca(NO3)2 HClC. Na2SO4 KNO3 HClD. FeCl3 NaOH KMnO4
【解析】C中试剂均没有特征现象,而且物质间不发生反应,无法鉴别;关于A、B、D选项的分析如下
【变式练习】1. 在下列各项“家庭小实验”中,不能达到预期目的的是( )A. 品尝——鉴别白糖和食盐B. 观察——鉴别黄铜和黄金C. 闻气味——鉴别酒精和白醋D. 点燃——鉴别羊毛和涤纶
【解析】白糖具有甜味,食盐具有咸味,采用品尝的方法可以区分二者,A能达到目的;黄铜和黄金都呈黄色,采用观察外观的方法不能区分二者,B不能达到目的;酒精具有酒的香味,白醋具有酸味,采用闻气味的方法可以区分二者,C能达到目的;羊毛燃烧产生烧焦羽毛味, 涤纶燃烧产生刺激性气味,采用点燃的方法可以区分二者,D能达到目的。
2. 下列实验操作和结论的说法正确的是( )A. 取少量溶液于试管中,滴加BaCl2溶液,有白色沉淀生成,证明溶液中一定含有Ag+B. 向某固体中滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐C. 只用水就可以将NH4NO3、BaSO4、CaO、NaOH四种固体物质区别出来D. 把燃着的木条插入某瓶无色气体中,木条熄灭,证明瓶中的气体一定是二氧化碳
3. 有三瓶失去标签的无色溶液,它们可能是稀HCl、稀H2SO4、Na2CO3、NaNO3、NaCl、Ba(OH)2这六种溶液中的三种。为确定它们各为何种溶液,小明做了如下实验:(1)把它们两两混合,均无明显现象。(2)取样,往样品中分别滴加紫色石蕊溶液。有一种溶液变红色,另一种溶液不变色,剩下的一种溶液变蓝色。能使紫色石蕊溶液变蓝色的原溶液显_____(填“酸性、中性、碱性”)。
(3)综合(1)(2)步实验现象及结论,可推断出这三种溶液中的一种溶液一定是Ba(OH)2溶液,还有一种溶液一定是________;为确定剩下的另一种溶液,再取样,往其中滴加一种无色溶液,产生白色沉淀,请写出其化学方程式:______________________________________
NaCl + AgNO3 AgCl↓ + NaNO3
类型二 物质或离子的共存(了解)
1. 共存的实质物质或离子之间不能发生反应,则它们可以共存;若能发生反应,则它们不能共存。2. 共存的条件(1)组内物质均可溶。(2)在同一溶液中,物质(即所含离子)之间不发生反应,即不会生成沉淀、气体或水。
3. 初中阶段常见的不共存的离子对Cl- ——Ag+(AgCl↓) ——Ba2+(BaSO4↓)
H+(H2O+CO2↑)Ca2+(CaCO3↓)、Ba2+(BaCO3↓)
H+(H2O)Cu2+[Cu(OH)2↓]、Fe3+[Fe(OH)3↓]、Mg2+[Mg(OH)2↓] (NH3↑+H2O)
【特别提醒】判断离子共存时,需注意溶液为电中性(不显电性),即在同一组物质的离子中,既含阳离子也含阴离子。
4. 解密物质共存中的隐含条件(1)pH<7或酸性溶液,则溶液一定存在H+,且该溶液中没有能与H+反应的物质(或离子)。常见的描述有:酸性溶液、pH=2(pH<7)的溶液、能使紫色石蕊溶液呈红色的溶液、加入活泼金属能放出氢气的溶液、加入碳酸盐或碳酸氢盐能放出气体的溶液等。(2)pH>7或碱性溶液,则溶液一定存在OH-,且该溶液中没有能与OH-反应的物质(或离子)。常见的描述有:碱性溶液、pH=11(pH>7)的溶液、使无色酚酞溶液呈红色的溶液、使紫色石蕊溶液呈蓝色的溶液等。
(3)溶液为无色透明,则溶液一定不存在有色离子如Cu2+、Fe2+、Fe3+、 、 等。溶液也不能形成浑浊或沉淀,即所给混合物中能发生反应,生成沉淀的离子不能共存。
【解析】强酸性溶液中含有氢离子、强碱性溶液中含有氢氧根离子。铜离子不能与氢氧根离子共存,A错误;镁离子不能与氢氧根离子共存,B错误;碳酸根离子不能与氢离子共存,C错误;钠离子、钡离子、氯离子、硝酸根离子间不反应,且能在强酸性或强碱性溶液中共存,D正确。
【变式练习 】1. 某溶液中大量存在的离子仅有 、Ba2+和X离子,则X是( ) A. OH- B. Cl- C. K+ D.
【解析】铵根离子和钡离子均属于阳离子,根据溶液中电荷守恒,所以X离子一定是阴离子,C错误;铵根离子与氢氧根离子会结合生成氨气,不能大量共存,A错误;氯离子与铵根离子、钡离子均不会结合生成沉淀、气体或水,氯离子可与铵根离子和钡离子大量共存,B正确;钡离子会与硫酸根离子结合生成硫酸钡沉淀,D错误。
2. 下列各组离子在指定的溶液中能大量共存的一组是( )A.在硝酸铵溶液中:Na+、Cu2+、OH-B.在稀盐酸中:Ba2+、 、Zn2+C.在氯化钠溶液中:K+、Ca2+、 D.在氢氧化钠溶液中:H+、Mg2+、Cl-
2023年中考化学复习---物质的检验与鉴别、除杂和共存课件PPT: 这是一份2023年中考化学复习---物质的检验与鉴别、除杂和共存课件PPT,共28页。PPT课件主要包含了酸溶液,OH-,碱溶液,Cl-,SO42-,两两反应,常见物质的除杂,NaOH溶液等内容,欢迎下载使用。
2023年中考二轮复习探究二 物质的检验与鉴别、分离与除杂、共存课件PPT: 这是一份2023年中考二轮复习探究二 物质的检验与鉴别、分离与除杂、共存课件PPT,共40页。PPT课件主要包含了②常见离子的检验,蓝色絮状沉淀,变浑浊,常见物质的鉴别,常见气体除杂举例,氢氧化钠,浓硫酸,稀硫酸等内容,欢迎下载使用。
初三九年级化学下册复习资料二部分重点专题突破专题三物质的检验鉴别和共存课件: 这是一份初三九年级化学下册复习资料二部分重点专题突破专题三物质的检验鉴别和共存课件,共39页。












