

江苏省泰州市2020-2022三年中考化学真题知识点分类汇编-06酸和碱、中和反应
展开一、单选题
1.(2021·江苏泰州·统考中考真题)下列说法正确的是
A.含有氧元素的物质一定是氧化物
B.只含一种元素的物质一定是单质
C.质子数相同的原子一定属于同种元素
D.能与稀盐酸反应产生气泡的物质一定是活泼金属
2.(2021·江苏泰州·统考中考真题)下列对实验现象的描述错误的是
A.浓硫酸滴到纸张上,纸张逐渐变黑
B.红磷在空气中燃烧,产生大量白烟
C.一氧化碳还原氧化铁,黑色固体变为红色固体
D.氯化铵和氢氧化钙混合加热,产生能使湿润的红色石蕊试纸变蓝的气体
3.(2022·江苏泰州·统考中考真题)下列有关溶液的说法正确的是
A.碘酒溶液中,酒精为溶质B.向水中加入蔗糖,导电性明显增强
C.氢氧化钙的溶解度随温度升高而增大D.积雪的路而撒食盐、可以促进积雪融化
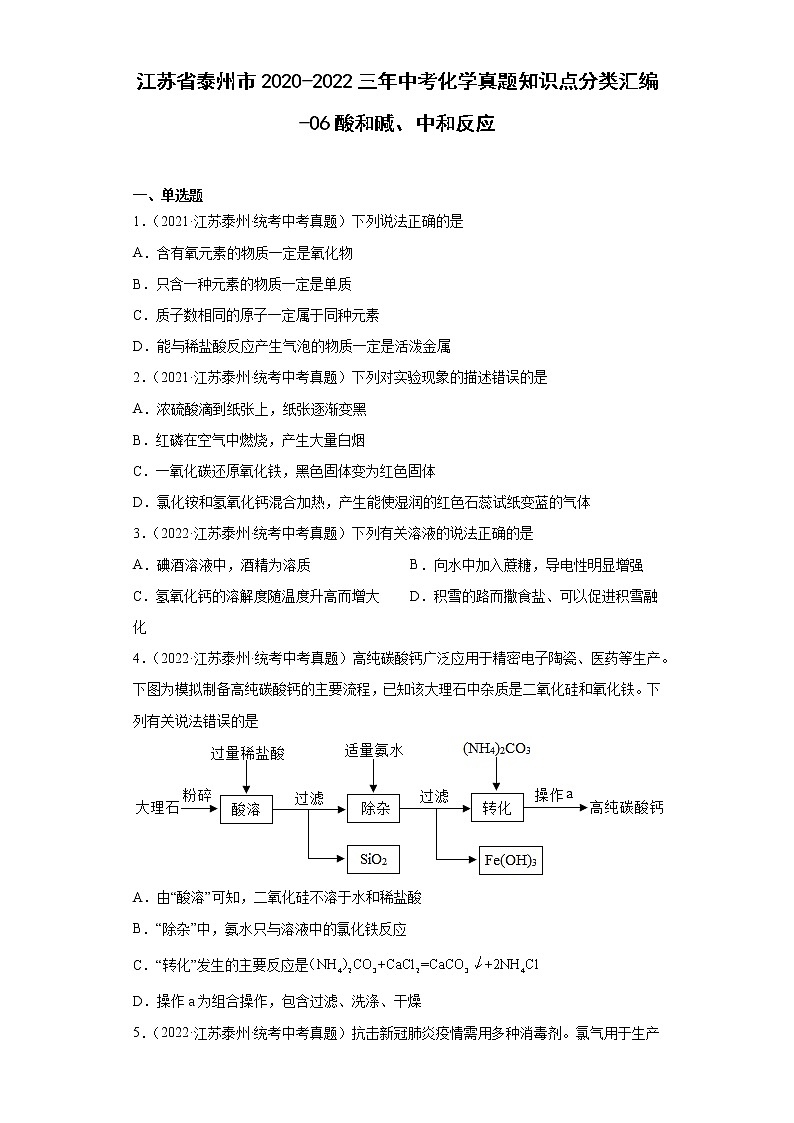
4.(2022·江苏泰州·统考中考真题)高纯碳酸钙广泛应用于精密电子陶瓷、医药等生产。下图为模拟制备高纯碳酸钙的主要流程,已知该大理石中杂质是二氧化硅和氧化铁。下列有关说法错误的是
A.由“酸溶”可知,二氧化硅不溶于水和稀盐酸
B.“除杂”中,氨水只与溶液中的氯化铁反应
C.“转化”发生的主要反应是
D.操作a为组合操作,包含过滤、洗涤、干燥
5.(2022·江苏泰州·统考中考真题)抗击新冠肺炎疫情需用多种消毒剂。氯气用于生产含氯消毒剂,氯气与水反应的微观示意图如下。下列说法正确的是
A.该反应前后元素化合价均没有变化B.反应物和生成物中共有两种氧化物
C.参加反应的甲、乙质量比为71:18D.丙物质的水溶液能使红色石蕊试纸变蓝
6.(2022·江苏泰州·统考中考真题)硫酸是重要的化工原料。下列有关硫酸的说法错误的是
A.浓硫酸具有吸水性B.稀硫酸能与纯碱反应
C.浓硫酸稀释后温度降低D.稀硫酸可用于金属表面除锈
7.(2022·江苏泰州·统考中考真题)推理和归纳是化学学习常用的思维方法。下列推理确的是
A.燃烧都有发光发热现象,则有发光发热现象的变化一定是燃烧
B.置换反应都有单质生成,则有单质生成的反应一定是置换反应
C.中和反应有盐和水生成,则有盐和水生成的反应一定是中和反应
D.单质是由一种元素组成的纯净物,则一种元素组成的纯净物一定是单质
二、多选题
8.(2022·江苏泰州·统考中考真题)下列实验操作能够达到实验目的的是
A.AB.BC.CD.D
三、推断题
9.(2020·江苏泰州·统考中考真题)A~F是初中化学常见物质。A是生命之源,是人体中含量最多的物质;B与A发生化合反应生成C,C俗称熟石灰;D是由三种非金属元素组成的盐,D和A混合,溶液温度显著降低,据此原理可制作“摇摇冰”;C与D混合加热反应生成A、E、F三种物质,E为有刺激性气味的气体。请回答下列问题:
(1)A的化学式为________;电解A的实验,正、负极产生的气体体积比为________。
(2)B俗称_________,B与A反应的化学方程式为__________。
(3)C的澄清溶液通常用来检验__________气体。
(4)D在农业上可用作________________肥。
(5)E能使湿润的红色石蕊试纸变______________色。
(6)C与D混合加热反应的化学方程式为________。
10.(2021·江苏泰州·统考中考真题)A~J是初中化学常见的物质,相互之间能发生下列反应:①A+B→C+D ②D+E→B ③C+F→G+H ④B+F→G+I ⑤H+JA其中A是一种黑色固体,C溶液是蓝色,F、H、I、J为单质,通常状况下I、J为气体,反应②是形成硫酸型酸雨的某一步反应,E的分子中两种原子的个数比为1:3,反应③是湿法冶金的先驱。请回答下列问题:
(1)E的化学式为______;反应④除生成气体处,还有的现象是______;F在使用时易与空气中_______等物质作用生成一种疏松多孔的物质,造成资源损失。
(2)写出反应的化学方程式;反应③_______;反应⑤_______。①~⑤五个反应中,属于置换反应的是______(填序号)。
(3)将过量F加入C溶液中充分反应,反应后与反应前相比,溶液质量______(填“增大”“减小”或“不变”),过滤后所得固体的成分为______。
(4)I在J中燃烧的化学方程式为______,I作为能源,其优势为______(答一点)。
11.(2022·江苏泰州·统考中考真题)A~H是初中化学常见物质,A和B为组成元素相同的两种气体,B可以产生温室效应,C为一种红棕色固体,C能与A在高温条件下反应生产B和金属单质D,E和F为组成元素相同的两种液体,G的稀溶液可使石蕊试液变红,且能和氯化钡溶液反应产生不溶于稀硝酸的白色沉淀,G的稀溶液能与C反应生成F和H。请回答以下问题。
(1)B的化学式为_____,G溶液中的阳离子符号为_____。
(2)E在C的催化作用下生成F的化学方程式为___,该反应属于_____(填基本反应类型)。
(3)向盛有足量G的稀溶液的烧杯中加入少量C,实验现象为_____。
(4)物质X在氧气中完全燃烧生成B和F,则物质X中一定含有的元素有____(填元素符号)。经测定X的相对分子质量为30,且每个分子中原子总数小于10,推测X的化学式可能有_____。
四、科学探究题
12.(2020·江苏泰州·统考中考真题)酸碱中和反应是初中阶段重要的一类反应,请你一起参与探究。
【实验探究Ⅰ】在50mL一定浓度的氢氧化钠溶液中滴加50mL一定浓度的盐酸,并用玻璃棒搅拌,观察到溶液的温度______,由此现象小李同学得出两者能发生反应的结论。通过查阅相关资料后,小张同学发现此结论不够严谨,设计了下列3个对比实验:
①50mL一定浓度的盐酸与50mL蒸馏水混合,测量溶液温度的变化。
②50mL一定浓度的氢氧化钠溶液与50mL蒸馏水混合,测量溶液温度的变化。
③50mL一定浓度的盐酸与50mL一定浓度的氢氧化钠溶液混合,测量溶液温度的变化。
用数字化实验技术测得3个实验,溶液温度随时间变化的关系如图所示。
(1)由图可知,盐酸、氢氧化钠溶液稀释时均________(填“放热”或“吸热”),但它们稀释时温度的变化量远________两溶液混合时温度的变化量。
(2)从微观角度分析,此中和反应的温度变化主要是由于________(填离子符号)两种离子发生反应放出热量的缘故。
【实验探究Ⅱ】
(1)在50mL一定浓度的氢氧化钠溶液中滴加2~3滴酚酞试液,再逐滴加入一定浓度的盐酸,并用玻璃棒搅拌,溶液颜色由红色刚好变为无色时,可说明两者发生了反应。该反应的化学方程式为________。
(3)取一定量反应后的无色溶液加热蒸发,在蒸发的过程中,“意外”发现溶液由无色又变成红色。同学们对红色溶液中溶质的成分(酚酞除外)进行再探究。
查阅资料:酚酞在pH<8.2的溶液中呈无色,在8.2
猜想二:NaCl、NaOH
猜想三:NaCl、NaOH和Na2CO3
同学们讨论后一致认为猜想__________是错误的,理由是___________。
实验验证:取样,滴加_______,无气泡产生,猜想三错误。
原因分析:反应后无色溶液中仍存在少量NaOH,加热蒸发,当溶液的pH在_______范围内,溶液的颜色变红。
总结反思:向某碱性溶液中滴加2~3滴无色酚酞试液,振荡后溶液的颜色_____(填“一定”或“不一定”)变红。
13.(2021·江苏泰州·统考中考真题)碳酸钙是初中阶段化学学习中的常见物质,某化学兴趣小组围绕此物质展开探究。
相关信息:一定体积的溶液中,离子数目越多,其离子浓度越大;电导率传感器用于测定溶液的导电性强弱,在其他条件相同下,溶液中离子浓度越大;溶液的电导率越大。
【实验探究Ⅰ】将碳酸钙粉末在酒精喷灯上灼烧一段时间,再将灼烧后的固体物质投入盛水的烧杯中,滴加2滴酚酞试液,酚酞试液变红。对此现象分析,得出结论。
(1)碳酸钙高温发生了分解,反应的化学方程式为______。
(2)分解后固体产物与水反应的化学方程式为______,此反应生成物能使酚酞试液变红,是因为在水溶液中产生______离子(填离子符号)。
小组经过讨论,对酚酞试液变红是否存在其他因素产生了疑问,进行下列实验。
【实验探究Ⅱ】在试管中加入少量碳酸钙粉末,加入2mL水,振荡摇匀,制成碳酸钙悬浊液,滴加2滴酚酞试液,酚酞试液变红。
(1)酚酞试液变红证明碳酸钙悬浊液显______性。
(2)在相同实验条件下,用电导率传感器测得水的电导率为8.5,碳酸钙悬浊液电导率为74.与水比较,碳酸钙悬浊液中离子浓度较______(填“大”或“小”),证明在碳酸钙悬浊液中有部分碳酸钙溶于水,形成碳酸钙的______(填“饱和”或“不饱和”)溶液。
(3)小组继续探究碳酸钙悬浊液使酚酞试液变红的微观原因,做了下面的对照实验:用pH传感器分别测得在常温下五种混合体系的pH,如下表所示。
从上表可知,“盐溶液一定显中性”的说法是______(填“正确”或“错误”)的。
结合①②③④的数据分析可知,Na2CO3溶液使酚酞试液变红与碳酸钠组成中______离子(填离子符号)有关。查阅资料可知碳酸钠能与水发生一定程度的反应生成一种钠盐和另一种化合物,试写出此反应两种生成物的化学式:_______。结合⑤的数据分析。碳酸钙悬浊液使酚酞试液变色原因与碳酸钠溶液使酚酞试液变色原因本质上是一致的。
【拓展延伸】进一步探究,将碳酸钙悬浊液滴加酚酞试液加热,红色会变浅,经测定pH减小。联系所学知识,对此现象产生的原因猜测合理的是______(填字母)。
A.碳酸钙的溶解度随着温度的升高而降低
B.温度升高增大了某离子与水作用的速率,碱性增强
C.加热时部分碳酸钙发生了分解反应
14.(2022·江苏泰州·统考中考真题)某化学兴趣小组时学对家中“管道疏通剂”进行下列探究:
“管道疏通剂”包装袋上相关信息如图。
查阅资料:铝和氢氧化钠固体遇水反应放出大量的热,能加快氢氧化钠对毛发等淤积物的腐蚀,同时产生的气体能增加管道内的气压,利于疏通。该反应的化学方程式为:。(注:NaA1O2名称为偏铝酸钠,溶液显碱性,)
(1)该疏通剂与水反应产生的___在空气中遇到明火可能会引起爆炸。该疏通剂需密封保存的原因是成分中的___(填化学式)会与空气中有关物质发生反应,其中发生化合反应的化学方程式为___。
(2)小华使用该疏通剂疏通某塑料软管时发现软管变形,原因可能是_____(写出一个即可),
活动二:探究成分作用
(3)小夏取少量该疏通剂加入适量水,充分反应后,无固体残留,说明疏通剂中____一定已完全反应。取少量反应后溶液,向其中滴入1滴酚酞试液,可观察到溶液呈____色。
(4)该疏通剂中含有硝酸钠,硝酸钠中氮元素的化合价为____。硝酸钠与氢氧化钠和铝粉均不反应,同学们对于疏通剂中硝酸钠的作用感到好奇。通过科学方法检验、该疏通剂与水反应前后硝酸钠的质量和化学性质均没有改变。由此,小夏猜测:硝酸钠可能是铝粉和氢氧化钠溶液反应的催化剂。为判断该猜测是否正确,请你设计一个实验方案:____。(实验方案包括操作、现象和结论。可选用的试剂有:铝粉、氢氧化钠溶液,硝酸钠粉末)
活动三:开展定量分析
(5)小文设计了图1装置测定该疏通剂样品中铝粉的质量分数。将300mg固体样品和足量水分别放在Y形管两侧,倾斜Y形管,将水倒入左侧:充分反应后,冷却到室温,利用量气管和水准管测定反应生成的氢气体积为100mL。已知该条件下氢气密度为0.09mg/mL。请计算样品中铝粉的质量分数。(写出计算过程)____。
(6)小明设计了不同的实验方案,装置如图2,精确称量了该装置在反应前后的质量,将其质量差作为生成氢气的质量,由此计算出样品中铝粉的质量分数。小明和小文测定过程均操作规范,小明测定的样品中铝粉的质量分数却比小文大,原因可能是_____。
选项
实验目的
实验操作
A
鉴别羊毛线和棉线
取样,灼烧,闻气味
B
除去粗盐中的难溶性杂质
溶解,蒸发结晶
C
测定柠檬汁的pH
取样,滴在湿润的pH试纸上,对照
D
检验某化肥是否为铵态氮肥
取样,加入熟石灰,研磨,闻气味
混合体系
①Na2CO3溶液
②NaCl溶液
③CaCl2溶液
④K2CO3溶液
⑤CaCO3悬浊液
pH
11.6
7.0
7.0
11.6
10.1
参考答案:
1.C
【详解】A.氧化物含有氧元素,但含氧元素的化合物不一定都是氧化物,如C2H5OH,选项A错误。
B.单质是由同种元素组成的纯净物,单质是由同种元素组成的,只含一种元素的物质不一定是单质,也可能是混合物,如氧气和臭氧的混合物、金刚石和石墨的混合物等,选项B错误。
C.元素是质子数(即核电荷数)相同的一类原子的总称,质子数相同的原子一定属于同种元素,选项C正确。
D.能与稀盐酸反应产生气泡的物质不一定是活泼金属,也可能是碳酸盐等,选项D错误。
故选:C。
2.C
【详解】A.浓硫酸具有脱水性,能将纸张中的氢、氧元素按照水中质量比例脱去,使纸张逐渐变黑,选项A正确;
B.红磷在空气中点燃和空气中氧气反应,产生大量的白烟,选项B正确;
C.红色的氧化铁固体在高温下被一氧化碳还原成黑色的铁粉,选项C错误;
D.氯化铵属于铵态物质,与碱性物质氢氧化钙混合,会产生氨气,氨气能使湿润的红色石蕊试纸变成蓝色,选项D正确;
故选:C。
3.D
【详解】A、碘酒溶液中,酒精为溶剂,碘是溶质,故A错误;
B、蔗糖不能解离出自由移动的离子,溶于水中不会增加溶液的离子浓度,所以不会增强溶液的导电性,故B错误;
C、氢氧化钙的溶解度随温度升高而减小,故C错误;
D、固体物质溶于水,所得溶液的沸点比纯水高,凝固点比纯水低;在积雪上撒盐,盐溶于水时形成的盐溶液的凝固点比水的凝固点低,从而使冰雪在较低的温度下也能融化,故D正确。
故选D。
4.B
【详解】A、稀盐酸中既有盐酸又有水,“酸溶”后过滤得到二氧化硅,所以二氧化硅不溶于水和稀盐酸。A正确。
B、据图可知,“除杂”中,氨水既与溶液中的氯化铁反应,又与过量的稀盐酸反应。B错。
C、据图可知,“转化”发生的主要反应是碳酸铵与氯化钙反应生成碳酸钙沉淀和氯化铵,化学方程式。C正确。
D、操作a先过滤,再洗涤洗去碳酸钙表面的氯化铵,然后干燥,得到高纯碳酸钙。D正确。
综上所述:选择B。
5.C
【分析】根据微观示意图,反应的方程式是:。
【详解】A、根据氯气与水反应的微观示意图,甲是单质氯气,反应后产生了氯化氢和HClO,氯元素由游离态变成了化合态,则一定有化合价的改变;错误;
B、氧化物是由两种元素组成的,且一种元素是氧元素的化合物;该反应中只有水一种氧化物;错误;
C、根据方程式,参加反应的甲(氯气)、乙(水)质量比为=(35.5×2):(1×2+16)=71:18,正确;
D、根据反应的微观示意图,丙是盐酸,盐酸能使紫色石蕊试纸变红;错误;
故选C。
6.C
【详解】A、浓硫酸具有吸水性,能作干燥剂,故说法正确;
B、纯碱是碳酸钠的俗称,碳酸钠溶液呈碱性,碳酸钠与稀硫酸反应生成硫酸钠、水和二氧化碳,故说法正确;
C、浓硫酸稀释放热,使溶液温度升高,故说法错误;
D、金属表面的锈主要是金属氧化物,稀硫酸能与金属氧化物反应生成盐和水,可用于金属表面除锈,故说法正确;
故选C。
7.D
【详解】A、燃烧通常是指可燃物与氧气发生的发光、放热的剧烈的氧化反应;有发光、发热现象的变化不一定是燃烧,例如灯泡放光放热属于物理变化;错误;
B、由一种单质与一种化合物反应,生成另一种单质与另一种化合物的反应是置换反应,置换反应有单质生成,但有单质生成的反应不一定为置换反应,如;错误;
C、中和反应是酸和碱作用生成盐和水的反应,中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如;错误;
D、由单质的定义可知,单质是由同一种元素组成的纯净物,则由一种元素组成的纯净物一定是单质;正确;
故选D。
8.AD
【详解】A、羊毛线的主要成分是蛋白质,灼烧时产生烧焦羽毛的气味;棉线的主要成分是植物纤维,灼烧时,产生烧纸的气味,可以鉴别;正确;
B、粗盐经过溶解、过滤、洗涤、蒸发结晶,得到氯化钠;错误;
C、用pH试纸测定溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,把试纸显示的颜色与标准比色卡对比来确定pH。不能用水湿润pH试纸,会稀释待测溶液,使溶液的酸性减弱,测定结果偏大;错误;
D、铵态氮肥中的铵根能和氢氧化钙反应生成盐、水和氨气,氨气有刺激性气味;正确。
故选AD。
9. H2O 1:2 生石灰 二氧化碳(或 CO2) 氮 蓝
【详解】(1)A~F是初中化学常见物质。A是生命之源,是人体中含量最多的物质;A的化学式为 H2O;电解A的实验,正、负极产生的气体体积比为1:2;
(2)B与A发生化合反应生成C,C俗称熟石灰;B是氧化钙,俗称 生石灰 ,B与A反应的化学方程式为CaO+ H2O= Ca(OH)2;
(3)二氧化碳能和氢氧化钙反应生成碳酸钙沉淀和水,氢氧化钙的澄清溶液通常用来检验二氧化碳气体;
(4)D是由三种非金属元素组成的盐,D和A混合,溶液温度显著降低,据此原理可制作“摇摇冰”,可知D是硝酸铵,在农业上可用作氮肥;
(5)C与D混合加热反应生成A、E、F三种物质,E为有刺激性气味的气体,可知E为氨气,氨气溶于水形成氨水,E能使湿润的红色石蕊试纸变蓝色;
(6)氢氧化钙与硝酸铵混合加热反应生成硝酸钙、氨气、水,化学方程式为。
10.(1) SO3 溶液由无色变成浅绿色 氧气和水
(2) CuSO4+Fe=FeSO4+Cu 2Cu+O22CuO ③④
(3) 减小 铁、铜
(4) 2H2+O22H2O 燃烧热值高,无污染
【分析】A~J是初中化学常见的物质,反应②是形成硫酸型酸雨的某一步反应,E的分子中两种原子的个数比为1:3,所以E是三氧化硫,D是水,B是硫酸,A是一种黑色固体,C溶液是蓝色,所以A是氧化铜,C是硫酸铜,反应③是湿法冶金的先驱,所以F是铁,G是硫酸亚铁,H是铜,硫酸和铁反应生成硫酸亚铁和氢气,所以I是氢气,铜和氧气在加热的条件下生成氧化铜,所以J是氧气,经过验证,推断正确。
(1)
由分析可知,E的化学式为SO3;反应④是硫酸和铁反应生成硫酸亚铁和氢气,除生成气体处,还有的现象是:溶液由无色变成浅绿色;F在使用时易与空气中氧气和水等物质作用生成一种疏松多孔的物质,造成资源损失,故填:SO3;溶液由无色变成浅绿色;氧气和水。
(2)
由分析可知,反应①氧化铜和硫酸生成硫酸铜和水;反应②三氧化硫和水生成硫酸;反应③是湿法冶金的先驱,铁和硫酸铜生成硫酸亚铁和铜;反应④硫酸和铁反应生成硫酸亚铁和氢气;反应⑤铜和氧气生成氧化铜,③④是单质和化合物生成单质和化合物,属于置换反应,故填:CuSO4+Fe=FeSO4+Cu;2Cu+O22CuO;③④。
(3)
将过量F加入C溶液中充分反应,铁和硫酸铜生成硫酸亚铁和铜,反应后与反应前相比 ,溶液质量减小,过滤后所得固体的成分为铜和铁,故填:减小;铁、铜。
(4)
氢气在氧气中燃烧生成水,氢气优势燃烧热值高,无污染,故填:2H2+O22H2O;燃烧热值高,无污染。
11.(1) CO2 H+
(2)
分解反应
(3)固体消失,溶液变黄
(4) C、H C2H6、CH2O
【分析】B可以产生温室效应,则B是二氧化碳;A和B为组成元素相同的两种气体,则A是CO;C为一种红棕色固体,C能与A(CO)在高温条件下反应生产B(CO2)和金属单质D,则C是氧化铁,D是铁;G的稀溶液可使石蕊试液变红,且能和氯化钡溶液反应产生不溶于稀硝酸的白色沉淀,则G是硫酸;G的稀溶液能与C反应生成F和H,E和F为组成元素相同的两种液体,则F是水,E是过氧化氢,H是硫酸铁;代入验证,推理正确。
【详解】(1)根据分析,B是CO2;G是稀硫酸,阳离子是;H+;
(2)E是过氧化氢,在C氧化铁的催化作用下产生水和氧气,方程式是:;该反应是一种物质反应产生两种物质的分解反应;
(3)G是稀硫酸加入少量C氧化铁,两者反应产生硫酸铁(溶液中是黄色的)和水,现象是固体消失,溶液变成黄色;
(4)B是二氧化碳,F是水,物质X在氧气中完全燃烧生成二氧化碳和水,根据质量守恒定律,则物质X中一定含有的元素有C、H,可能有氧元素;
当不含有O时,设X的化学式是CaHb,则12a+b=30,
当a=1时,b=18,因为每个分子中原子总数小于10,不合理;
当a=2时,b=6,因为每个分子中原子总数小于10,则X的化学式是C2H6;
当a=3及以上时,相对分子质量超过30;不合理;
当含有O时,设X的化学式是CaHbOc,则12a+b+16c=30,则只有a=c=1,b=2合理,即化学式是:CH2O。
12. 升高 放热 小于 H+、OH- 三 反应物中不含碳元素 足量稀盐酸 8.2~14 不一定
【详解】[实验探究Ⅰ]在50mL一定浓度的氢氧化钠溶液中滴加50mL一定浓度的盐酸,并用玻璃棒搅拌,因中和反应放热,可观察到溶液的温度升高;
(1)由图可知,实验①、实验②中,溶液在稀释过程中温度都有上升,故盐酸、氢氧化钠溶液稀释时均放热,结合实验③曲线,可以发现盐酸、氢氧化钠溶液稀释时温度的变化量远低于两溶液混合时温度的变化量;
(2)从微观角度分析,此中和反应的温度变化主要是由于氢离子和氢氧根离子两种离子发生反应生成水分子放出热量的缘故,氢离子和氢氧根离子的离子符号分别是:H+、OH-。
[实验探究Ⅱ]
(1)在50mL一定浓度的氢氧化钠溶液中滴加2~3滴酚酞试液,再逐滴加入一定浓度的盐酸,并用玻璃棒搅拌,溶液颜色由红色刚好变为无色时,可说明两者发生了反应。氢氧化钠和盐酸反应生成氯化钠和水,该反应的化学方程式为:;
(3)根据质量守恒定律可知,反应前后元素种类不变,因此猜想三是错误的,理由是反应物中没有碳元素;
实验验证:取样,滴加足量的稀盐酸,无气泡产生,猜想三错误,因为碳酸钠能和盐酸反应生成二氧化碳气体,产生气泡;(本题中用足量的稀硫酸、稀硝酸均可)
原因分析:由资料可知,酚酞在pH<8.2的溶液中呈无色,在8.2
13.
OH﹣ 碱 大 饱和 错误 NaHCO3、NaOH A
【详解】[实验探究I]
(1)碳酸钙高温分解生成氧化钙和二氧化碳,反应的化学方程式为:,故填:。
(2)氧化钙与水反应生成氢氧化钙,反应的化学方程式为;氢氧化钙在水中解离出OH﹣,该离子能使酚酞变红。故填:;OH-。
[实验探究Ⅱ]
(1)酚酞遇碱性溶液变红,酚酞试液变红,说明碳酸钙的悬浊液呈碱性,故填:碱。
(2)电导率越大说明离子浓度越大,碳酸钙悬浊液电导率大于水,所以离子浓度也比水大;因为是碳酸钙悬浊液,有没有溶解完的固体碳酸钙,故为碳酸钙的饱和溶液,故填:大;饱和。
(3)从表格中可以看出盐的溶液不一定都显中性,有的还显碱性,如碳酸钠、碳酸钾;①②对比说明钠离子不能使酚酞变红,①④对比说明是使酚酞变红;碳酸钠能与水发生一定程度的反应生成一种钠盐和另一种化合物,生成物为NaHCO3、NaOH。故填:错误;;NaHCO3、NaOH。
[拓展延伸]
A.碳酸钙的溶解度随温度升高而降低,溶液中碳酸钙变少,碱性减弱,酚酞红色变浅,选项A正确;
B.温度升高增大了某离子与水作用的速率,碱性增强,酚酞红色变深,选项B错误;
C.加热时部分碳酸钙分解生成氧化钙,氧化钙与水生成氢氧化钙,碱性增强,酚酞红色变深,选项C错误。
故选A。
14. 氢气 NaOH、Al 铝和氢氧化钠固体遇水反应放出大量的热,使塑料软管变形 铝 红 +5 操作:取两支相同的试管甲和乙,分别装入等量的铝粉,乙试管还要加入适量硝酸钠粉末,然后,同时加入等量足量的氢氧化钠溶液;
现象:观察到乙试管产生气泡的速率比甲试管快;
结论:硝酸钠能加快铝和氢氧化钠的反应;(合理即可) 设样品中铝粉的质量分数为x。
答:样品中铝粉的质量分数是27%。 铝和氢氧化钠固体遇水反应放出大量的热,使水分蒸发跑出装置,装置的质量差除了氢气、还有水蒸气,所以结果偏大
【详解】(1)根据题目信息,该疏通剂与水反应产生氢气,氢气可燃,氢气和空气混合遇到明火可能爆炸;该疏通剂中含有铝、氢氧化钠,NaOH和空气中的二氧化碳反应产生碳酸钠、水;Al和空气中的氧气反应产生氧化铝,该反应是两种物质反应产生一种物质的化合反应,反应的化学方程式为;所以要密封保存;
(2)塑料软管变形,原因可能是铝和氢氧化钠固体遇水反应放出大量的热,使塑料管变形 (合理即可);
(3)疏通剂中硝酸钠溶于水,氢氧化钠溶于水,铝不溶于水;氢氧化钠和铝反应产生的偏铝酸钠也溶于水,充分反应后,无固体残留,说明铝一定已完全反应;反应后溶液含有偏铝酸钠,其溶液显碱性,碱性溶液使酚酞试液变红;
(4)硝酸钠中,钠是+1价,氧是-2价,设氮的化合价是x,则:(+1)+x+(-2)×3=0,x=+5;
通过科学方法检验、该疏通剂与水反应前后硝酸钠的质量和化学性质均没有改变;所以只要证明硝酸钠能改变铝粉和氢氧化钠溶液反应的速率,即可证明硝酸钠可能是铝粉和氢氧化钠溶液反应的催化剂,因为催化剂能改变其他物质的反应速率,而本身的质量和化学性质均没有改变;则设计实验:
操作:取两支相同的试管甲和乙,分别装入等量的铝粉,乙试管还要加入适量硝酸钠粉末,然后,同时加入等量足量的氢氧化钠溶液;
现象:观察到乙试管产生气泡的速率比甲试管快;
结论:硝酸钠能加快铝和氢氧化钠的反应;(合理即可);
(5)见答案。
(6)小明的实验方案是利用差量法,测定氢气的质量;但是铝和氢氧化钠固体遇水反应放出大量的热,此时水分蒸发跑出装置,则反应前后装置的质量差除了氢气、还有水蒸气,得出的氢气的质量偏大,所以结果偏大。
云南2020-2022三年中考化学真题知识点分类汇编-05酸和碱、中和反应: 这是一份云南2020-2022三年中考化学真题知识点分类汇编-05酸和碱、中和反应,共19页。试卷主要包含了单选题,填空题,实验题,流程题,计算题等内容,欢迎下载使用。
西藏2020-2022三年中考化学真题知识点分类汇编-05酸和碱、中和反应: 这是一份西藏2020-2022三年中考化学真题知识点分类汇编-05酸和碱、中和反应,共13页。试卷主要包含了单选题,填空题,科学探究题,推断题等内容,欢迎下载使用。
天津2020-2022三年中考化学真题知识点分类汇编-05酸和碱、中和反应: 这是一份天津2020-2022三年中考化学真题知识点分类汇编-05酸和碱、中和反应,共12页。试卷主要包含了多选题,单选题,填空题,推断题等内容,欢迎下载使用。