


2023高考化学总复习微专题大素养化学平衡原理中的图像分析题13课件
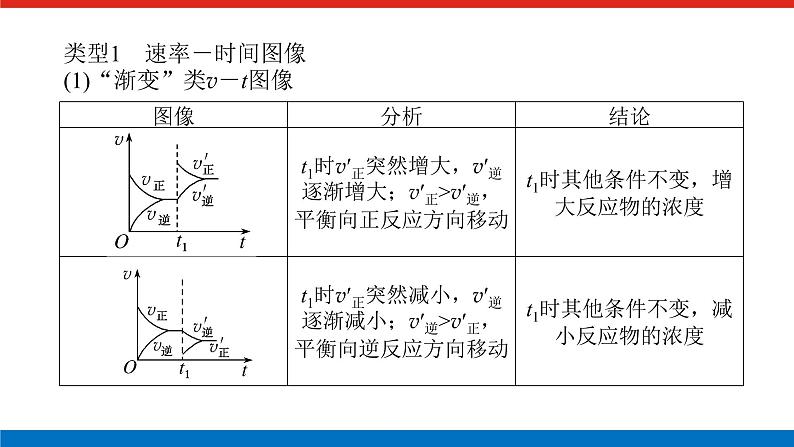
展开类型1 速率-时间图像(1)“渐变”类v-t图像
(2)“断点”类v-t图像①速率-时间图像“断点”分析 当可逆反应达到平衡后,若某一时刻外界条件发生改变,都可能使速率—时间图像的曲线出现不连续的情况,即出现“断点”。根据“断点”前后的速率大小,即可对外界条件的变化情况作出判断。如图,t1时刻改变的条件可能是使用了催化剂或增大压强(仅适用于反应前后气体物质的量不变的反应)。
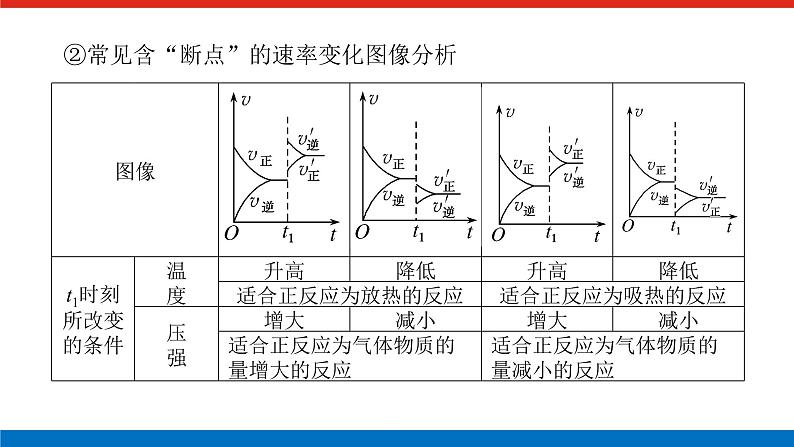
②常见含“断点”的速率变化图像分析
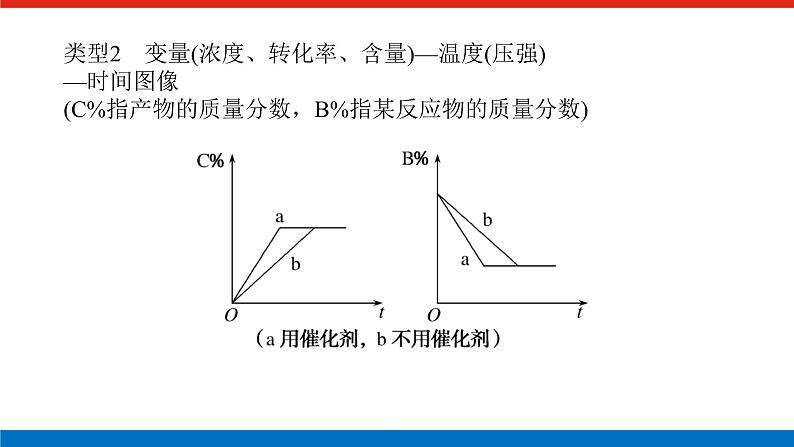
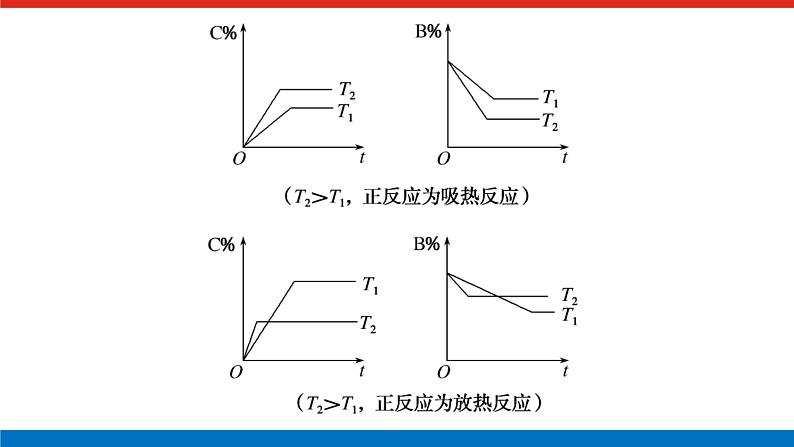
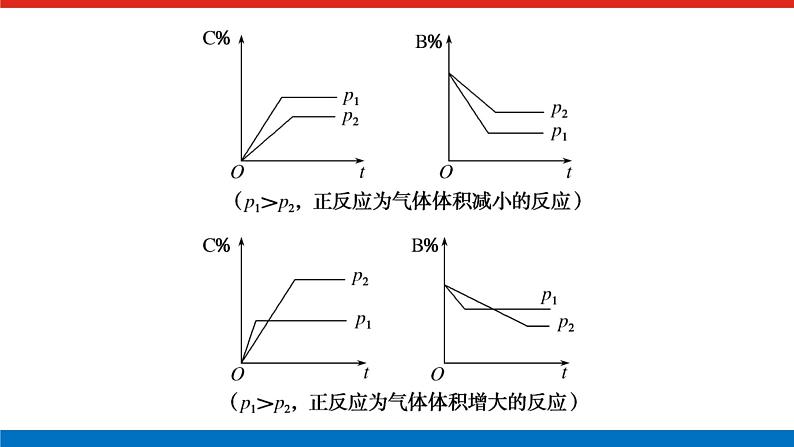
类型2 变量(浓度、转化率、含量)—温度(压强)—时间图像(C%指产物的质量分数,B%指某反应物的质量分数)
类型3 恒压(或恒温)线(α表示反应物的转化率,c表示反应物的平衡浓度) 图①,若p1>p2>p3,则正反应为气体体积减小的反应,ΔH<0;图②,若T1 >T2,则正反应为放热反应。
(特殊图像的类型)1.对于化学反应mA(g)+nB(g)⇌p(C)+qD(g),M点前,表示从反应物开始,v正>v逆;M点为刚达到平衡点(如下图);M点后为平衡受温度的影响情况,即升温,A的百分含量增加或C的百分含量减少,平衡左移,故正反应ΔH<0。
2.对于化学反应mA(g)+nB(g)⇌pC(g)+qD(g),L线上所有的点都是平衡点(如下图)。L线的左上方(E点),E点A的百分含量大于此压强时平衡体系的A的百分含量,所以,E点v正>v逆;则L线的右下方(F点),v正
【素养专练】一、基础图像题1.可逆反应2X(g)+Y(s)⇌2Z(g)在t1时刻达到平衡状态。当增大平衡体系压强(减小容器体积)时,下列有关正、逆反应速率(v)随时间变化的图像正确的是( )
解析:此可逆反应是反应前后气体的分子数不变的反应,达到平衡状态后,增大平衡体系的压强,正、逆反速率仍相等,但由于压强增大,所以反应速率都增大;综上,本题选C。
2.某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)⇌2C(g),达到平衡后,在不同的时间段内反应物的浓度随时间的变化如图甲所示,正逆反应速率随时间的变化如图乙所示,
下列说法中正确的是( ) A.30~40 min间该反应使用了催化剂B.化学方程式中的x=1,正反应为吸热反应C.30 min时降低温度,40 min时升高温度D.前8 min A的平均反应速率为0.08 ml·L-1·min-1
3.利用I2O5可消除CO污染,其反应为:I2O5(s)+5CO(g)⇌5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 ml CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是( ) A.b点时,CO的转化率为20%B.容器内的压强保持恒定,表明反应达到平衡状态C.b点和d点的化学平衡常数:Kb>KdD.0到0.5 min反应速率v(CO)=0.3 ml·L-1·min-1
5.CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)⇌CH3OH(g) ΔH。现在容积均为1 L的a、b、c、d、e五个密闭容器中分别充入1 ml CO和2 ml H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是( ) A.该反应的ΔH<0B.在500℃条件下达平衡时CO的转化率为60%C.平衡常数K1(300℃)
6.(NH4)2SO3氧化是氨法脱硫的重要过程。某小组在其他条件不变时,分别研究了一段时间内温度和(NH4)2SO3初始浓度对空气氧化(NH4)2SO3速率的影响,结果如图。
7.已知反应:CO(g)+3H2(g)⇌CH4(g)+H2O(g)。起始以物质的量之比为1∶1充入反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为▲)。下列有关说法正确的是( ) A.上述反应的ΔH<0B.N点时的反应速率一定比M点的快C.降低温度,H2的转化率可达到100%D.工业上用此法制取甲烷应采用更高的压强
解析:根据图像,随着温度的升高,H2的转化率降低,说明平衡向逆反应方向移动,根据勒夏特列原理,正反应为放热反应,ΔH<0,A项正确;N点压强大于M点的,M点温度高于N点的,因此无法确定两点的反应速率快慢,B项错误;此反应是可逆反应,不能完全进行到底,C项错误;控制合适的温度和压强,既能保证反应速率较快,也能保证H2有较高的转化率,采用更高的压强对设备的要求更高,增加经济成本,D项错误。
8.以二氧化碳和氢气为原料制取乙醇的反应为2CO2(g)+6H2(g)⇌CH3CH2OH(g)+3H2O(g)。某压强下的密闭容器中,按CO2和H2的物质的量比为1∶3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是( ) A.a点的平衡常数小于b点B.b点,v正(CO2)=v逆(H2O)C.a点,H2和H2O的物质的量相等D.其他条件恒定,充入更多H2,v(CO2)不变
解析:从图像可知,温度越高氢气的含量越高,说明升高温度平衡向逆反应方向移动,平衡常数越小,故平衡常数:a>b,A错误;b点只能说明该温度下,CO2和H2O的浓度相等,不能说明v正(CO2)=v逆(H2O),B错误;从图像可知,a点H2和H2O的物质的量百分数相等,故物质的量相等,C正确;其他条件恒定,充入更多H2,反应物浓度增大,正反应速率增大,v(CO2)也增大,D错误。
10.氨催化氧化时会发生如下两个竞争反应Ⅰ、Ⅱ。4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) Ⅰ4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ΔH<0 Ⅱ为分析某催化剂对该反应的选择性,在1 L密闭容器中充入1 ml NH3和2 ml O2,测得有关物质的物质的量与温度的关系如图所示。
(1)该催化剂在低温时选择反应_____(填“Ⅰ”或“Ⅱ”)。(2)520 ℃时,4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g)的平衡常数K=___________ (不要求得出计算结果,只需列出数字计算式)。(3)C点比B点所产生的NO的物质的量少的主要原因是__________________________________________。
该反应为放热反应,当温度升高,平衡向左移动
(3)已知4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH<0,正反应是放热反应,当反应达到平衡后,温度升高,平衡向左移动,导致NO的物质的量逐渐减小,即C点比B点所产生的NO的物质的量少。
11.一定条件下合成乙烯:6H2(g)+2CO2(g) CH2===CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是( ) A.生成乙烯的速率:v(M)有可能小于v(N)B.平衡常数:KM>KNC.当温度高于250 ℃,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低D.若投料比n(H2)∶n(CO2)=3∶1,则图中M点时,乙烯的体积分数为7.7%
12.顺-1,2-二甲基环丙烷和反1,2二甲基环丙烷可发生如下转化: 该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)在一定温度时为常数,分别称作正、逆反应速率常数。回答下列问题:
(1)已知:T1温度下,k(正)=0.006 s-1,k(逆)=0.002 s-1,该温度下反应的平衡常数值K1=____;该反应的活化能Ea(正)小于Ea(逆),则ΔH______0(填“小于”“等于”或“大于”)。(2)T2温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是____(填曲线编号),平衡常数值K2=________;温度T1________T2(填“小于”“等于”或“大于”),判断理由是___________________________________。
放热反应升高温度时平衡向逆反应方向移动
13.研究发现利用NH3可消除硝酸工业尾气中的NO污染。NH3与NO的物质的量之比分别为1∶3、3∶1、4∶1时,NO脱除率随温度变化的曲线如图所示。
(1)曲线a中,NO的起始浓度为6×10-4 mg·m-3,从A点到B点经过0.8 s,该时间段内NO的脱除速率为____________mg·m-3·s-1。(2)曲线b对应的NH3与NO的物质的量之比是________,其理由是________________________________________________________________________________________________________________________________________________。
根据勒夏特列原理,NH3与NO的物质的量之比越大,NH3的量越多,促使平衡向正反应方向移动,NO的脱除率越大,再根据图像,可推得曲线b对应的NH3与NO的物质的量之比为3∶1
14.(1)目前,科学家正在研究一种以乙烯作为还原剂的脱硝(NO)原理,其脱硝机理示意图如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示。
①写出该脱硝原理总反应的化学方程式:________________________________________。②为达到最佳脱硝效果,应采取的条件是____________________。
350 ℃、负载率3.0%
(2)汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以AgZSM5为催化剂,测得NO转化为N2的转化率随温度变化情况如图3所示。
若不使用CO,温度超过775 K,发现NO的分解率降低,其可能的原因是__________________________________________________________;在n(NO)/n(CO)=1的条件下,应控制的最佳温度在________左右。
NO分解反应是放热反应,升高温度不利于分解反应进行
2023届高三一轮复习 化学平衡原理中的图像分析题教学课件: 这是一份2023届高三一轮复习 化学平衡原理中的图像分析题教学课件,共43页。
2023高考化学总复习微专题大素养滴定原理的拓展应用14课件: 这是一份2023高考化学总复习微专题大素养滴定原理的拓展应用14课件,共19页。PPT课件主要包含了否或不能等内容,欢迎下载使用。
2023高考化学总复习微专题大素养“铝三角”中的图像题05课件: 这是一份2023高考化学总复习微专题大素养“铝三角”中的图像题05课件,共40页。PPT课件主要包含了知识基础,素养专练,答案D,答案B,碱式滴定管,答案A,真题演练·素养通关,KSCN,一元弱,高温焙烧等内容,欢迎下载使用。












