


广东省梅州市蕉岭县蕉岭中学2022-2023学年高三上学期第三次质检化学试题(Word版pdf答案)
展开绝密★启用前
蕉岭中学2022-2023学年高三第一学期第三次质检
化学学科试题
总分:100分 时间:75分钟
考试范围:已复习内容占80%+未复习内容20%
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Ti-48 Ni-59 Cd-112 Te-128
第I卷(选择题)
一、选择题:本题共12小题,共40分。第1-8小题,每题3分;第9-12小题,每题4分。每小题只有一个选項符合题目要求。
1.2022年北京冬奥会首次使用氢能作为火炬燃料,“飞扬”火炬的内核是“氢芯”,储存氢气的气瓶采用了铝合金材质,并用上了碳纤维缠绕,在火焰区当中植入微量显色剂,实现氢气燃烧时的淡蓝色火焰变为红色。下列说法正确的是( )
- 显色剂是一些易燃物,如甲基橙、石蕊,燃烧时使火焰变为红色
- 储存氢气的气瓶采用的铝合金属于新型无机非金属材料
- 显色剂使淡蓝色火焰变为红色,这一变化为物理变化
- 缠绕的碳纤维属于有机高分子材料
2.古医典中富含化学知识,下列描述与氧化还原反应无关的是( )
A.汞的性质:汞得硫则赤如丹
B.强水(硝酸):用水入五金皆成水
C.熬制胆矾:熬胆矾铁釜,久之亦化为铜
D.制取黄铜:红铜(Cu)六斤、倭铅(Zn)四斤,先后入罐熔化,冷定取出,即成黄铜
3.下列化学用语使用不正确的是( )
A.NH4Br的电子式:
B.甲醛的分子式为:CH2O
C.中子数为20的氯原子:1720Cl
D.CO(NH2)2的球棍模型:
4.设为阿伏伽德罗常数的值,下列说法不正确的是( )
A.三肽C6H11N3O4中的肽键数目为
B.0.1 mol CH3COOH与足量CH3CH2OH充分反应生成的CH3COOCH2CH3分子数目为0.1NA
C.5g D2O(标准状况下)中所含质子数目为2.5
D.,生成乙烷时断裂的共价键总数为2
5.甲硫醇是一种重要的化工原料,硫化氢与甲醇合成甲硫醇的催化过程如图。下列说法中不正确的是( )
A.上述过程中总反应是取代反应
B.1molCH3SH中含有5NA个共价键
C.若CD3OD和H2S参与,则可能生成CHD2SH和D2O
D.催化剂的使用大大提升了甲硫醇的平衡转化率
6.下列各溶液中加入试剂后,发生反应的离子方程式书写正确的是( )
A.向Mg(HCO3)2溶液中滴加足量NaOH溶液:Mg2++HCO3-+OH-=MgCO3↓+H2O
B.水杨酸与过量碳酸钠溶液反应:CO32-+→+CO2↑+H2O
C.Na2O2与H218O反应:2Na2O2+2H218O=4Na++4OH-+18O2↑
D.Na2S2O3溶液中加入过量次氯酸钠:S2O32-+6ClO-+H2O=2SO42-+4Cl-+2HClO
7.钠和钾是两种常见金属,下列说法正确的是( )
A. 钠元素的第一电离能大于钾 B. 基态钾原子价层电子轨道表示式为
C. 钾能置换出NaCl溶液中的钠 D. 钠元素与钾元素的原子序数相差18
8.氨广泛应用于化工、化肥、制药等领域,一种新型合成方法如下。下列说法错误的是( )
A.反应①属于人工固氮
B.反应③可利用电解溶液的方法实现
C.该转化过程总反应为
D.反应⑤在无水环境中进行时有白烟产生
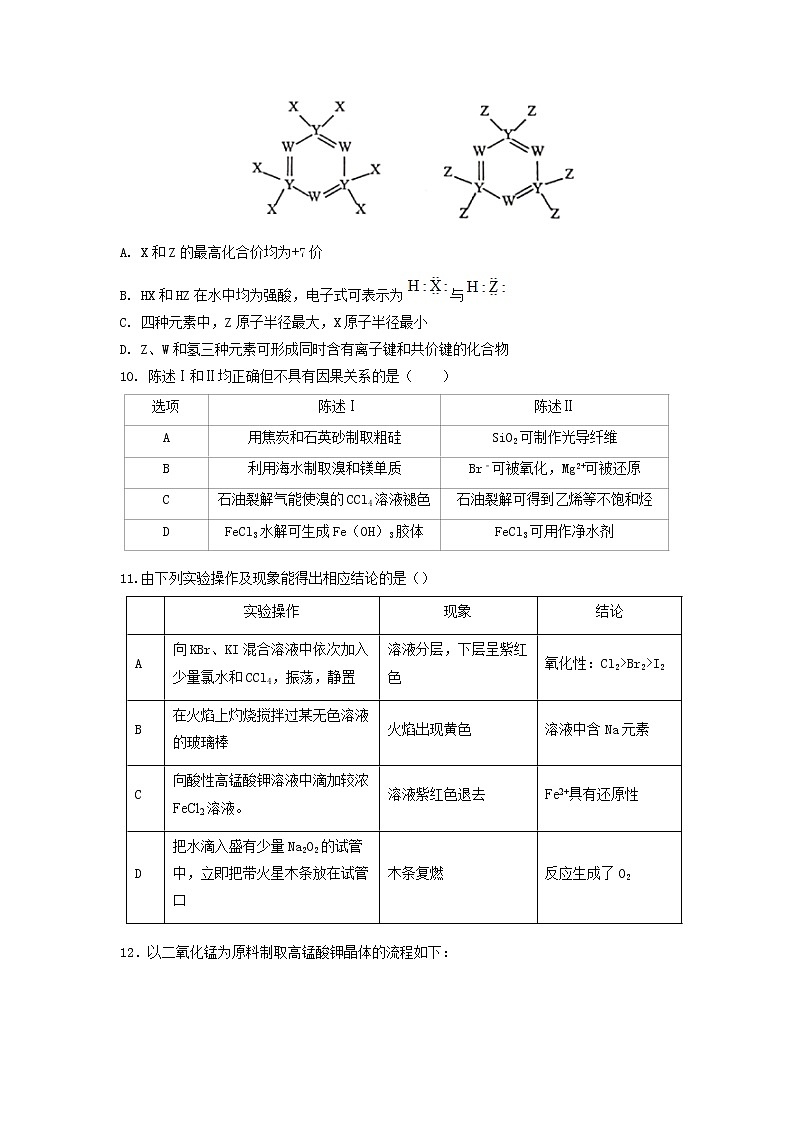
9. 如图所示的两种化合物可应用于阻燃材料和生物材料的合成。其中W、X、Y、Z为原子序数依次增大的短周期元素,X和Z同主族,Y原子序数为W原子价电子数的3倍。下列说法正确的是( )
A. X和Z的最高化合价均为+7价
B. HX和HZ在水中均为强酸,电子式可表示为与
C. 四种元素中,Z原子半径最大,X原子半径最小
D. Z、W和氢三种元素可形成同时含有离子键和共价键的化合物
10. 陈述Ⅰ和Ⅱ均正确但不具有因果关系的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 用焦炭和石英砂制取粗硅 | SiO2可制作光导纤维 |
B | 利用海水制取溴和镁单质 | Br﹣可被氧化,Mg2+可被还原 |
C | 石油裂解气能使溴的CCl4溶液褪色 | 石油裂解可得到乙烯等不饱和烃 |
D | FeCl3水解可生成Fe(OH)3胶体 | FeCl3可用作净水剂 |
11.由下列实验操作及现象能得出相应结论的是()
| 实验操作 | 现象 | 结论 |
A | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色 | 氧化性:Cl2>Br2>I2 |
B | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 溶液中含Na元素 |
C | 向酸性高锰酸钾溶液中滴加较浓FeCl2溶液。 | 溶液紫红色退去 | Fe2+具有还原性 |
D | 把水滴入盛有少量Na2O2的试管中,立即把带火星木条放在试管口 | 木条复燃 | 反应生成了O2 |
12.以二氧化锰为原料制取高锰酸钾晶体的流程如下:
下列说法不正确的是( )
A.“灼烧”不能在瓷坩埚或石英坩埚中进行
B.母液中的溶质只有、
C.“结晶”的操作步骤为:水浴加热浓缩、冷却结晶、过滤、洗涤、低温干燥
D.“转化”中的反应方程式为:
第II卷(非选择题)
二、非选择题:本题共5小题,共60分。
13.(共12分,每空2分)有机合成中成环及环的元素增减是合成路线硫代硫酸钠(Na2S2O3)可用作分析试剂及鞣革还原剂。它受热、遇酸易分解。工业上可用反应2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2制得。实验室模拟此过程的装置如图所示。
回答下列问题:
(1)b中反应的化学方程式为________________________________,c中试剂为__________________。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是________(写化学式)。
(3)d中的试剂为________。
(4)实验中要控制SO2生成速率,可以采取的措施有____________________________(写出两条)。
(5)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是_________________________。
14.(共12分,每空2分)碲化镉玻璃中主要含有CdTe(其中含有少量Fe、Ni、Mg、Si、O等元素组成的化合物),工业上利用废弃碲化镉(CdTe)玻璃回收其中金属的工艺流程如下。
已知:①常温时,有关物质的如下表。
②当溶液中离子浓度小于时,可认为沉淀完全。
回答下列问题:
(1)在“焙烧”时为提高效率可采用的措施有________________________(答出一条即可)。写出“浸渣”的工业用途:________________________。
(2)实验室中,“操作A”需要的玻璃仪器有____________。“高温尾气”中的在水溶液中可用将其还原为Te单质,写出该反应的化学方程式:__________________。
(3)“氧化除铁”步骤中可以先调节pH为5,然后再加入,则此时被氧化的离子方程式为__________________。
(4)测得“滤液I”中浓度为,取1L滤液,则至少加入______g固体才能使沉淀完全。
15.(共12分,除标明外每空2分)回答下列问题
(1)火箭推进剂中较普遍的组合是肼()和,两者反应生成和水蒸气。已知:
①
②
③
和反应生成和的热化学方程式为___________
(2)溶液常用于腐蚀印刷电路铜板,发生,若将此反应设计成原电池,当线路中转移0.2mol电子时,则被腐蚀铜的质量为___________g。
(3)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
①B为生物燃料电池的___________(填“正”或“负”)极。(1分)
②在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是___________。
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:,
①放电时,负极,则正极反应为___________
②放电时,___________(填“正”或“负”)极附近溶液的碱性增强。(1分)
(5)潜艇中使用的液氨液氧燃料电池工作原理如图所示:
电极a的电极反应式为___________
16.(共13分,除标明外每空2分)全球首次在350公里时速的奥运版复兴号高铁列车上依托5G技术打造的超高清直播演播室,实现了超高清信号的长时间稳定传输。请回答下列问题:
(1)5G芯片主要材质是高纯硅。基态Si原子价层电子的运动状态有_______种,若其电子排布式表示为[ Ne]3s23违背了_______。(各1分)
(2)高纯硅制备过程中会有SiHCl3、SiCl4等中间产物生成。沸点:SiHCl3_______ SiCl4(填“>”或“<”),(1分)与SiCl4互为等电子体的离子为_______(任写1种即可)。(1分)已知电负性:H>Si,则SiHCl3充分水解的化学方程式为_______。
(3)复兴号高铁车体材质用到Mn、Co等元素。
①Mn的一种配合物化学式为[ Mn(CO)5( CH3CN)],下列说法正确的是_______ (填字母标号)。
A. CH3CN与Mn原子配位时,提供孤电子对的是C原子
B. Mn原子的配位数为6
C. CH3CN中C原子的杂化类型为sp2、sp3
D. CH3CN中σ键与π键数目之比为5:2
②已知r(Co2+) =65 pm,r(Mn2+) =67 pm,推测MnCO3比CoCO3的分解温度_______(填“高”或“低”),(1分)解释原因_______。
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)为aD(1D= 10 -10m) ,其中阴离子( N3- )采用面心立方最密堆积方式,则该氮化钛的密度_______g· cm-3(列出计算式即可)。
17.(共11分,除标明外每空2分)一种合成解热镇痛类药物布洛芬的方法如下:
已知是一种还原剂,回答下列问题。
(1)C分子式为_______。
(2)D的结构简式是_______。
(3)E→F的化学方程式为_______。
(4)化合物M的分子式为,与布洛芬互为同系物,且有6个化学环境相同的氢原子,写出一种符合条件的M的结构简式_______。
(5)参照上述合成路线,设计一条以2—丙醇主要原料合成合成路线(其他无机试剂任选)。(3分)
2022届广东省梅州市高三下学期4月总复习质检(二模)化学试题(PDF版含答案): 这是一份2022届广东省梅州市高三下学期4月总复习质检(二模)化学试题(PDF版含答案),文件包含2022届广东省梅州市高三二模4月化学试题pdf、2022年高三第二次质检化学答案定稿pdf等2份试卷配套教学资源,其中试卷共11页, 欢迎下载使用。
广东省梅州市丰顺县中2022-2023学年高三上学期期末考试化学试题(Word版含答案): 这是一份广东省梅州市丰顺县中2022-2023学年高三上学期期末考试化学试题(Word版含答案),共15页。试卷主要包含了单选题,解答题等内容,欢迎下载使用。
广东省梅州市大埔县虎山高级中学校2022-2023学年高三上学期期末考试化学试题(Word版含答案): 这是一份广东省梅州市大埔县虎山高级中学校2022-2023学年高三上学期期末考试化学试题(Word版含答案),共14页。试卷主要包含了01,158 ml·L-1·s-1等内容,欢迎下载使用。












