

- 2022金华十校高一上学期期末考试历史含答案 试卷 0 次下载
- 2022金华十校高一上学期期末考试生物含解析 试卷 0 次下载
- 2022金华十校高一上学期期末考试物理含解析 试卷 1 次下载
- 2022金华十校高一上学期期末考试生物含答案 试卷 0 次下载
- 2022金华十校高一上学期期末考试物理含答案 试卷 1 次下载
2022金华十校高一上学期期末考试化学含答案
展开金华十校2021—2022学年第一学期期末调研考试
高一化学试题卷
说明:1.全卷满分100分,考试时间90分钟;
2.将答案写在答题卷相应的位置上;
3.可能用到的相对原子质量:H-1C-12N-14 O-16Na-23Mg-24S-32 Cl-35.5 Ca-40 Fe-56 Cu-64 Ba-137
一、选择题(本大题共25小题,每小题2分,共50分.每小题列出的四个选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1.是地球上分布最广泛的物质,的摩尔质量为()
A.10 B.18 C. D.
2.下列物质的俗名与化学式对应正确的是()
A.铁红—B.生石灰—
C.苛性钠—D.漂白液有效成分—
3.下列关于我国飞机所用的材料中,主要成分属于金属材料的是()
A.座椅滑轨——铝锂合金 B.轮胎——橡胶 C.尾翼主盒——碳纤维 D.风挡——玻璃
4.完成下列实验需用右图所示仪器的是()
A.制备少量气体 B.溶解少量固体
C.配置的溶液 D.配制溶液
5.下列变化中只涉及物理变化的是()
A.铁粉作食品的抗氧化剂B.氯气加压制液氯
C.过氧化钠作呼吸面具的供氧剂 D.盐酸除锈
6.当光束通过下列分散系时,能产生丁达尔效应的是()
A.溶液 B.溶液 C.胶体 D.稀
7.常温下实现下列转化,一定要加入其它物质作还原剂的是()
A. B.C.D.
8.下列化学用语表示正确的是()
A.氯气的分子结构模型: B.硫原子的结构示意图:
C.的电离方程式:
D.用电子式表示的形成过程:
9.下列物质中存在共价键的是()
A.B.C.D.
10.下列有关实验安全的叙述不正确的是()
A.观察活泼金属与反应时,需要戴护目镜
B.标准符号示意“毒性物质”
C.浓溶液沾到手上应立即用大量水冲洗
D.中学实验室中可以将未用完的钠、钾和白磷等放回原试剂瓶
11.下列说法不正确的是()
A.氯化钠溶液中存在水合钠离子和水合氯离子 B.“月壤”中含有,该原子的中子数是5
C.红磷、白磷都是磷元素的同素异形体 D.在合金中加入适量稀土金属,能大大改善合金的性能
12.下列反应的离子方程式书写正确的是()
A.碳酸钡与盐酸反应:
B.用小苏打治疗胃酸过多:
C.碳酸氢铵溶液与足量的氢氧化钠溶液反应:
D.用铝与溶液反应疏通污水管道:
13.下列各组离子在无色透明溶液中能大量共存的是()
A.B.
C.D.
14.下列几种类推结论符合事实的是()
A.碳酸钠溶于水放热,则碳酸氢钠溶于水也放热
B.可改写为,则也可改写为
C.是氧化还原反应,则也是氧化还原反应
D.溶于生成,则也能溶于生成
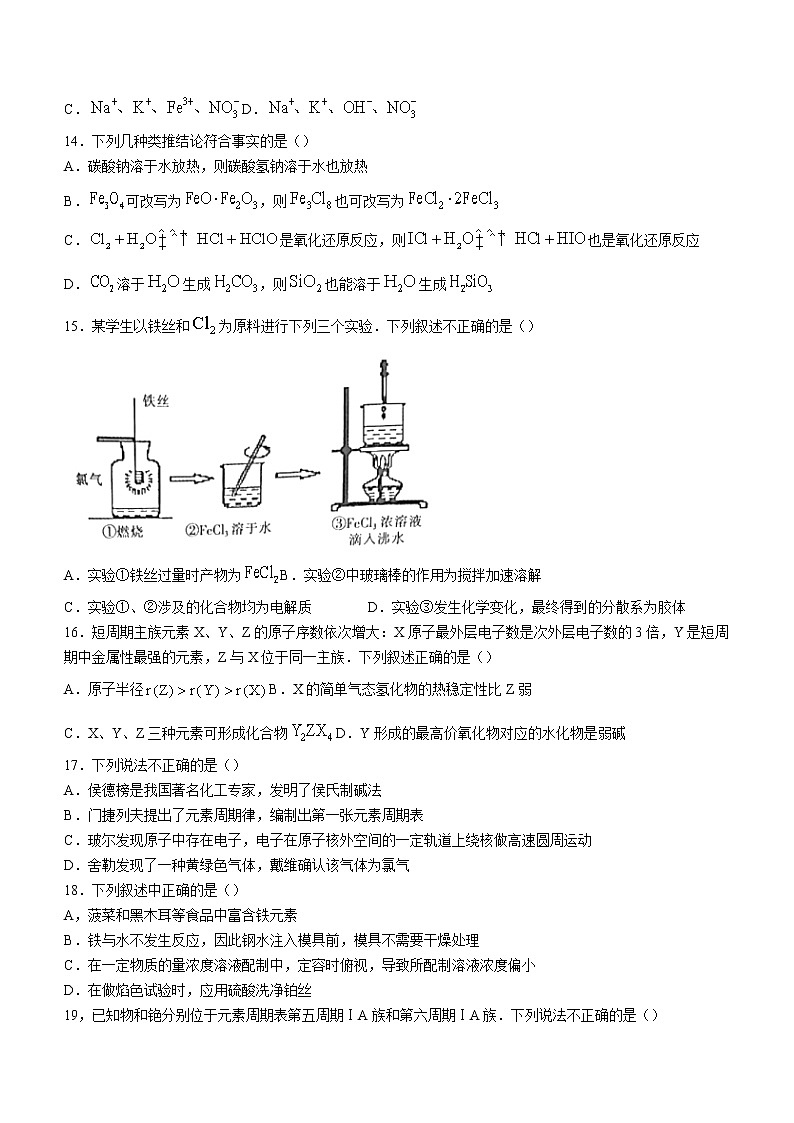
15.某学生以铁丝和为原料进行下列三个实验.下列叙述不正确的是()
A.实验①铁丝过量时产物为B.实验②中玻璃棒的作用为搅拌加速溶解
C.实验①、②涉及的化合物均为电解质 D.实验③发生化学变化,最终得到的分散系为胶体
16.短周期主族元素X、Y、Z的原子序数依次增大:X原子最外层电子数是次外层电子数的3倍,Y是短周期中金属性最强的元素,Z与X位于同一主族.下列叙述正确的是()
A.原子半径B.X的简单气态氢化物的热稳定性比Z弱
C.X、Y、Z三种元素可形成化合物D.Y形成的最高价氧化物对应的水化物是弱碱
17.下列说法不正确的是()
A.侯德榜是我国著名化工专家,发明了侯氏制碱法
B.门捷列夫提出了元素周期律,编制出第一张元素周期表
C.玻尔发现原子中存在电子,电子在原子核外空间的一定轨道上绕核做高速圆周运动
D.舍勒发现了一种黄绿色气体,戴维确认该气体为氯气
18.下列叙述中正确的是()
A,菠菜和黑木耳等食品中富含铁元素
B.铁与水不发生反应,因此钢水注入模具前,模具不需要干燥处理
C.在一定物质的量浓度溶液配制中,定容时俯视,导致所配制溶液浓度偏小
D.在做焰色试验时,应用硫酸洗净铂丝
19,已知物和铯分别位于元素周期表第五周期ⅠA族和第六周期ⅠA族.下列说法不正确的是()
A.绝原子的最外层电子数是1B.铷比铯的金属性弱
C.铯比铷的原子序数大32D.硝酸铯是离子化合物
20.下列说法不正确的是()
A.氯化氢溶于水破坏的微粒间作用力为共价键
B.氯气比氢气容易液化,是因为氯气分子间作用力较强
C.三氯化磷分子中磷原子和氯原子最外电子层都具有8电子的稳定结构
D.硫酸氢钠固体溶于水破坏离子键,电离出钠离子和硫酸氢根离子
21.近期科学家首次用X射线激光技术观察到与在催化剂表面生成的历程(部分微粒未画出).反应过程如下图,下列说法正确的是()
A.状态Ⅰ→状态Ⅱ发生了化学变化 B.和O生成的过程涉及电子转移
C.是具有非极性共价键的直线形分子D.状态Ⅲ→状态Ⅴ表示与的反应
22.下列实验装置进行的相应实验,达不到实验目的的是()
A.用图1装置除去中含有的少量气体
B.用图2装置加热蒸发饱和溶液制备晶体
C.用图3装置制取少量气体
D,用图4装置除去少量江水中的泥沙
23.利用废旧镀锌铁皮制备胶体粒子的流程图如下:
已知:镀锌铁皮就是铁皮表面镀上一层锌;溶于强碱时生成.
下列有关说法正确的是()
A.用氢氧化钠溶液处理废旧镀锌铁皮,主要目的是为了处理铁皮表面的油污
B.“酸溶”的离子方程式为
C.“氧化”后溶液中所存在的离子有:
D.最后一步“反应”中的作用是将部分还原成
24.表示阿伏加德罗常数的值,下列说法中不正确的是()
A.与含的稀盐酸充分反应,转移电子数目为
B.质量为的和混合物中含有中子数为
C.常温常压下,的和混合气体中,含有氧原子的数目小于
D.相同浓度的硫酸钾和硫酸铁混合液中浓度为,则溶液中的数目为
25.固体粉末可能由中的几种等物质的量混合而成,进行如下实验:
①取固体溶于足量水中,得到澄清透明溶液,将溶液分为三等份.
②在第一份溶液中滴加足量稀盐酸无明显现象,再滴加足量溶液,过滤、洗涤、干燥,得到固体.
③在第二份溶液中滴加溶液无明显现象,继续滴加双氧水,溶液显血红色.
④在第三份溶液中滴加足量溶液,过滤、洗涤、灼烧,得到固体.
下列说法正确的是()
A.固体粉末中肯定没有
B.根据④中的沉淀颜色能判断固体粉末中是否含有
C.固体粉末中肯定含有
D.上述实验无法确定固体粉末是否含有,需进一步通过焰色试验确定
二、填空题(本大题共5小题,共46分)
26.(6分)请按要求完成下列填空.
(1)下列给定的物质中:①②铝条③熔融氯化钠④乙醇.属于电解质的是________(填编号).
(2)写出金属钠投入水中反应的化学方程式_________________.
(3)比较沸点:_________(填“>”“<”“=”).
27.(10分)如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答问题:
族 周期 | ⅠA |
|
|
|
|
|
| 0 |
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
|
2 |
|
|
| ② | ③ | ④ |
|
|
3 | ⑤ |
| ⑥ | ⑦ |
|
| ⑧ |
|
(1)镁元素在周期表中的位置是_____________.
(2)②的最高价氧化物的结构式为____________.
(3)④⑤元素可形成既含离子键又含非极性共价键的离子化合物,写出该化合物的电子式:_________;写出⑥的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式_________________.
(4)W是第四周期与④同主族的元素.据此推测W不可能具有的性质是__________(填字母).
A.最高化合价为B.简单气态氢化物比稳定
C.最高价氧化物对应水化物的酸性比硫酸弱 D.单质在常温下可与氢气化合
(S)已知X为第ⅡA族元素(前四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,写出Y的原子序数_________(用含a的代数式表示).
28.(12分)已知氯气与碱反应时,产物受温度的影响.实验室中利用如图装置(部分装置省略)制备,和,并探究其氧化还原性质.
回答下列问题:
(1)仪器a的名称是____________.
(2)装置A产生氯气的化学方程式为____________.
(3)装置B的作用为____________.
(4)装置D中发生反应的离子方程式为____________.
(5)装置E可选用试剂____________(填标号).
A.溶液 B.溶液 C.澄清石灰水 D.稀硫酸
(6)探究,的氧化能力
操作:向1号和2号试管中,分别滴加适量中性溶液.
现象:1号试管溶液颜色不变,2号试管溶液变为棕色.
结论:该条件下氧化能力________(填“大于”或“小于”).
29.(8分)固体化合物X由3种元素组成.某学习小组进行了如下实验:
已知:A为二元化合物,其标况下的密度;Z加盐酸得到蓝色溶液:B加硫酸产生白色沉淀.请回答:
(1)A的分子式______________.
(2)化合物X含有_____________元素(填元素符号),X的化学式_____________.
(3)实验室常将通过热的固体Z制备氨气,该反应的化学方程式是_____________.
30.(10分)化学与人类生活、生产和社会可持续发展密切相关,请回答下列问题.
Ⅰ.(1)春秋末期工艺官书《考工记》中记载有“涑帛”的方法,即利用含有碳酸钠的水溶液来洗涤丝帛.请写出碳酸钠水溶液中通入气体的化学方程式___________________.
(2)用的溶液吸收,所得溶液中和物质的量浓度之比为____________.
Ⅱ.如图为铁及其化合物的“价一类”二维图.
(3)图中①处填_____________,②处填_____________.
(4)某小组在探究性质的实验(实验1)时,观察到溶液变红,片刻红色褪去,有气体生成.
三、计算题(本题4分)
31.向含有一定量盐酸和的混合溶液中逐滴滴加溶液,产生沉淀的质量m与加入的物质的量n之间的关系如图所示,按要求填空:
(1)段产生的沉淀为_____________(填写化学式).
(2)原混合溶液中_____________.
金华十校2021-2022学年第一学期期末调研考试
高一化学参考答案
一、选择题(本大题共25小题,每小题2分,共50分)
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
答案 | D | A | A | D | B | C | C | A | A | B |
题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
答案 | B | D | D | B | A | C | C | A | C | D |
题号 | 21 | 22 | 23 | 24 | 25 |
|
|
|
|
|
答案 | B | A | C | D | C |
|
|
|
|
|
二、填空题(本大题共5小题,共46分)
26.(6分)
(1)①③(2分)(2)2Na+2H2O=2NaOH+H2↑(2分)(3)>(2分)
27.(10分)
(1)第三周期第ⅡA族(1分)
(2)O=C=O(1分)
(3)(2分);2OH-+Al2O3=2AlO2-+H2O (2分)
(4)BD (2分)
(5)a+1、a+11(2分)
28.(12分)
(1)分液漏斗(2分)
(2)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O (2分)
(3)除去氯气中的氯化氢气体(2分)
(4)2OH-+Cl2=Cl-+ClO-+H2O(2分)
(5)B(2分)
(6)小于(2分)
29.(8分)
(1)SO2(2 分)
(2)Ba、Cu、S(2 分);BaCuS2(2 分)
(3)2NH3+3CuO3Cu+N2↑+3H2O(或 2NH3+6CuO3Cu2O+N2↑+3H2O)(2 分)
30.(10分)
(1)Na2CO3+H2O+CO2=2NaHCO3(2分)
(2)1:3 (2分)(3)①单质(2分)②Fe(OH)3(2分)
(4)SCN-[或Fe(SCN)3]被氧化为SO42− (SCN-[或Fe(SCN)3]被氧化也给分) (2分)
三、计算题(本题4分)
31.(1)Cu(OH)2(2分)(2)4(2分)
浙江省金华十校2022-2023学年高一上学期期末考试化学含答案: 这是一份浙江省金华十校2022-2023学年高一上学期期末考试化学含答案,共13页。试卷主要包含了5mL蒸馏水,4L,074等内容,欢迎下载使用。
浙江省金华十校2022-2023学年高二上学期期末考试化学含答案: 这是一份浙江省金华十校2022-2023学年高二上学期期末考试化学含答案,共14页。试卷主要包含了可能用到的相对原子质量,下列叙述错误的是,下列说法正确的是,可逆反应等内容,欢迎下载使用。
2022-2023学年浙江省金华十校高一上学期期末考试 化学 PDF版: 这是一份2022-2023学年浙江省金华十校高一上学期期末考试 化学 PDF版,共7页。











