



高考化学一轮复习精讲精练第08讲 氧化还原反应的基本概念和规律(精讲)(2份打包,解析版+原卷版,可预览)
展开第8讲 氧化还原反应的基本概念和规律
【核心素养分析】
证据推理与模型认知:建立氧化还原反应的观点,掌握氧化还原反应的规律,结合常见的氧化还原反应理解有关规律;通过分析、推理等方法认识氧化还原反应的特征和实质,建立氧化还原反应计算和配平的思维模型。
科学探究与创新意识:认识科学探究是进行科学解释和发现。创造和应用的科学实践活动;能从氧化还原反应的角度,设计探究方案,进行实验探究,加深对物质氧化性、还原性的理解。
【重点知识梳理】
知识点一 氧化还原反应的相关概念
一、氧化还原反应
1.氧化还原反应的本质和特征
2.氧化还原反应的相关概念及其关系
例如,反应MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O中,氧化剂是MnO2,还原剂是HCl,氧化产物是Cl2。生成1 mol Cl2时转移电子数目为2NA,被氧化的HCl的物质的量是2_mol,盐酸表现的性质是酸性和还原性。
【特别提醒】元素由化合态变为游离态时,该元素不一定被还原。如:Cu2+→Cu时,铜元素被还原,Cl-→Cl2时,氯元素被氧化。
3.氧化还原反应中电子转移的表示方法
(1)双线桥法
①表示方法
写出Cu与稀硝酸反应的化学方程式并用双线桥标出电子转移的方向和数目:
。
②注意事项
a.箭头指向反应前后有元素化合价变化的同种元素的原子,且需注明“得到”或“失去”。
b.箭头的方向不代表电子转移的方向,仅表示电子转移前后的变化。
c.失去电子的总数等于得到电子的总数。
(2)单线桥法
①表示方法
写出Cu与稀硝酸反应的化学方程式并用单线桥标出电子转移的方向和数目:
。
②注意事项
a.箭头从失电子元素的原子指向得电子元素的原子。
b.不标“得到”或“失去”,只标明电子转移的总数。
c.线桥只出现在反应物中。
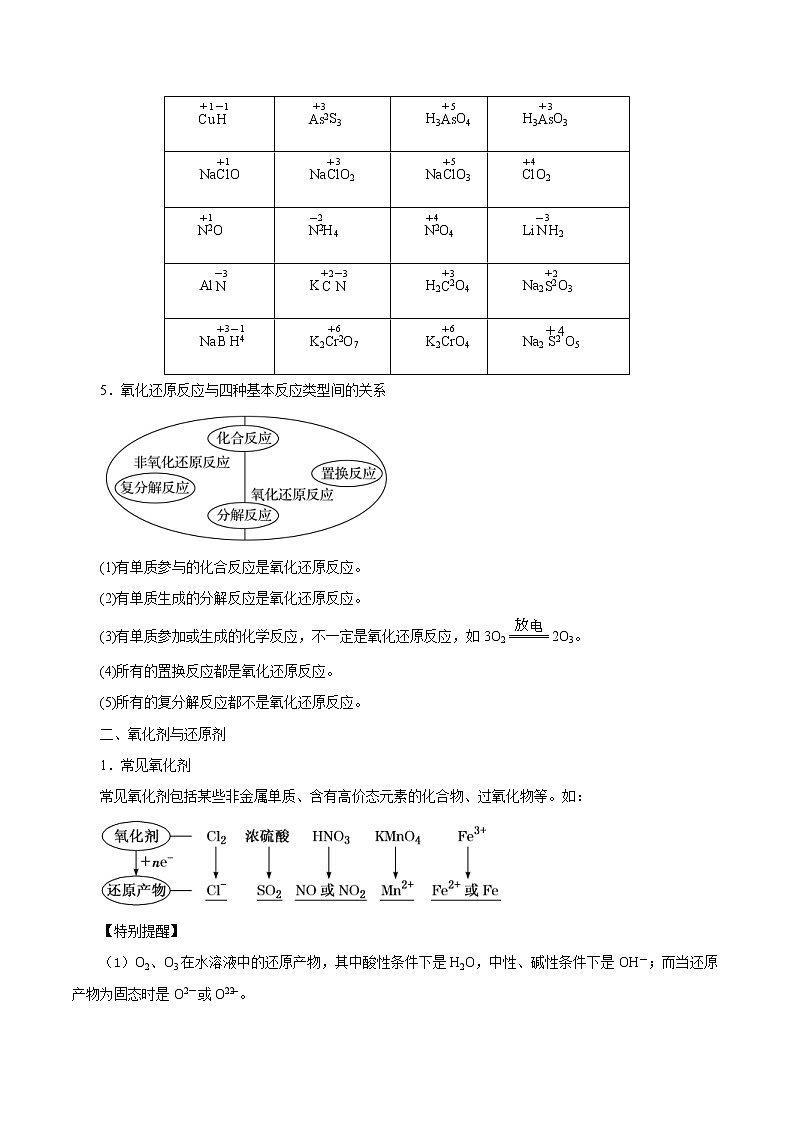
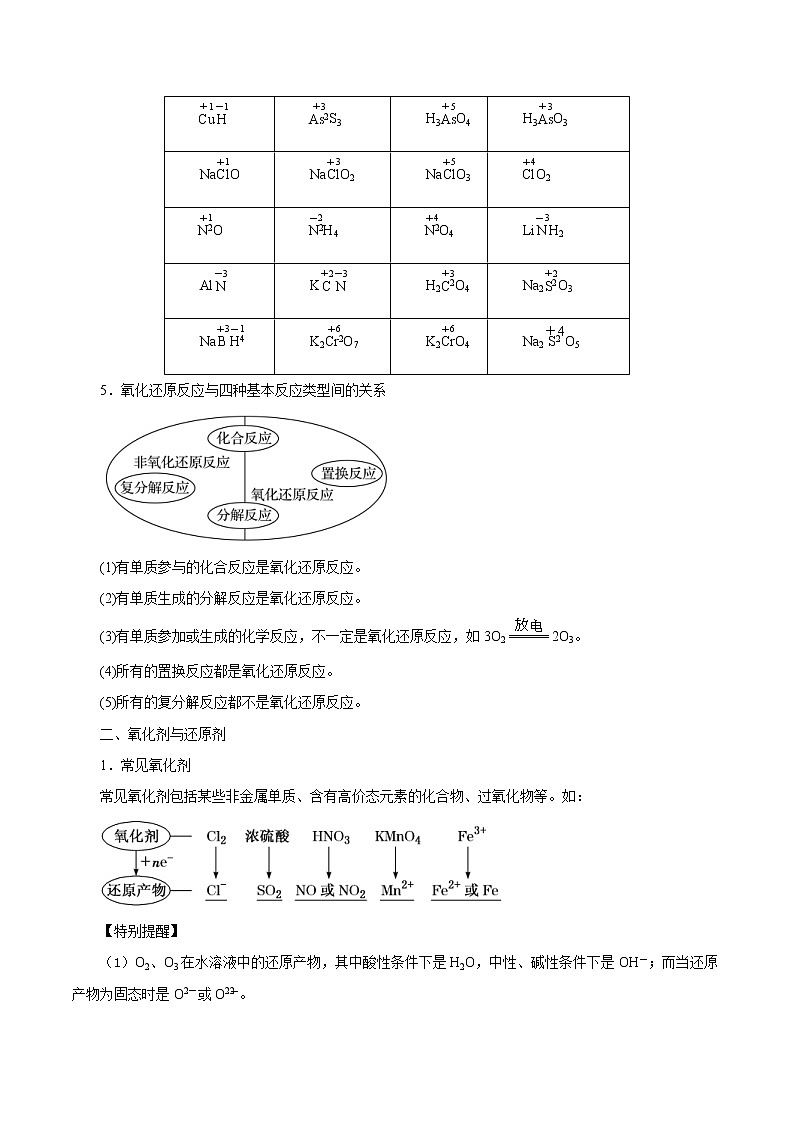
4.一些特殊物质中元素的化合价
(OH)2
O(OH)2
PO4
LiPO4
K2O4
Cu
Cl
(OH)2Cl2
S3
H3O4
H3O3
NaO
NaO2
NaO3
O2
O
H4
O4
LiH2
Al
K
H2O4
Na2O3
Na
K2O7
K2O4
Na2O5
5.氧化还原反应与四种基本反应类型间的关系
(1)有单质参与的化合反应是氧化还原反应。
(2)有单质生成的分解反应是氧化还原反应。
(3)有单质参加或生成的化学反应,不一定是氧化还原反应,如3O22O3。
(4)所有的置换反应都是氧化还原反应。
(5)所有的复分解反应都不是氧化还原反应。
二、氧化剂与还原剂
1.常见氧化剂
常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:
【特别提醒】
(1)O2、O3在水溶液中的还原产物,其中酸性条件下是H2O,中性、碱性条件下是OH-;而当还原产物为固态时是O2-或O。
(2)浓硝酸的还原产物是NO2,稀HNO3的还原产物是NO。
2.常见还原剂
常见还原剂包括活泼的金属单质、非金属离子及低价态化合物、低价金属阳离子、非金属单质及其氢化物等。如:
3.既可作氧化剂,又可作还原剂的物质或粒子
具有中间价态的物质或粒子既具有氧化性,又具有还原性,当遇到强还原剂反应时,作氧化剂,表现氧化性;当遇到强氧化剂反应时,作还原剂,表现还原性。常考物质或粒子归纳如下:
【特别提醒】同一种氧化剂(或还原剂)所对应的还原产物(或氧化产物)不是一成不变的,而是决定于还原剂(或氧化剂)的性质、反应条件、反应物的浓度、反应介质的酸碱性等多种因素。如KMnO4在酸性溶液中的还原产物一般是Mn2+;在中性或碱性溶液中的还原产物一般是锰的较高价态的化合物,如MnO2、K2MnO4等。
【名师归纳】氧化还原反应概念的“五个误区”
误区一:某元素由化合态变为游离态时,该元素不一定被还原,也不一定被氧化。因为元素处于化合态时,其化合价可能为正,也可能为负。若元素由负价变为0价,则其被氧化,若元素由正价变为0价,则其被还原。
误区二:在氧化还原反应中,非金属单质不一定只作氧化剂,大部分非金属单质往往既具有氧化性又具有还原性,只是以氧化性为主。如在反应Cl2+H2OHCl+HClO中,Cl2既表现氧化性又表现还原性。
误区三:物质的氧化性或还原性的强弱取决于元素原子得失电子的难易程度,与得失电子数目的多少无关。
误区四:氧化还原反应中的反应物不一定都是氧化剂或还原剂,有的反应物可能既不是氧化剂也不是还原剂。如Cl2+H2OHCl+HClO,H2O既不是氧化剂,也不是还原剂。
误区五:在氧化还原反应中,一种元素被氧化,不一定有另一种元素被还原,也可能是同一元素既被氧化又被还原。如:2Na2O2+2H2O===4NaOH+O2↑中,Na2O2既是氧化剂又是还原剂,氧元素一部分化合价升高,一部分化合价降低。
知识点二 物质氧化性、还原性强弱的判断
一、氧化性、还原性强弱的认识
1.氧化性指物质得电子的性质(或能力);还原性指物质失电子的性质(或能力)。
2.氧化性、还原性的强弱取决于物质得、失电子的难易程度,与得、失电子数目的多少无关。例如:Na-e-===Na+,Al-3e-===Al3+,根据金属活动性顺序可知,Na比Al活泼,更易失去电子,所以Na比Al的还原性强。
3.从元素的价态考虑:最高价态——只有氧化性,如H2SO4、KMnO4等;最低价态——只有还原性,如金属单质、Cl-、S2-等;中间价态——既有氧化性,又有还原性,如Fe2+、S、Cl2等。
二、氧化性、还原性强弱的比较方法
物质氧化性(得电子的能力)、还原性(失电子的能力)的强弱取决于物质得失电子的难易,与得失电子的数目无关,但也与外界因素(如反应条件、反应物浓度、酸碱性等)有关,具体判断方法如下:
1.依据氧化还原反应原理来判断
(1)氧化性强弱:氧化剂>氧化产物。
(2)还原性强弱:还原剂>还原产物。
2.依据“二表、一律”判断
(1)依据元素周期表判断
①同主族元素对应单质的氧化性从上到下逐渐减弱,对应阴离子的还原性逐渐增强。
②同周期元素对应单质的还原性从左到右逐渐减弱,氧化性逐渐增强。
(2)依据金属活动性顺序表判断
(3)依据元素周期律判断
①非金属元素的最高价氧化物对应水化物的酸性越强,其对应单质的氧化性越强。
如酸性:HClO4>H2SO4>H3PO4>H2CO3>H2SiO3,则氧化性:Cl2>S>P>C>Si。
②金属元素的最高价氧化物对应水化物的碱性越强,其对应单质的还原性越强。
如碱性:NaOH>Mg(OH)2>Al(OH)3,则还原性:Na>Mg>Al。
3.依据产物中元素价态的高低判断
(1)相同条件下,不同氧化剂作用于同一种还原剂,氧化产物价态高的其氧化性强。例如:
(2)相同条件下,不同还原剂作用于同一种氧化剂,还原产物价态低的其还原性强。例如:
4.依据电化学原理判断
(1)原电池:一般情况下,两种不同的金属构成原电池的两极,其还原性:负极>正极。
(2)电解池:用惰性电极电解混合溶液时,在阴极先放电的阳离子的氧化性较强,在阳极先放电的阴离子的还原性较强。
5.依据影响因素判断
(1)浓度:同一种物质,浓度越大,氧化性(或还原性)越强。如氧化性:浓H2SO4>稀H2SO4,浓HNO3>稀HNO3;还原性:浓HCl>稀HCl。
(2)温度:同一种物质,温度越高其氧化性越强。如热的浓硫酸的氧化性比冷的浓硫酸的氧化性强。
(3)酸碱性:同一种物质,所处环境酸(碱)性越强其氧化(还原)性越强。如氧化性:KMnO4(酸性)>KMnO4(中性)>KMnO4(碱性)。
6.依据反应条件判断
浓度
同一种物质,浓度越大,氧化性(或还原性)越强。如氧化性:浓H2SO4>稀H2SO4,浓HNO3>稀HNO3;还原性:浓HCl>稀HCl
温度
同一种物质,温度越高其氧化性越强。如热的浓硫酸的氧化性比冷的浓硫酸的氧化性强
知识点三 氧化还原反应的规律及其应用
一、价态规律
1.升降规律
氧化还原反应中,化合价有升必有降,升降总值相等。
2.价态归中规律
含不同价态的同种元素的物质间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低价―→中间价”,而不会出现交叉现象。简记为“两相靠,不相交”。
例如:不同价态硫之间可以发生的氧化还原反应是下图中的①②③④。
【特别提醒】不会出现⑤中H2S转化为SO2,而H2SO4转化为S的情况。
3.歧化反应规律
“中间价―→高价+低价”。具有多种价态的元素(如氯、硫、氮和磷元素等)均可发生歧化反应。
例如:Cl2+2NaOH===NaCl+NaClO+H2O。
二、强弱规律
1.根据氧化性和还原性规律判断
同一个反应中,氧化剂的氧化性强(填“强”或“弱”)于氧化产物的氧化性,还原剂的还原性强于还原产物的还原性。如反应2FeCl3+2KI===2FeCl2+I2+2KCl中,氧化性:Fe3+>I2;还原性:I->Fe2+。
2.根据金属活动性或非金属活动性顺序判断
K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag,由左至右,单质的还原性逐渐减弱;K+、Ca2+、Na+、Mg2+、Al3+、Zn2+、Fe2+、Sn2+、Pb2+、(H+)、Cu2+、Hg2+、Ag+,由左至右,阳离子的氧化性逐渐增强;F2、Cl2、Br2、I2、S,由左至右,单质的氧化性逐渐减弱;F-、Cl-、Br-、I-、S2-,由左至右,阴离子的还原性逐渐增强。
3.根据产物中元素价态的高低判断
如2Fe+3Cl22FeCl3,Fe+SFeS,则氧化性:Cl2>(填“>”或“<”)S。
三、先后规律
同一体系中,当有多个氧化还原反应发生时,反应的先后顺序遵循强者优先的规律。例如:向含相同物质的量浓度的S2-、I-、Br-溶液中,缓慢通入氯气,还原性强的离子优先发生反应,先后顺序为S2-、I-、Br-;向含等物质的量浓度的Fe3+、Cu2+、H+、Ag+溶液中,缓慢加入足量的镁粉,氧化性强的离子优先发生反应,先后顺序为Ag+、Fe3+、Cu2+、H+。
四、守恒规律
氧化还原反应中,氧化剂得电子总数等于还原剂失电子总数。
【典型题分析】
高频考点一 氧化还原反应的判断
例1.(山东卷)下列叙述不涉及氧化还原反应的是( )
A. 谷物发酵酿造食醋 B. 小苏打用作食品膨松剂
C. 含氯消毒剂用于环境消毒 D. 大气中NO2参与酸雨形成
【答案】B
【解析】涉及淀粉水解成葡萄糖,葡萄糖氧化成乙醇,乙醇氧化成乙酸,涉及氧化还原反应,A不符合题意;小苏打即NaHCO3,NaHCO3受热分解产生无毒的CO2,因此可用小苏打作食品膨松剂,不涉及氧化还原反应,B符合题意;利用含氯消毒剂的强氧化性消毒杀菌,涉及氧化还原反应,C不符合题意;NO2与水反应有HNO3产生,因此NO2参与了硝酸型酸雨的形成,涉及氧化还原反应,D不符合题意。答案选B。
【举一反三】(2019·北京卷)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
物质(括号内为杂质)
除杂试剂
A
FeCl2溶液(FeCl3)
Fe粉
B
NaCl溶液(MgCl2)
NaOH溶液、稀HCl
C
Cl2(HCl)
H2O、浓H2SO4
D
NO(NO2)
H2O、无水CaCl2
【答案】B
【解析】FeCl3与Fe反应生成FeCl2,FeCl3+Fe=2FeCl2,此过程中Fe的化合价发生变化,涉及到了氧化还原法应,故A不符合题意;MgCl2与NaOH溶液发生复分解反应MgCl2+2NaOH=Mg(OH)2 +2NaCl,过量的NaOH溶液可用HCl除去HCl+NaOH=NaCl+H2O ,此过程中没有元素化合价发生变化,未涉及氧化还原反应,故B符合题意;部分氯气与H2O 发生反应生成氯化氢和次氯酸,反应过程中氯元素化合价变化,涉及到了氧化还原法应,故C不符合题意;NO2 与水反应生成硝酸和NO。反应过程中氮元素化合价发生变化,涉及到了氧化还原法应,故D不符合题意;综上所述,本题应选B。
【变式探究】 (2018·北京卷)下列实验中的颜色变化,与氧化还原反应无关的是( )
选项
A
B
C
D
实验
NaOH溶液滴入FeSO4溶液中
石蕊溶液滴入氯水中
Na2S溶液滴入AgCl浊液中
热铜丝插入稀硝酸中
现象
产生白色沉淀,随后变为红褐色
溶液变红,随后迅速褪色
沉淀由白色逐渐变为黑色
产生无色气体,随后变为红棕色
【答案】C
【解析】A项,NaOH溶液滴入FeSO4溶液中,会生成Fe(OH)2白色沉淀,Fe(OH)2被氧化为Fe(OH)3,反应过程中出现灰绿色,最后变为红褐色,与氧化还原反应有关;B项,由于氯水显酸性,先使紫色石蕊溶液变红,后由于HClO具有氧化性,使红色溶液迅速褪色,与氧化还原反应有关;C项,向AgCl浊液中滴加Na2S溶液,白色沉淀变成黑色,发生沉淀的转化,反应的离子方程式为2AgCl+S2-===Ag2S+2Cl-,与氧化还原反应无关;D项,热铜丝插入稀硝酸中发生的反应为3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O,NO被氧气氧化生成红棕色的NO2,与氧化还原反应有关。
高频考点二 氧化还原反应中相关概念的判断
例2.(重庆巴蜀中模拟)LiAlH4是重要的储氢材料,可与水发生反应:LiAlH4+2H2O===LiAlO2+4H2↑。下列说法中正确的是 ( )
A.氢气既是氧化产物又是还原产物
B.LiAlH4既是氧化剂又是还原剂
C.若生成标准状况下4.48 L H2,则转移0.4 mol电子
D.还原剂与氧化剂的物质的量之比为2∶1
【答案】A
【解析】由反应方程式可知,LiAlH4中H由-1价升高为0价,被氧化,是还原剂,H2O中H由+1价降低为0价,被还原,是氧化剂,氢气既是氧化产物又是还原产物,A正确、B错误;由反应方程式可知,每1 mol LiAlH4反应,转移4 mol电子,生成4 mol H2,若生成标准状况下4.48 L(即0.2 mol)H2,则转移0.2 mol电子,C错误;LiAlH4为还原剂,H2O为氧化剂,还原剂与氧化剂的物质的量之比为1∶2,D错误。
【变式探究】(广东中山纪念中学模拟)含氟的卤素互化物通常做氟化剂,使金属氧化物转化为氟化物,如2Co3O4+6ClF3===6CoF3+3Cl2+4X。下列有关该反应的说法中,正确的是 ( )
A.X与O3互为同位素
B.ClF3中氯元素为+4价
C.Co3O4在反应中做氧化剂
D.1 mol Co3O4参加反应转移9 mol电子
【答案】D
【解析】根据质量守恒定律可知,X为O2,其与O3互为同素异形体,A错误。ClF3中F元素非金属性大于Cl元素,氟元素为-1价,则氯元素为+3价,B错误。反应中Co元素的化合价由+价升高到+3价,被氧化,O元素的化合价由-2价升高到0价,被氧化,则Co3O4做还原剂,C错误。Co3O4中O元素的化合价由-2价升高到0价,Co元素的化合价由+价升高到+3价,1 mol Co3O4参加反应转移电子的物质的量为[2×4+3×(3-)] mol=9 mol,D正确。
高频考点三 氧化性、还原性强弱的判断
例3.(河南省实验中学模拟)已知:Co2O3、Cl2、Fe3+、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是( )
A.3Cl2+6FeI2(少量)===2FeCl3+4FeI3
B.Cl2(少量)+FeI2===FeCl2+I2
C.Co2O3+6HCl(浓)===2CoCl2+Cl2↑+3H2O
D.Co2O3+2Fe2++6H+===2Fe3++2Co2++3H2O
【答案】A
【解析】因为氧化性:Cl2>Fe3+>I2,所以Cl2与FeI2 反应时先氧化I-,后氧化Fe2+,Cl2过量时将FeI2完全氧化,发生反应的化学方程式为2FeI2+3Cl2===2FeCl3+2I2,A错误;Cl2与FeI2反应,Cl2不足时先氧化I-,若还有剩余的Cl2,才氧化Fe2+,B正确;因为氧化性:Co2O3>Cl2,所以反应Co2O3+6HCl(浓)===2CoCl2+Cl2↑+3H2O能发生,C正确;因为氧化性:Co2O3>Fe3+,所以反应Co2O3+2Fe2++6H+===2Fe3++2Co2++3H2O能发生,D正确。
【变式探究】(福建泉州五中模拟)已知2Fe3++2I-===I2+2Fe2+、2Fe2++Br2===2Br-+2Fe3+。现向含有FeBr2、FeI2的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色,则下列叙述中正确的是 ( )
①氧化性:Br2>Fe3+>I2
②原溶液中Br-一定被氧化
③通入氯气后,原溶液中的Fe2+一定被氧化
④不能确定通入氯气后的溶液中是否还存在Fe2+
⑤若取少量所得溶液,加入CCl4后静置,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中Fe2+、Br-均被完全氧化
A.①②③④ B.①③④⑤
C.②④⑤ D.①②③④⑤
【答案】B
【解析】由已知的两个化学方程式及同一个反应中氧化剂的氧化性大于氧化产物的氧化性可知,氧化性Fe3+>I2、Br2>Fe3+,故①正确;向溶液中滴加KSCN溶液,溶液变为红色说明溶液中含有Fe3+,又还原性I->Fe2+>Br-,氯气的量不确定,则Br-不一定被氧化,②错误,③正确;由上述分析可知溶液中存在Fe3+,但不能确定是否所有的Fe2+均被氧化为Fe3+,④正确;上层溶液中若含Br-,则产生淡黄色沉淀,只产生白色沉淀,则说明溶液中只含Cl-,即溶液中的Fe2+、Br-均被完全氧化,⑤正确。
高频考点四 价态规律、守恒规律的应用
例4.(安徽淮北一中模拟)已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G―→Q+NaCl
②Q+H2OX+H2
③Y+NaOH―→G+Q+H2O
④Z+NaOH―→Q+X+H2O
这五种化合物中Cl元素化合价由低到高的顺序是 ( )
A.G、Y、Q、Z、X B.X、Z、Q、G、Y
C.X、Z、Q、Y、G D.G、Q、Y、Z、X
【答案】A
【解析】反应①中,NaCl中Cl元素为-1价,则Cl元素的化合价:Q>G>-1;反应②中,H元素的化合价降低,则Cl元素化合价升高,则Cl元素化合价:X>Q;反应③为歧化反应,结合①分析可知,Cl元素的化合价:Q>Y>G;同理可知,反应④中Cl元素的化合价:X>Z>Q。综上所述,五种化合物中氯元素的化合价:X>Z>Q>Y>G,故A项正确。
【变式探究】(江苏苏州中学模拟)用CuS、Cu2S处理酸性废水中Cr2O,发生反应如下。
反应Ⅰ:CuS+Cr2O+H+―→Cu2++SO+Cr3++H2O(未配平)
反应Ⅱ:Cu2S+Cr2O+H+―→Cu2++SO+Cr3++H2O(未配平)
下列有关说法正确的是 ( )
A.反应Ⅰ、Ⅱ中Cu2+和SO都是氧化产物
B.处理1 mol Cr2O时反应Ⅰ、Ⅱ中消耗H+的物质的量相等
C.反应Ⅱ中参与反应的还原剂、氧化剂的物质的量之比为3∶5
D.反应Ⅰ、Ⅱ中处理1 mol Cr2O,转移电子数不相等
【答案】C
【解析】反应Ⅰ中CuSSO,Cr2O2Cr3+,根据得失电子守恒配平方程式:3CuS+4Cr2O+32H+===3Cu2++3SO+8Cr3++16H2O;反应Ⅱ中Cu2SSO,Cu2S2Cu2+,Cr2O2Cr3+,根据得失电子守恒配平方程式:3Cu2S+5Cr2O+46H+===6Cu2++3SO+10Cr3++23H2O。反应Ⅰ中铜元素的化合价未发生变化,A错误;处理1 mol Cr2O时,反应Ⅰ消耗8 mol H+,反应Ⅱ消耗9.2 mol H+,B错误;反应Ⅱ中硫化亚铜是还原剂,重铬酸根离子是氧化剂,还原剂、氧化剂的物质的量之比为3∶5,C正确;处理重铬酸根离子的物质的量相等,则转移电子数相等,D错误。
高频考点五 强弱规律、先后规律的应用
例5.(辽宁阜新实验中学模拟)现有下列三个氧化还原反应:
①2FeCl3+2KI===2FeCl2+2KCl+I2
②2FeCl2+Cl2===2FeCl3
③2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O
若某溶液中含有Fe2+、Cl-和I-,要除去I-而不氧化Fe2+和Cl-,可以加入的试剂是( )
A.Cl2 B.KMnO4
C.FeCl3 D.HCl
【答案】C
【解析】本题是寻找一种氧化剂,其氧化性应大于I2的氧化性,而小于Cl2和Fe3+的氧化性(也可等于Fe3+的氧化性)。由反应①知氧化性:Fe3+>I2,还原性:I->Fe2+;由反应②知氧化性:Cl2>Fe3+,还原性:Fe2+>Cl-;由反应③知氧化性:MnO>Cl2,还原性:Cl->Mn2+;由此推知氧化性强弱顺序为KMnO4>Cl2>FeCl3>I2,还原性强弱顺序为I->Fe2+>Cl->Mn2+。所以KMnO4可氧化Cl-、Fe2+及I-,Cl2可氧化Fe2+及I-,FeCl3只能氧化I-。
【变式探究】(河北冀州中学模拟)现有下列三个反应:
①Cl2+FeI2===FeCl2+I2
②2Fe2++Br2===2Fe3++2Br-
③Co2O3+6HCl(浓)===2CoCl2+Cl2↑+3H2O
下列说法正确的是 ( )
A.①②③中的氧化产物分别是I2、Fe3+、Cl2
B.氧化性:Cl2>Co2O3>Fe3+
C.根据反应①一定可以推理得到Cl2+FeBr2===FeCl2+Br2
D.在反应③中当有1 mol Co2O3参加反应时,有1 mol HCl被氧化
【答案】A
【解析】三个反应中元素化合价升高所得的产物是I2、Fe3+、Cl2,它们是氧化产物,A正确;氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,在反应①中,氧化性:Cl2>I2,在反应②中,氧化性:Br2>Fe3+,在反应③中,氧化性:Co2O3>Cl2,所以氧化性强弱顺序是Co2O3>Cl2>Br2>Fe3+,B错误;根据氧化性强弱顺序:Cl2>Br2>Fe3+,Cl2和FeBr2反应时,氯气优先氧化Fe2+,再氧化Br-,C错误;在反应③中,当有1 mol Co2O3参加反应时,生成1 mol Cl2,有6 mol HCl参加反应,其中2 mol HCl被氧化,D错误。
高频考点六 氧化还原反应规律的综合应用
例6.(湖南衡阳八中模拟)含氰化物的废液乱倒或与酸混合,均易生成有剧毒且易挥发的氰化氢。工业上常采用碱性氯化法来处理高浓度氰化物污水,发生的主要反应为CN-+OH-+Cl2―→CO2+N2+Cl-+H2O(未配平)。下列说法错误的是(其中NA表示阿伏加德罗常数的值) ( )
A.Cl2是氧化剂,CO2和N2是氧化产物
B.上述离子方程式配平后,氧化剂与还原剂的化学计量数之比为5∶2
C.该反应中,若有1 mol CN-发生反应,则有5NA个电子发生转移
D.若将该反应设计成原电池,则CN-在正极区发生反应
【答案】D
【解析】反应中Cl元素化合价降低,N、C元素化合价升高,则Cl2是氧化剂,CO2和N2是氧化产物,故A正确;配平的离子方程式为2CN-+8OH-+5Cl2===2CO2+N2+10Cl-+4H2O,氧化剂与还原剂的化学计量数之比为5∶2,故B正确;C元素化合价由+2价升高为+4价,N元素化合价由-3价升高为0价,所以若有1 mol CN-发生反应,则有5NA个电子发生转移,故C正确;若将该反应设计成原电池,则CN-应在负极区发生氧化反应,故D错误。
【方法技巧】首先分析题意的考查点,再确定用什么规律解决问题。涉及“几种元素被氧化(或还原)”或“谁先被氧化(或还原)”问题,用先后规律解答;涉及电子转移数或氧化剂(氧化产物)与还原剂(还原产物)比例问题,必然用守恒规律解答;涉及能否发生某反应,一般属于强弱规律,而判断同种元素的不同价态的物质之间反应的化合价变化问题,则要依据价态归中规律。
【变式探究】(天津新华中学模拟)环保督察不是“一阵风”,生态环境部对大气污染、水体污染等高度重视。氰化物是污染水体的重要物质,该类物质有剧毒,特别是HCN具有挥发性,毒性更大。一般可采用次氯酸钠法进行处理,该处理方法的原理可分如下两步。
步骤①:NaCN与NaClO反应生成NaOCN和NaCl;
步骤②:NaOCN与NaClO反应生成Na2CO3、CO2、NaCl和N2。
下列有关判断正确的是 ( )
A.NaCN与NaOCN中C、N的化合价分别相等
B.步骤①可在酸性条件下进行
C.步骤②的氧化产物是CO2、Na2CO3、N2
D.步骤②生成标准状况下5.6 L气体时,转移0.75 mol电子
【答案】D
【解析】NaCN与NaOCN中Na元素的化合价均为+1价,NaOCN中含有O,O元素的化合价不是0,故这两种化合物中C元素、N元素的化合价至少有一种不相等,A错误;HCN易挥发且有毒,而酸性条件下CN-易与H+结合生成HCN,故步骤①不能在酸性条件下进行,B错误;步骤②的离子方程式为2OCN-+3ClO-===CO2↑+CO+3Cl-+N2↑,氧化剂是NaClO,还原剂是NaOCN,氧化产物是N2,还原产物是NaCl,C错误;根据上述离子方程式可知,生成1 mol N2转移电子的物质的量为6 mol,N2的体积占气体总体积的,生成标准状况下5.6 L气体时,n(e-)=6××=0.75 mol,D正确。
高考化学一轮复习精讲精练第16讲 氮及其化合物(精讲)(2份打包,解析版+原卷版,可预览): 这是一份高考化学一轮复习精讲精练第16讲 氮及其化合物(精讲)(2份打包,解析版+原卷版,可预览),文件包含高考化学一轮复习精讲精练第16讲氮及其化合物精讲解析版doc、高考化学一轮复习精讲精练第16讲氮及其化合物精讲原卷版doc等2份试卷配套教学资源,其中试卷共36页, 欢迎下载使用。
高考化学一轮复习精讲精练第15讲 硫及其化合物(精讲)(2份打包,解析版+原卷版,可预览): 这是一份高考化学一轮复习精讲精练第15讲 硫及其化合物(精讲)(2份打包,解析版+原卷版,可预览),文件包含高考化学一轮复习精讲精练第15讲硫及其化合物精讲解析版doc、高考化学一轮复习精讲精练第15讲硫及其化合物精讲原卷版doc等2份试卷配套教学资源,其中试卷共36页, 欢迎下载使用。
高考化学一轮复习精讲精练第08讲 氧化还原反应的基本概念和规律(精练)(2份打包,解析版+原卷版,可预览): 这是一份高考化学一轮复习精讲精练第08讲 氧化还原反应的基本概念和规律(精练)(2份打包,解析版+原卷版,可预览),文件包含高考化学一轮复习精讲精练第08讲氧化还原反应的基本概念和规律精练解析版doc、高考化学一轮复习精讲精练第08讲氧化还原反应的基本概念和规律精练原卷版doc等2份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。












