

2023青岛第五十八中学高一上学期期中考试化学试题含答案
展开高一化学试卷
2022.11
注意事项:
1.本试卷分第Ⅰ卷和第Ⅱ卷两部分。第Ⅰ卷为选择题,共40分;第Ⅱ卷为非选择题,共60分,满分100分,考试时间为90分钟。
2.第Ⅰ卷共8页,每小题有一个正确答案,请将选出的答案标号(A、B、C、D)涂在答题卡上。第Ⅱ卷共1页,将答案用黑色签字笔(0.5mm)写在答题纸上。
3.试卷卷面分5分,如不规范,分等级(5、3、1分)扣除。
H—1 C—12 N—14 O—16 Na—23 Mg—24 Al—27 S—32
Fe—56 Cu—64 Ca—40 Cl—35.5 K—39 I—127 Ba—137
第Ⅰ卷(共40分)
一、选择题(本题共10个小题,每小题2分,共20分。每小题只有一个正确答案。)
1.“绿色商品”是指对环境无污染的商品。下列属于“绿色商品”的是( )
A.含氟冰箱 B.含铅汽油 C.含磷洗涤剂 D.含碘食盐
2.已知 H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,则下列说法正确的是( )
A.NaH2PO2属于正盐 B.H3PO2属于三元酸
C.NaH2PO2属于酸式盐 D.H3PO2属于二元酸
3.如果1g水中含有x个H20分子,则9g金属铝中含有原子数为( )
A.9x B.6x C.3x D.x
4.关于反应K2H3IO6+9HI===2KI+4I2+6H2O,下列说法正确的是( )
A.K2H3IO6发生氧化反应
B.KI是还原产物
C.生成12.7 g I2时,转移0.1 ml电子
D.还原剂与氧化剂的物质的量之比为7∶1
5.某地有甲、乙两个工厂排放污水,污水中各含有下列8种离子中的4种(两厂不含相同离子):Ag+、Ba2+、Fe3+、Na+、Cl-、SO42-、NO3-、OH-。两厂单独排放时,都会造成严重的水污染。如果将两厂的污水按一定比例混合,过滤沉淀后污水就变为无色澄清且只含NaNO3而排放,污染程度大大降低。关于污染源的分析,你认为正确的是( )
A.Cl- 和NO3-一定来自不同的工厂 B.SO42- 和NO3-可能来自同一工厂
C.Ag+ 和Na+ 可能来自同一工厂 D.Na+ 和NO3-一定来自同一工厂
6. NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.56g铁与足量氯气完全反应;在反应中转移的电子数为2NA
B.在1 L 0.1ml·L-1的HF溶液中,含有H+离子数目为0.1NA
C.3.2gNH2-含有的电子数为2NA
D.0.1 ml·L-1的NaHSO4溶液中,Na+数目为0.1NA
7.下列离子方程式书写正确的是( )
A.饱和Na2CO3溶液中通入过量CO2:COeq \\al(2-,3)+CO2+H2O===2HCOeq \\al(-,3)
B.碳酸镁与稀盐酸反应:COeq \\al(2-,3)+2H+===CO2↑+H2O
C.盐酸滴入氨水中:H++OH-=== H2O
D.Ca(HCO3)2溶液中滴入少量Ca(OH)2溶液:
Ca2++OH-+HCOeq \\al(-,3)===CaCO3↓+H2O
8.将a g 含NaOH样品溶解在b mL 0.l ml·L-1 的硫酸中,再加入c mL 0.1 ml·L-1 的氢氧化钡溶液,反应后所得溶液恰好呈中性,则样品中 NaOH 的纯度是( )
A.[(b-c)/125a]×100% B.[(b-2c)/125a]×100%
C.[(b-c)/250a]×100% D.[(8b-8c)/a]×100%
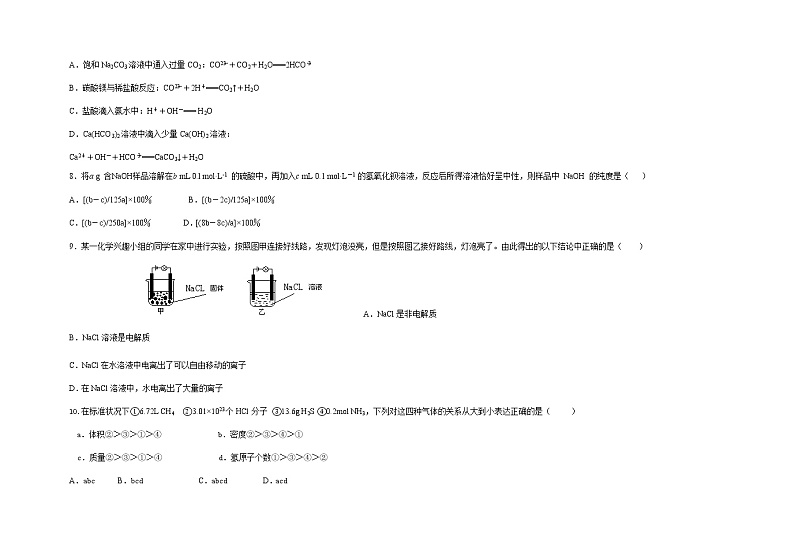
9.某一化学兴趣小组的同学在家中进行实验,按照图甲连接好线路,发现灯泡没亮,但是按照图乙接好路线,灯泡亮了。由此得出的以下结论中正确的是( )
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl在水溶液中电离出了可以自由移动的离子
D.在NaCl溶液中,水电离出了大量的离子
10.在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2ml NH3,下列对这四种气体的关系从大到小表达正确的是( )
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
A.abc B.bcd C.abcd D.acd
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.下列有关实验现象与分析或结论都正确的是( )
12.下列叙述正确的是( )
A.切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2===Na2O2
B.一定条件下,2.3 g Na完全与O2反应生成3.6 g产物,失去的电子数为0.1NA
C.钠在空气中受热时,熔化为银白色的小球,产生黄色的火焰,生成白色粉末
D.钠在空气中长期放置,最终主要生成物为碳酸钠
13.含元素碲(Te)的几种物质存在如图所示转化关系。下列说法错误的是( )
A.反应①利用了H2Te的还原性 B.反应②中H2O作氧化剂
C.反应③利用了H2O2的氧化性
D.H2Te2O5转化为H2Te4O9发生了氧化还原反应
14.三种气体X、Y、Z的相对分子质量关系为Mr(X)
B.若一定条件下,三种气体体积均为2.24 L,则它们的物质的量一定均为0.1 ml
C.同温同压下,同质量的三种气体,气体密度最小的是X
D.同温下,体积相同的两容器分别充2 g Y气体和1 g Z气体,则压强之比为4∶1
15.工业上常用CuFeS2和FeS2(二硫化亚铁)炼铁和制硫酸,反应如下
①2CuFeS2+7O2eq \(=====,\s\up7(高温))CuSO4+CuO+Fe2O3+3SO2
②4FeS2+11O2eq \(=====,\s\up7(高温))2Fe2O3+8SO2
已知CuFeS2中Cu为+1价,S为-2价。下列说法正确的是( )
A.反应①②中Fe均被氧化
B.反应①中CuSO4和CuO只是氧化产物
C.反应②中Fe2O3和SO2既是氧化产物又是还原产物
D.反应①②生成等物质的量的SO2时,转移的电子数之比为56∶33
第Ⅱ卷(60分)
16.(10分)(1) 某无色透明溶液可能存在Na+、Fe3+、Ba2+、NO3-、CO32-、
HCO3-、SO42-中的几种离子,现有如下操作:
Ⅰ、取适量该溶液加入CaCl2溶液无沉淀,继续滴加盐酸产生无色无味的气体。
Ⅱ、另取该溶液滴加一定量的NaOH溶液有白色沉淀生成。
试回答下列问题:
该溶液中一定存在的离子有_____________,一定不存在的离子_____________。用离子方程式表示操作Ⅱ的实验现象____________________________。
(2)下列各项中的两种物质在溶液中的反应,可用同一离子方程式表示的是 ,请写出该离子反应方程式:_____________________________________________。
A、硫酸氢钠和少量氢氧化钡溶液、硫酸和氢氧化钡溶液
B、纯碱溶液和盐酸、石灰石和硫酸
C、烧碱溶液和醋酸溶液、盐酸和澄清石灰水
D、碳酸铵溶液和氢氧化钠溶液、碳酸铵溶液和氢氧化钙溶液、
17.(9分)氯是海水中含量最丰富的元素,氯的单质及其化合物在生成、生活领域应用广泛。
自来水厂常用液氯进行杀菌消毒。氯气溶于水发生的可逆反应为
(用离子方程式表示)。
用液氯消毒会产生微量有机氯代物,危害人体健康,可以使用二氧化氯(ClO2)代替液氯。工业上以二硫化亚铁(FeS2)、氯酸钠(NaClO3)和硫酸溶液混合制备二氧化氯气体。已知黄铁矿中的硫元素最终氧化成,写出制备二氧化氯的离子方程式 。
生产漂白粉工厂的主要设备是氯化塔,塔从上到下分为四层,右图为生产流程示意图。生产漂白粉反应的化学方程式为 。实际生产中,将石灰乳(含有3%-6%水分的熟石灰)从塔顶喷洒而下,氯气从塔的最底层通入。这样加料的目的是 。
18.(16分)Ⅰ.下列实验装置与实验操作正确的是
П.实验室里需要纯净的氯化钠溶液,但现在只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:
如果此方案正确,那么
(1)操作①加热可选择______________仪器,加热后产生的气体有刺激气味,写出反应的化学方程式
(2)操作②BaCl2溶液是否可改为加硝酸钡溶液?为什么?
(3)操作③加Na2CO3的目的是____________________________________
(4)操作④加热煮沸的目的是_______________________________________________。
(5)纯净的NaCl溶液通过 (操作)得到NaCl固体。用NaCl固体配制0.1 ml·L-1的NaCl溶液,实验中造成所配溶液浓度偏低的原因可能是________。
A.容量瓶中原来含有少量蒸馏水
B.定容摇匀后少量溶液外流
C.向容量瓶中加水定容时眼睛一直仰视刻度线
19.(14分)化学兴趣小组同学想用金属钠和空气制备纯度较高的Na2O2(N2不与金属钠反应),可利用的装置如下。回答下列问题:
(1)装置Ⅳ中盛放的药品是 ,若没有该装置可能导致生成的Na2O2中含有碳酸钠,其反应方程式为 。
(2)若规定气体的气流方向从左到右,各仪器接口的标号字母(a、b……)顺序:空气进入
(3)装置Ⅱ的作用是 。
(4)某学习小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①使酚酞溶液变红是因为 红色褪去的可能原因是 。
②加入MnO2反应的化学方程式为
20.(11分)(1)纯净的过氧化钙(CaO2)是一种新型水产养殖增氧剂,常用于鲜活水产品的运输,可以起到杀菌、解酸(吸收二氧化碳)、防腐、供氧的作用。
分别写出供氧、解酸(吸收二氧化碳)的化学方程式:_________________________、
____________________________。
(2)现有某过氧化钙(CaO2)样品,带有结晶水,含有CaO杂质。
a. 称取5.42 g过氧化钙样品,灼烧时发生如下反应:2(CaO2·xH2O)eq \(=====,\s\up7(高温))2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL,则该样品中CaO2的物质的量为________。
b. 另取同一样品5.42 g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中的Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 7.0 g。
①样品中CaO的质量为____________________。
②样品中CaO2·xH2O中的x为____________。实验现象
分析或结论
A
新制氯水放置数天后pH将增大
氯化氢具有挥发性,酸性减弱
B
液氯滴到干燥的有色布条上,有色布条褪色
液氯中的次氯酸具有漂白性
C
漂白粉长时间放置,失去漂白、杀菌能力
漂白粉与空气中的CO2反应,生成HClO, HClO分解
D
氯气将鲜花漂白
氯气有漂白性
高一化学期中答案
选择40分
除标注外,每空2分,共60分
16 (10分)
(1)Ba2+、HCO3- Fe3+、CO32-、SO42-
HCO3-+ OH-= CO32-+ H2O、Ba2++ CO32-= BaCO3↓
(2)A 、Ba2++ SO42-+2 OH-+2H+= BaSO4↓+2 H2O
(16分)Ⅰ④⑥
П(1) 坩埚 NH4HCO3==NH3↑+CO2↑+H2O
(2)不行,改用Ba(NO3)2溶液会引入新的杂质离子,以后操作中无法除去。
(3)除去过量的Ba2+ (4)除去溶解在溶液中CO2和HCl
(5)蒸发结晶 C
19.(14分)(1) NaOH溶液 , 2Na2O2+2CO2===2Na2CO3+O2
(2)h, g ,f , e , a , b , c ,d
(3) 防止空气中的水蒸气和二氧化碳进入装置Ⅰ
(4) ①过氧化钠和水反应生成氢氧化钠 反应生成的H2O2具有漂白作用(合理即可)
② 2H2O2eq \(=====,\s\up7(MnO2))2H2O+O2↑
20.(11分)
(1)2CaO2+2H2O===2Ca(OH)2+O2↑
Ca(OH)2+CO2===CaCO3↓+H2O
(2)0.06 ml 0.56 g 0.5(3分)
题号
1
2
3
4
5
6
7
8
9
10
答案
D
A
B
D
A
C
D
A
C
C
题号
11
12
13
14
15
答案
C
BD
D
AB
CD
山东省青岛市第五十八中学2023-2024学年高一上学期期中考试化学试卷含答案: 这是一份山东省青岛市第五十八中学2023-2024学年高一上学期期中考试化学试卷含答案,共14页。试卷主要包含了本试卷分第I卷和第II卷两部分,设是阿伏加德罗常数的值,下列离子方程式正确的是,是有机合成中用途很广泛的物质等内容,欢迎下载使用。
北京市西城区第五十六中学2023-2024学年高一上学期期中考试化学试题含答案: 这是一份北京市西城区第五十六中学2023-2024学年高一上学期期中考试化学试题含答案,共14页。试卷主要包含了 下列说法正确的是, 下列物质中,不属于电解质的是等内容,欢迎下载使用。
北京市西城区第五十六中学2023-2024学年高一上学期期中考试化学试题(含答案): 这是一份北京市西城区第五十六中学2023-2024学年高一上学期期中考试化学试题(含答案),文件包含56中高一年级化学试卷docx、56中高一年级化学答案及评分标准docx等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。












