


- 课件 2.1 共价键(2)(键参数-键能、键长、键角)-高中化学选择性必修2(新教材同步课件) 课件 0 次下载
- 课件 2.2 分子的空间结构(1)(分子结构的测定、多样的分子空间结构)-高中化学选择性必修2(新教材同步课件) 课件 0 次下载
- 课件 2.2 分子的空间结构(3)(杂化轨道理论)-高中化学选择性必修2(新教材同步课件) 课件 1 次下载
- 课件 2.3 分子结构与物质的性质(1)(共价键的极性、分子的极性)-高中化学选择性必修2(新教材同步课件) 课件 0 次下载
- 课件 2.3 分子结构与物质的性质(2)(键的极性对化学性质的影响)-高中化学选择性必修2(新教材同步课件) 课件 0 次下载
化学人教版 (2019)第二节 分子的空间结构完整版课件ppt
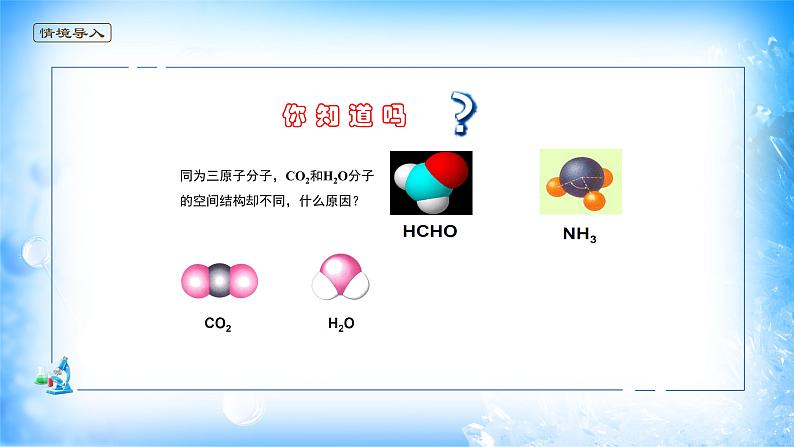
展开同为三原子分子,CO2和H2O分子的空间结构却不同,什么原因?
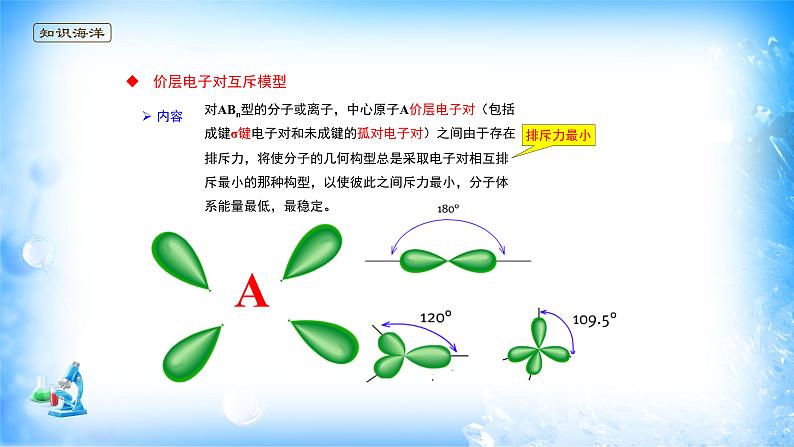
对ABn型的分子或离子,中心原子A价层电子对(包括成键σ键电子对和未成键的孤对电子对)之间由于存在排斥力,将使分子的几何构型总是采取电子对相互排斥最小的那种构型,以使彼此之间斥力最小,分子体系能量最低,最稳定。
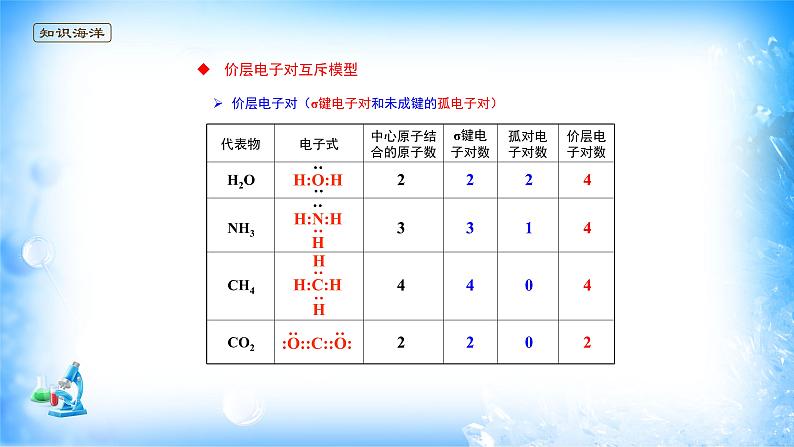
价层电子对(σ键电子对和未成键的孤电子对)
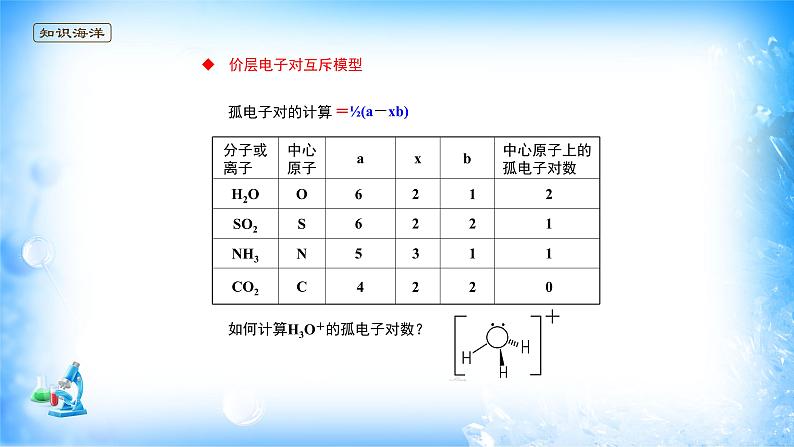
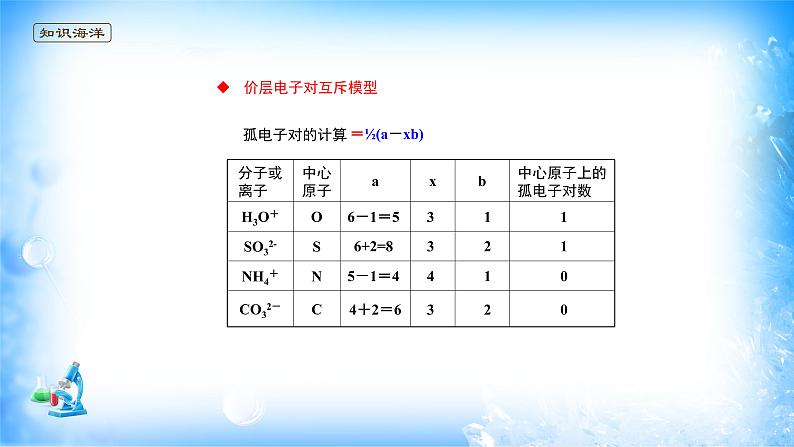
中心原子上的孤电子对数 = ½(a-xb)
=σ键电子对数+孤电子对数
σ键电子对数=与中心原子结合的原子数
如何计算H3O+的孤电子对数?
价层电子对数目:2 3 4VSEPR模型:
价电子对的空间构型即VSEPR模型
VSEPR模型应用——预测分子立体构型
中心原子的孤对电子也要占据中心原子的空间,并与成键电子对互相排斥。推测分子的立体模型必须略去VSEPR模型中的孤电子对
直线形 CO2 BeCl2
平面三角形 BF3 BCl3 SO3
ABn 型分子的VSEPR模型和立体结构
正四面体 CH4、CCl4
三角锥形 NH3、NF3
【例】若ABn型分子的中心原子A上没有未用于形成共价键的孤对电子,运用价层电子对互斥模型,下列说法正确的( )A.若n=2,则分子的立体构型为V形B.若n=3,则分子的立体构型为三角锥形C.若n=4,则分子的立体构型为正四面体形D.以上说法都不正确
【例】用价层电子对互斥模型判断SO3的分子构型( ) A. 正四面体形 B. V形 C. 三角锥形 D. 平面三角形
【例】用价层电子对互斥模型推测下列分子或离子的空间构型:BeCl2____________, SCl2______________,BF3______________, PF3 _______________,NH4+_____________, SO32-_______________。
【例】下列分子和离子中,中心原子价层电子对的几何构型为四面体且分子或离子的空间构型为V形的是( )A.NH4+ B.PH3C.H3O+ D.OF2
【思考】CH4、NH3、H2O VSEPR模型均为四面体形,为什么键角:CH4 > NH3 > H2O
【提示】斥力:孤电子对—成键电子>成键电子—成键电子 ,CH4 中心原子没有孤电子对,NH3 中心原子有一个孤电子对,H2O 中心原子有两个孤电子对,所以键角:CH4 > NH3 > H2O
原理:具有相同价电子数和相同原子数的分子或离子具有相同的结构特征,这一原理称为“等电子原理”
注意:阳离子价电子数=原子的价电子数之和-电荷数阴离子价电子数=原子的价电子数之和+电荷数的绝对值
例如:(1)根据“等电子原理”,仅有第二周期元素组成的共价分子中,互为等电子体的有: 和 ; 和 。(2)根据等电子原理,下列分子的结构最相似的是( ) A. CH4 B. CO2 C. NH4+ D. H2O
(1)互为等电子体的分子或离子的立体构型相同。(2)制造新材料等方面也有重要应用。
【例】下列各组粒子的空间结构相同的是( )①NH3和H2O;②NH4+和H3O+;③NH3和H3O+;④O3和SO2;⑤CO2和BeCl2A. 全部 B. ① ② ③ ⑤ C. ③ ④ ⑤ D. ② ⑤
【例】根据已知的一些分子的结构推测另一些与它等电子的微粒的立体构型,并推测其物理性质。硅和锗是良好的半导体材料,它们的等电子体磷化铝(AlP)和砷化镓(GaAs)也是很好的半导体材料;
中心原子上的孤对电子数目
人教版 (2019)选择性必修2第二节 分子的空间结构示范课课件ppt: 这是一份人教版 (2019)选择性必修2第二节 分子的空间结构示范课课件ppt,共47页。
高中化学苏教版 (2019)选择性必修2专题4 分子空间结构与物质性质第一单元 分子的空间结构说课ppt课件: 这是一份高中化学苏教版 (2019)选择性必修2专题4 分子空间结构与物质性质第一单元 分子的空间结构说课ppt课件,共18页。PPT课件主要包含了H2O,CO2,HCHO,NH3,形形色色的分子,五原子分子立体结构,最常见的是正四面体,CH4,价层互斥理论,孤电子对的计算等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修2第二节 分子的空间结构优质习题ppt课件: 这是一份高中化学人教版 (2019)选择性必修2第二节 分子的空间结构优质习题ppt课件,共31页。PPT课件主要包含了预测分子的空间构型,如何计算价层电子对数,½a-xb,课堂小结等内容,欢迎下载使用。













