

江苏省连云港市赣榆智贤中学2022-2023学年高二上学期第一次学情检测化学试题(含答案)
展开赣榆智贤中学高二年级第一学期第一次学情检测
化学试题
一、单选题(共14小题,14*3=42分,每小题只有1个选项符合题意)
1.某温度下,在恒容密闭容器中加入一定量X,发生反应2X(s)Y (s)+Z(g),一段时间后达到平衡。下列说法错误的是
A.升高温度,若c(Z)增大,则△H>0
B.加入一定量Z,达新平衡后m(Y)减小
C.加入一定量X,达新平衡后c(Z)增大
D.加入一定量氩气,平衡不移动
2.已知反应X(g)+3Y(g) ⇌2Z(g) △H的能量变化如下图所示。下列说法正确的是
A.△H= E2- E1 B.更换高效催化剂,E3不变
C.恒压下充入一定量的氦气n(Z)减少 D.压缩容器,c(X)减小
3.在密闭容器发生下列反应aA(g)⇌cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
A.a<c+d B.平衡向正反应方向移动
C.D的体积分数变大 D.A的转化率变大
4.某温度下,在密闭容器中发生反应HCHO(g)+H2(g)⇌CH3OH(g) ΔH = -85.2kJ·mol-1,反应达到平衡后,改变某条件,下列示意图正确的是
A. B.
C. D.
5.已知在制备高纯硅的过程中发生反应:
。一定条件下,在2L的密闭容器中充入一定量反应物进行该反应,下列有关说法正确的是
A.升温可提高SiHCl3的产率
B.平衡后加压(缩小容器体积),化学平衡逆向移动
C.向容器中加入Si,可使SiCl4的转化率增大
D.该反应的平衡常数
6.已知反应在四种不同情况下的反应速率分别如下:
①v(A)=0.1 mol·L-1·min-1
②v(B)=0.15 mol·L-1·min-1
③
④v(D=0.1 mol·L-1·min-1
则该反应进行速率快慢顺序正确的是
A.①>②>③>④ B.②>①=④>③
C.③>①>②>④ D.④>③>①>②
7.二甲醚()是一种极具发展潜力的有机化工产品和洁净燃料。加氢制二甲醚的反应体系中,主要发生反应的热化学方程式为
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
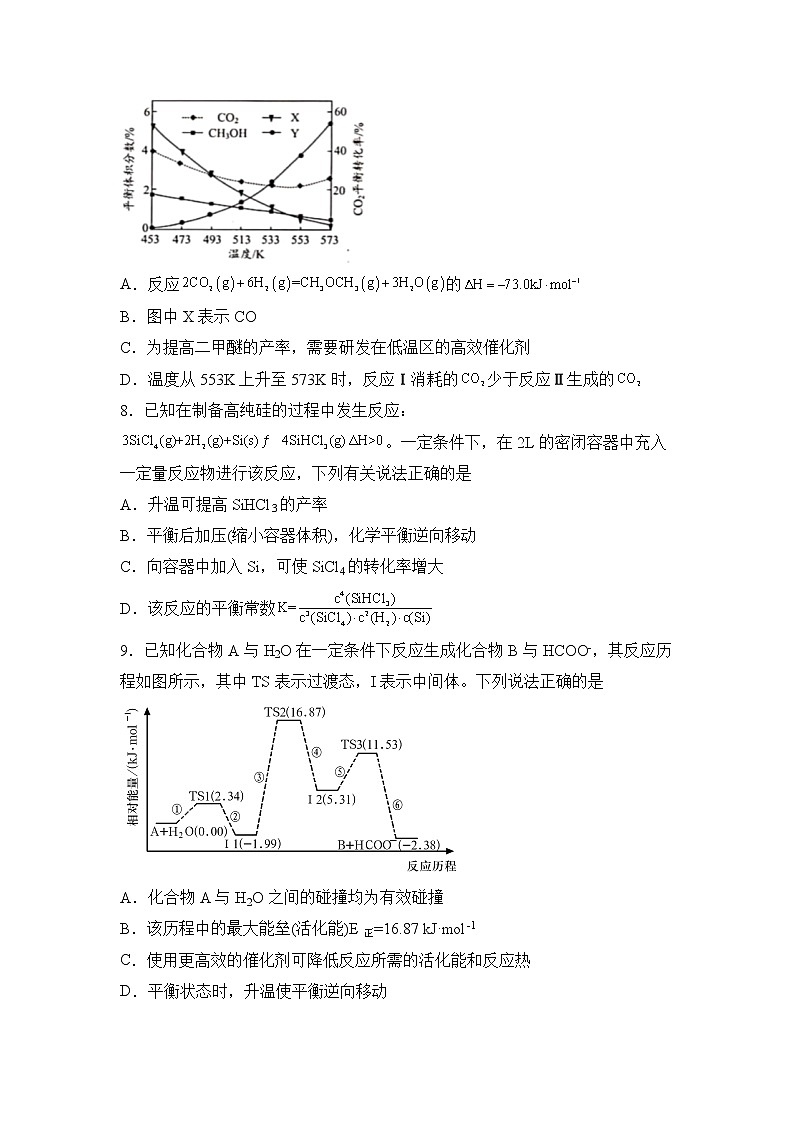
在2MPa,起始投料时,的平衡转化率及CO、、的平衡体积分数随温度变化如图所示。下列有关说法正确的是
A.反应的
B.图中X表示CO
C.为提高二甲醚的产率,需要研发在低温区的高效催化剂
D.温度从553K上升至573K时,反应Ⅰ消耗的少于反应Ⅱ生成的
8.已知在制备高纯硅的过程中发生反应:
。一定条件下,在2L的密闭容器中充入一定量反应物进行该反应,下列有关说法正确的是
A.升温可提高SiHCl3的产率
B.平衡后加压(缩小容器体积),化学平衡逆向移动
C.向容器中加入Si,可使SiCl4的转化率增大
D.该反应的平衡常数
9.已知化合物A与H2O在一定条件下反应生成化合物B与HCOO-,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是
A.化合物A与H2O之间的碰撞均为有效碰撞
B.该历程中的最大能垒(活化能)E正=16.87 kJ·mol-1
C.使用更高效的催化剂可降低反应所需的活化能和反应热
D.平衡状态时,升温使平衡逆向移动
10.某温度时,在催化剂作用下,2 L恒容密闭容器中发生反应I2(g)+H2(g)2HI(g),部分数据如表:
t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
n(HI)/mol | 0 | 0.18 | 0.35 | 0.50 | 0.62 |
则2~6 min内,以H2的物质的量浓度变化表示的反应速率为
A.0.02 mol•L-1•min-1 B.0.04 mol•L-1•min-1
C.0.08 mol•L-1•min-1 D.0.16 mol•L-1•min-1
11.在容积不变的密闭容器中发生反应:CO(g)+H2O(g)CO2(g)+H2(g) ΔH<0,830℃时反应的平衡常数是1.0,下列说法正确的是
A.容器内的压强不变时,说明反应达到平衡状态
B.若平衡时移走CO2,则平衡向正反应方向移动,化学反应速率加快
C.830℃时,充入0.1molCO和0.3molH2O保持温度不变,CO平衡转化率为75%
D.1000℃时,某时刻CO2、H2、CO和H2O的浓度均为0.05mol/L,此时平衡向正反应方向移动
12.一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇:CO(g)+2H2(g)CH3OH(g)。如图是该反应在不同温度下CO的转化率随时间变化的曲线。下列判断正确的是
A.T1>T2
B.该反应的ΔH>0
C.T1时的平衡常数K1>T2时的平衡常数K2
D.T1时的平衡常数K1<T2时的平衡常数K2
13.在2L的密闭容器中,,将2molA气体和1molB气体在反应器中反应,测定A的转化率与温度的关系如实线图所示(图中虚线表示相同条件下A的平衡转化率随温度的变化)。下列说法正确的是
A.反应的
B.X点的化学平衡常数大于Y点的化学平衡常数
C.图中Y点v(正)>v(逆)
D.图中Z点,增加B的浓度不能提高A的转化率
14.铁的配合物离子(用表示)催化某反应的一种反应机理如下图所示,下列说法不正确的是
A.该过程的总反应为
B.增大HCOO-浓度有利于反应Ⅰ→Ⅱ速率加快
C.增大H+浓度有利于反应Ⅲ→Ⅳ速率加快
D.该催化循环中元素的化合价发生了变化
二、填空题(共3小题)
15.在一密闭容器中发生反应N2+3H2=2NH3 ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示。
回答下列问题:
(1)处于平衡状态的时间段是___________(填字母,下同)。
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)判断t1、t3、t4时刻分别改变的一个条件。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
t1时刻___________;t3时刻___________;t4时刻___________。
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是___________。
A.t0~t1 B.t2~t3
C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线______。
16.运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气:C(s)+H2O(g)⇌H2(g)+CO(g) ΔH=+131.3kJ·mol-1,ΔS=+133.7J·mol-1·K-1
①该反应在低温下___________(填“能”或“不能”)自发进行。
②写出该反应的平衡常数表达式___________。
(2)已知在400℃时,N2(g)+3H2(g)⇌2NH3(g)的K=0.5。
①400℃时,2NH3(g)⇌N2(g)+3H2(g)的K'=___________(填数值)。
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正___________v(N2)逆(填“>”“<”“=”或“不能确定”)。
③若在恒温下将容器的容积缩小到原来的二分之一,则合成氨反应的平衡___________移动(填“向左”、“向右”或“不”);反应的∆H___________(填“增大”、“减小”或“不变”)。
(3)水煤气转化反应CO(g)+H2O(g) ⇌CO2(g)+H2(g)在一定温度下达到化学平衡。现将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下两组数据:
实验编号 | 温度/℃ | 起始量)/mol | 平衡量)/mol | 达到平衡所需时间)/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 5 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
①平衡常数K(650℃)___________K(900℃)(填“大于”,“小于”或“等于”)
②若将实验2中CO和H2O的物质的量加倍,则平衡时H2的物质的量浓度为___________。
17.恒温恒容下,将2 mol红棕色气体A和1.5 mol无色气体B通入体积为1 L的密闭容器中发生如下反应:,2 min时反应达到平衡状态,此时剩余1.1 mol B,并测得C的浓度为1.2 mol/L。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为_______mol/(L·min)
(2)x=_______;A的转化率与B的转化率之比为_______
(3)写出该温度下的平衡常数表达式_______(用相关字母表示),数值_______
(4)向平衡后的容器中继续充入0.8 molA(g)、0.9 molB(g)、0.8 molC(g)、1.2mol D(s),此时,v(正)_______v(逆)。(填“>”、“=”或“<”)
赣榆智贤中学高二年级化学试题答案
一.选择题
1.C 2C . 3 A . 4.C 5A . 6. C 7. C 8. A 9. D 10 A
.11. C 12. C 13.B 14.D
二.填空题
15. ACDF C E B A
16.
(1) 不能 K=
(2) 2 = 向右 不变
(3) 大于 0.4mol·L-1
17.(1)0.6
(2) 3 3:2
(3) K= 1.09
(4)>
2022-2023学年江苏省连云港市赣榆智贤中学高一3月阶段检测化学试题: 这是一份2022-2023学年江苏省连云港市赣榆智贤中学高一3月阶段检测化学试题,文件包含江苏省连云港市赣榆智贤中学高一3月阶段检测化学试题原卷版docx、江苏省连云港市赣榆智贤中学高一3月阶段检测化学试题解析版docx等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。
江苏省连云港市高级中学2022-2023学年高二下学期6月第二次学情检测化学试题(Word版含答案): 这是一份江苏省连云港市高级中学2022-2023学年高二下学期6月第二次学情检测化学试题(Word版含答案),共13页。试卷主要包含了单项选择题,非选择题等内容,欢迎下载使用。
江苏省连云港市赣榆智贤中学2022-2023学年高二化学上学期第一次学情检测试题(Word版附解析): 这是一份江苏省连云港市赣榆智贤中学2022-2023学年高二化学上学期第一次学情检测试题(Word版附解析),共22页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。












