

2019-2020学年湖南省长沙市长郡中学高一(上)期中化学试卷
展开2019-2020学年湖南省长沙市长郡中学高一(上)期中化学试卷
一、选择题(共16小题,每小题3分,满分48分)
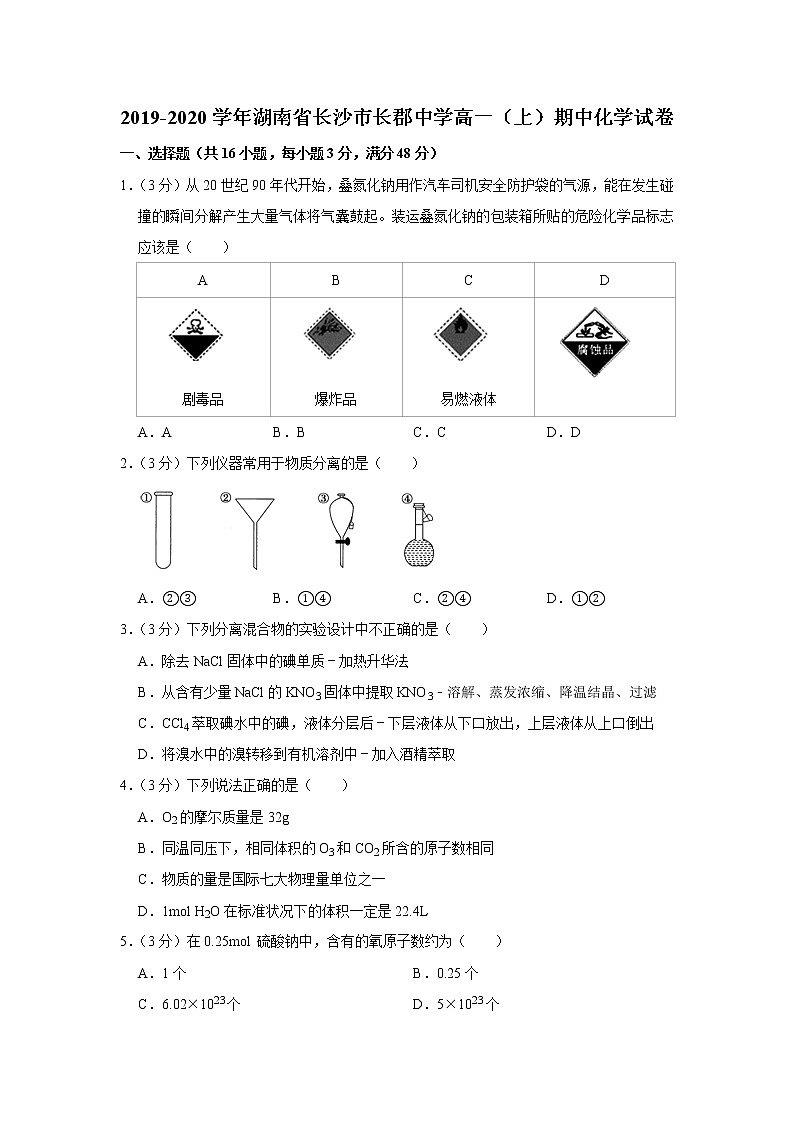
1.(3分)从20世纪90年代开始,叠氮化钠用作汽车司机安全防护袋的气源,能在发生碰撞的瞬间分解产生大量气体将气囊鼓起。装运叠氮化钠的包装箱所贴的危险化学品标志应该是( )
A | B | C | D |
剧毒品 | 爆炸品 | 易燃液体 |
A.A B.B C.C D.D
2.(3分)下列仪器常用于物质分离的是( )
A.②③ B.①④ C.②④ D.①②
3.(3分)下列分离混合物的实验设计中不正确的是( )
A.除去NaCl固体中的碘单质﹣加热升华法
B.从含有少量NaCl的KNO3固体中提取KNO3﹣溶解、蒸发浓缩、降温结晶、过滤
C.CCl4萃取碘水中的碘,液体分层后﹣下层液体从下口放出,上层液体从上口倒出
D.将溴水中的溴转移到有机溶剂中﹣加入酒精萃取
4.(3分)下列说法正确的是( )
A.O2的摩尔质量是32g
B.同温同压下,相同体积的O3和CO2所含的原子数相同
C.物质的量是国际七大物理量单位之一
D.1mol H2O在标准状况下的体积一定是22.4L
5.(3分)在0.25mol 硫酸钠中,含有的氧原子数约为( )
A.1个 B.0.25个
C.6.02×1023个 D.5×1023个
6.(3分)下列物质中分子数由少到多的排列顺序是( )
①6g H2;②2mol NH3;③9mL 水(4℃);④22.4L O2(标准状况)。
A.①②④③ B.③④②① C.④②①③ D.③②④①
7.(3分)在下列四种溶液中的 NO3﹣离子浓度与50mL1mol/L的Al(NO3)3 溶液中 NO3﹣离子浓度相等的是( )
A.150mL1mol/L的NaNO3 B.75mL2mol/L的Ca(NO3)2
C.150mL2mol/L的KNO3 D.75mL3mol/L 的NH4 NO3
8.(3分)某氯原子的质量是ag,用NA表示阿伏加德罗常数的值,下列说法正确的是( )
①mg该氯原子的物质的量一定是mol
②该氯原子的摩尔质量是aNAg•mol﹣1
③ag该氯原子所含的质子数是17NA。
A.①③ B.②③ C.①② D.①②③
9.(3分)对下列物质进行的分类正确的是( )
A.纯碱、烧碱均属于碱
B.凡能电离出H+的化合物均属于酸
C.盐类物质一定含有金属阳离子
D.CuSO4•5H2O属于纯净物
10.(3分)下列关于钠的说法中不正确的是( )
A.金属钠和氧气反应,条件不同,产物则不同
B.钠长期放置在空气中,最终将变成碳酸钠
C.钠的化学性质比较活泼,少量的钠可以保存在煤油中
D.当钠着火时可用水扑灭
11.(3分)下列化学反应中,既是离子反应,又是氧化还原反应的是( )
A.2NaOH+H2SO4═Na2SO4+2H2O
B.Fe+H2SO4═FeSO4+H2↑
C.BaCl2+H2SO4═BaSO4↓+2HCl
D.H2+CuOCu+H2O
12.(3分)和下列离子反应方程式相对应的化学方程式正确的是( )
A.Cu2++2OH﹣═Cu(OH)2 CuCO3+2NaOH═Cu(OH)2↓+Na2CO3
B.Ba2++SO42﹣═BaSO4↓ Ba(OH)2+H2SO4═BaSO4↓+2H2O
C.Ag++Cl﹣═AgCl↓ AgNO3+NaCl═AgCl↓+NaNO3
D.Cu+2Ag+═Cu2++2Ag↓ Cu+2AgCl═2Ag+CuCl2
13.(3分)下列各组离子一定能大量共存的是( )
A.在无色溶液中:NH4+,Fe2+,SO42﹣,CO32﹣
B.澄清透明的溶液:MnO4﹣,Al3+,SO42﹣,K+
C.使酚酞溶液变红的溶液:H+,Cl﹣,NO3﹣,Ba2+
D.在pH=1的溶液中:K+,CO32﹣,NO3﹣,HCO3﹣
14.(3分)关于氧化还原反应的说法,正确的是( )
A.物质失去的电子数越多,其还原性越强
B.物质所含元素化合价升高的反应叫还原反应
C.某元素由化合态变为游离态,则它一定被还原
D.置换反应一定属于氧化还原反应
15.(3分)下列对于反应:3NO2+H2O═2HNO3+NO的说法正确的是( )
A.氧化剂与还原剂的质量比为1:2
B.NO2是氧化剂,水是还原剂
C.生成1mol NO则有6mol电子发生转移
D.氧化产物与还原产物的物质的量比为1:2
16.(3分)已知:
①2BrO3﹣+Cl2=Br2+2ClO3﹣;
②5Cl2+I2+6H2O=2HIO3+10HCl;
③ClO3﹣+5Cl﹣+6H+=3Cl2↑+3H2O
下列按物质氧化性顺序由强到弱排列正确的是( )
A.Cl2>BrO3﹣>ClO3﹣>IO3﹣ B.BrO3﹣>ClO3﹣>Cl2>IO3﹣
C.ClO3﹣>BrO3﹣>IO3﹣>Cl2 D.BrO3﹣>Cl2>ClO3﹣>IO3﹣
二、填空题(共4小题,每小题10分,满分42分)
17.(10分)(1)下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置,将A、B、C、D填入适当的空格中
①除去粗盐水中的泥沙: 。
②与海水晒盐原理相似的是 。
③用四氯化碳从碘水中提取碘: 。
④分离CCl4(沸点:76.75℃)和苯(沸点:110.6℃)的混合物(互溶) 。
(2)下列关于物质的检验,说法正确的是 。(填字母代号)
A.待检液加入稀HCl酸化的BaCl2溶液,有白色沉淀生成,则原溶液中一定有SO42﹣存在
B.待检液加入AgNO3溶液,产生白色沉淀,则原溶液中一定有Cl﹣存在
C.待检液加入NaOH溶液并加热,有能使红色石蕊试液变蓝的气体生成,则原溶液中一定有NH4+存在
D.待检液加入盐酸,产生无色无味的气体,则原溶液中一定有CO32﹣存在
18.(12分)现有下列八种物质:①铝;②Ba(OH)2溶液;③蔗糖固体;④稀硫酸;⑤熔融的NaOH;⑥FeCl3饱和溶液;⑦CO2;⑧新制备的氢氧化铁胶体分散系。
(1)上述物质属于非电解质的有 。(填序号)
(2)上述物质能导电且属于电解质的有 。(填序号)
(3)若将⑥滴入下列物质中,能形成⑧的是 。(填字母代号)
A.NaOH浓溶液 B.NaCl浓溶液 C.冷水 D.沸水
(4)可利用哪种效应鉴别⑥和⑧: 。
(5)⑦和足量②反应的离子方程式为 。
(6)①与⑤的水溶液反应的离子方程式为 。
19.(10分)重铬酸钾(K2Cr2O7)和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O。
(1)浓盐酸在反应中表现出来的性质是 (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)Cl2是 (“氧化”或“还原”)产物;产生0.1molCl2,则转移电子的物质的量为 mol。
(3)从铬元素(Cr)的化合价上判断,Cr、CrCl3、K2Cr2O7三种物质中的铬元素既表现氧化性又表现还原性的是 (写化学式,下同)。
(4)已知氯气有毒,与水反应生成两种酸。实验室制备氯气可选用 溶液进行尾气处理。
20.(10分)实验室常用浓盐酸的质量分数为36.5%,密度为1.20g•cm﹣3。
(1)此盐酸的物质的量浓度为 。
(2)需要95mL 3.00mol•L﹣1的盐酸,配制时需以上浓盐酸的体积为 mL。
(3)上述实验中所用到的玻璃仪器有烧杯、玻璃棒、量筒以及 。(两种仪器)
(4)用浓盐酸配制3.00mol•L﹣1稀盐酸,操作步骤的正确顺序是 。(填字母代号)
a.计算需要浓盐酸的体积
b.用量筒量取浓盐酸
c.将烧杯中的溶液注入所需容积的容量瓶中,并用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶
d.把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却
e.盖好瓶塞,反复上下颠倒,摇匀
f.继续向容量瓶中加蒸馏水至刻度线下1~2cm处,改用某仪器小心滴加蒸馏水至凹液面与刻度线相平
(5)下列操作使溶液物质的量浓度偏高的是: 。
A.量取浓盐酸时仰视刻度线
B.容量瓶洗净后未经干燥处理
C.未冷却至室温就转移定容
D.没有将洗涤液转移到容量瓶中
E.定容时俯视刻度线
F.摇匀后立即观察,发现溶液未达到刻度线,再加几滴蒸馏水至刻度线
三、计算题(共1小题,满分10分)
21.(10分)完成下列有关物质的量的计算
(1)1.204×1023个CH4分子的物质的量是 mol。
(2)标准状况下,34g NH3的体积是 L。
(3)含有相同氧原子数的SO2和SO3,其分子的质量比为 。
(4)标准状况下,aL HCl气体溶于水配制成bL溶液,其物质的量浓度为 mol/L。
(5)3.6g碳在一定量的氧气中完全燃烧,反应后生成CO和CO2混合气体的平均摩尔质量是32g/mol,则生成的CO的质量是 g。
2019-2020学年湖南省长沙市长郡中学高一(上)期中化学试卷
参考答案
一、选择题(共16小题,每小题3分,满分48分)
1.B; 2.A; 3.D; 4.B; 5.C; 6.B; 7.D; 8.C; 9.D; 10.D; 11.B; 12.C; 13.B; 14.D; 15.A; 16.B;
二、填空题(共4小题,每小题10分,满分42分)
17.B; D; C; A; C; 18.③⑦; ⑤; D; 丁达尔效应; CO2+Ba2++2OH﹣=BaCO3↓+H2O; 2Al+2OH﹣+2H2O=2AlO2﹣+3H2↑; 19.②; 氧化; 0.2; CrCl3; 氢氧化钠; 20.12mol/L; 25.0; 100mL容量瓶、胶头滴管; abdcfe; ACE;
三、计算题(共1小题,满分10分)
21.0.2; 44.8; 6:5; ; 6.3;
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布
日期:2021/4/8 10:15:48;用户:刘然;邮箱:15810579892;学号:39289586
2023-2024学年湖南省长沙市长郡重点中学高二(上)入学化学试卷(含解析): 这是一份2023-2024学年湖南省长沙市长郡重点中学高二(上)入学化学试卷(含解析),共35页。试卷主要包含了单选题,流程题,实验题,简答题等内容,欢迎下载使用。
2021-2022学年湖南省长沙市长郡中学高二(上)期中考试化学试卷(含答案解析): 这是一份2021-2022学年湖南省长沙市长郡中学高二(上)期中考试化学试卷(含答案解析),共17页。试卷主要包含了8kJ/ml,6kJ/ml,【答案】B,【答案】D,【答案】C等内容,欢迎下载使用。
2019-2020学年湖南省长沙市长郡中学高一(上)期末化学试卷: 这是一份2019-2020学年湖南省长沙市长郡中学高一(上)期末化学试卷,共7页。












