






- 第2讲 物质的量浓度及其计算 课件 课件 1 次下载
- 练案[2] 第一章 第2讲 物质的量浓度及其计算 试卷 1 次下载
- 练案[3] 第二章 第3讲 物质的组成、性质和分类 试卷 0 次下载
- 第4讲 离子反应 课件 课件 0 次下载
- 练案[4] 第二章 第4讲 离子反应 试卷 0 次下载
第3讲 物质的组成、性质和分类
展开第3讲 物质的组成、性质和分类
1.物质的组成(1)元素的存在形态①游离态:元素以________形式存在的状态。②化合态:元素以__________形式存在的状态。
考点一 物质的组成与分类
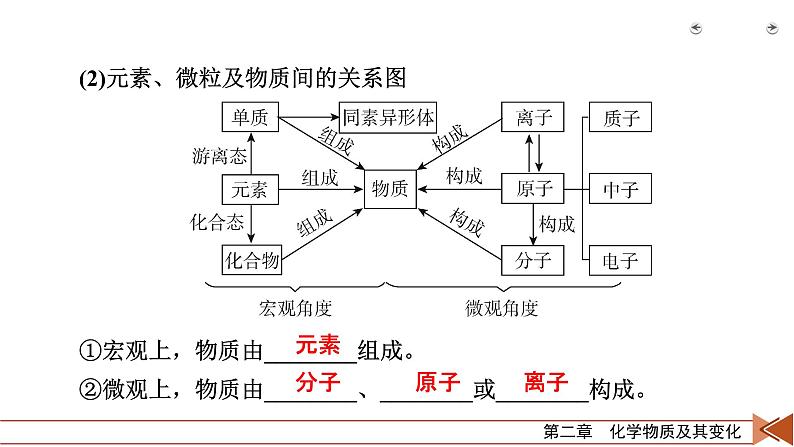
(2)元素、微粒及物质间的关系图①宏观上,物质由________组成。②微观上,物质由________、________或________构成。
(4)深刻理解几组概念
只含一种元素的物质不一定是单质,如O2和O3的混合物、金刚石与石墨的混合物等。只含一种元素的纯净物才是单质。
2.物质的分类分类的定义:把事物按照__________________进行归类分组的一种方法。物质的分类方法(1)树状分类法用单一分类法分类后,对分出的同类事物按一定标准再分类,形成有一定从属关系的不同等级系统的一种分类方法,形象的称为树状分类法。
A.明确分类标准是对物质正确树状分类的关键
B.树状分类法在无机化合物分类中的应用
①碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物,如Mn2O7为酸性氧化物。②酸性氧化物不一定是非金属氧化物,如Mn2O7是酸性氧化物;非金属氧化物也不一定是酸性氧化物,如CO、NO都不是酸性氧化物。③酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱,如SiO2、Fe2O3都不能与水反应。④能与酸反应生成盐和水的氧化物不一定是碱性氧化物,如Na2O2不是碱性氧化物。
(2)交叉分类法根据不同的分类标准对同一事物进行分类的一种分类方法。指出下列物质分类的标准。
(2)常见的物理变化、化学变化
(3)物理变化和化学变化的判断方法
(4)常见的易混淆物质变化①化学变化:结晶水合物的脱水、同素异形体间的转化、蛋白质的变性、电解、水解、煤的干馏、气化和液化,石油的裂化与裂解等。②物理变化:焰色反应、活性炭的吸附、盐析、蒸馏、升华、潮解等。
4.物质转化及其规律(1)化学反应的分类
(2)单质、氧化物、酸、碱和盐的转化关系转化示意图
请写出①②③④⑦的化学方程式,并注明反应类型:①_____________________,____________;②___________________________,____________;③_________________________________________,______________;④_____________________________,____________;⑤______________________________________;______________
2Ca+O2═══2CaO
CaO+H2O═══Ca(OH)2
Ca(OH)2+Na2CO3═══CaCO3↓+2NaOH
Fe+2HCl═══FeCl2+H2↑
CaCO3+2HCl═══CaCl2+H2O+CO2↑
思考:金属和盐反应时,是否一定生成金属和盐?请举例说明。提示:不一定。如:Fe+2FeCl3═══3FeCl2、Cu+2FeCl3═══CuCl2+2FeCl2。
1.判断正误,正确的打“√”,错误的打“×”。(1)只含一种元素的物质一定是纯净物,只用同一化学式表示的物质也一定是纯净物。( )(2)与水反应可生成酸的氧化物都是酸性氧化物。( )(3)既能与酸反应又能与碱反应的物质是两性氧化物或是两性氢氧化物。( )(4)232Th转化成233U是化学变化。( )
(5)用铂丝蘸取Na2SO4、Na2CO3、NaCl溶液进行焰色反应是化学变化。( )(6)Na2CO3·10H2O的风化、NaOH的潮解都属于物理变化。( )(7)煤的气化、液化、干馏都是物理变化。( )(8)臭氧变成氧气是物理变化。( )(9)冰水混合物属于化合物,高分子化合物属于混合物。( )(10)胆矾(CuSO4·5H2O)、明矾[ KAl(SO4)2·12H2O]均属于混合物。( )
× × × × √ ×
(11)NaHSO4、NaHCO3都属于酸式盐,溶液都呈酸性。( )(12)利用NH4Cl溶液除铁锈是化学变化。( )(13)SiO2既能与NaOH溶液反应又能与氢氟酸反应,因此是两性氧化物。( )(14)石油的分馏和煤的气化均属于化学变化。( )[提示] 石油的分馏是物理变化,煤的气化是化学变化。(15)硅胶、P2O5、CaCl2·6H2O均可用作食品干燥剂。( )[提示] CaCl2·6H2O不能作食品干燥剂。
(16)通过化学变化可以直接将水转变为汽油。( )[提示] 石油中含有碳、氢元素,水中含有氢、氧元素,二者无法直接转化。(17)Fe与H+、Cu2+、S、I2反应不能生成Fe3+。( )[提示] H+、Cu2+、S、I2均为弱氧化剂,只能将铁氧化成+2价。(18)从海水中提取物质都必须通过化学反应才能实现。( )[提示] 海水淡化、海水晒盐都是物理变化。
3.深度思考:无机化合物可根据其组成和性质进行分类:(1)如图所示的物质分类方法名称是______________。
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
(3)写出⑦转化为⑤的化学方程式:_________________________________。(4)呼吸面具中用⑧作为O2来源的反应原理为:___________________________________,___________________________________。(5)实验室制备⑦常用_________和__________反应,检验该气体的方法是_________________________________________________。
CO2+2NaOH═══Na2CO3+H2O
2Na2O2+2CO2═══2Na2CO3+O2
2Na2O2+2H2O═══4NaOH+O2↑
通入澄清石灰水中,若变浑浊,则生成的气体为CO2
微考点1 物质分类与性质(1)“春蚕到死丝方尽,蜡炬成灰泪始干”是唐代诗人李商隐的著名诗句,下列关于该诗句中所涉及物质的说法错误的是( )A.蚕丝的主要成分是蛋白质B.蚕丝属于天然高分子材料C.“蜡炬成灰”过程中发生了氧化反应D.古代的蜡是高级脂肪酸酯,属于高分子聚合物
[解析] A项,蚕丝的主要成分是蛋白质,蛋白质属于天然高分子化合物,蚕丝属于天然高分子材料,A、B两项正确;“蜡炬成灰”过程中发生了燃烧反应,燃烧反应属于氧化反应,C项正确;古代的蜡烛多是由动物油脂制造,动物油脂属于高级脂肪酸酯,但高级脂肪酸酯不属于高分子聚合物,D项错误。
(2)(2022·陕西西安模拟)下列说法正确的是( )A.蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖B.FeO、Al2O3、NO2分别属于碱性氧化物、两性氧化物、酸性氧化物C.乙醇、氯化银和乙酸分别属于非电解质、强电解质和弱电解质D.天然气、沼气和水煤气分别属于可再生能源、二次能源和化石能源
[解析] A.蚕丝、羊毛属于蛋白质,淀粉属于多糖,故A错误;B.酸性氧化物与碱反应只生成盐和水,与水反应只生成酸,而二氧化氮与水反应生成硝酸和一氧化氮,即NO2不属于酸性氧化物,故B错误;C.乙醇在熔融状态下和水溶液中不能导电,属于非电解质,AgCl虽然难溶于水,但溶于水的部分完全电离,属于强电解质,醋酸在溶液中不能完全电离,属于弱电解质,故C正确;D.天然气属于化石能源,不能再生,沼气属于可再生能源,通过微生物的发酵可以生成,水煤气属于二次能源,工业上用碳和水反应生成,故D错误。
[解析] 含有两种或两种以上成分的物质属于混合物,A项物质由两种单质组成,故属于混合物。
(2)(2021·广东,2,2分)广东有众多国家级非物质文化遗产,如广东剪纸、粤绣、潮汕工夫茶艺和香云纱染整技艺等。下列说法不正确的是( )A.广东剪纸的裁剪过程不涉及化学变化B.冲泡工夫茶时茶香四溢,体现了分子是运动的C.染整技艺中去除丝胶所用的纯碱水溶液属于纯净物D.制作粤绣所用的植物纤维布含有天然高分子化合物[解析] C项,纯碱水溶液是纯碱与水组成的混合物,并非纯净物,错误。
[易错易混] 植物纤维主要有棉、麻等,动物纤维有毛、蚕丝等,它们都含有天然高分子化合物。合成纤维有涤纶、锦纶等。
微考点2 物质的性质与转化(1)(2021·广东,6,2分)劳动成就梦想。下列劳动项目与所述的化学知识没有关联的是( )
[解析] A项,84消毒液的有效成分为NaClO,具有强氧化性,可用来杀菌消毒,正确;B项,厨余垃圾中含有蛋白质、油脂、纤维素等物质,富含N、P、K等元素,可用于制肥料,正确;C项,油脂属于酯类物质,油脂在碱性条件下水解生成高级脂肪酸盐(肥皂的成分),正确;D项,CH3COOH与水垢中的CaCO3反应生成可溶性的(CH3COO)2Ca,所用的化学知识与乙醇在氧化剂的作用下被氧化为乙酸没有关系,故选D。
(2)(2021·湖南,1,3分)下列有关湘江流域的治理和生态修复的措施中,没有涉及化学变化的是( )A.定期清淤,疏通河道B.化工企业“三废”处理后,达标排放C.利用微生物降解水域中的有毒有害物质D.河道中的垃圾回收分类后,进行无害化处理
[解析] A项,清淤只是物质的空间移动,不涉及化学变化,符合题意;B项,“三废”中含有害物质,必须把有害物质转化为无害物质才能排放,涉及化学变化,不符合题意;C项,利用微生物把有毒有害物质降解为无毒无害物质,涉及化学变化,不符合题意;D项,无害化处理是通过物理、化学或生物的方法将有毒有害物质转化为无毒无害物质,涉及化学变化,不符合题意。
物质间转化的5个常见易错点S燃烧不能直接生成SO3而是生成SO2。Al2O3、SiO2、Fe2O3与H2O不反应,不能直接转化为Al(OH)3、H2SiO3、Fe(OH)3。NH3催化氧化不能直接生成NO2。Fe与Cl2反应不能直接生成FeCl2。Fe与H+、Cu2+、S、I2反应不能直接生成Fe3+。
[解析] 根据转化关系可知,A应是非金属单质,A能被氧气氧化生成C,C能被氧化生成D,则A在氧化物中显不同价态,E有强酸性和强氧化性,则A中元素是非金属性较强的元素。氯气和氢气反应生成氯化氢,氯化氢和氧气不反应,A项错误;碳和氧气反应生成一氧化碳,CO和O2反应生成二氧化碳,CO2和H2O反应生成碳酸,但碳酸是弱酸,B项错误;N2和H2反应生成NH3,NH3和O2反应生成一氧化氮,氮气和氧气反应生成一氧化氮,NO和O2反应生成NO2,NO2和H2O反应生成硝酸,硝酸是强酸且具有强氧化性,C项正确;硅和氧气反应时,无论氧气是否过量都生成SiO2,且SiO2与H2O不反应且硅酸是弱酸,D项错误。
(2)(2022·山东滨州高三检测)下列说法在一定条件下可以实现的是( )①酸性氧化物与碱发生反应 ②弱酸与盐溶液反应可以生成强酸 ③没有水生成,也没有沉淀和气体生成的复分解反应 ④两种酸溶液充分反应后的溶液体系为中性 ⑤有单质参加的非氧化还原反应 ⑥两种氧化物反应的产物有气体A.①②③④⑤⑥B.②④⑤⑥C.①②③⑤D.③④⑤⑥
[易错警示] 常考易错的几个物质的转化(1)结晶水合物失去结晶水的过程属于化学变化。(2)浓硫酸的吸水性属于物理性质,脱水性属于化学性质。(3)煤的干馏、煤的气化以及煤的液化都属于化学变化,石油的分馏属于物理变化,石油的裂化和裂解都属于化学变化。(4)同素异形体之间的转化属于化学变化。
1.分散系(1)定义:把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。分散质:分散系中__________的物质;分散剂:分散系中______________的物质。
(2)分类①把分散系分为溶液、胶体和浊液的标准是分散质________________。可用如下方式直观地表示:
(3)理清三种分散系的差异
(1)胶体区别于其他分散系的本质特征是胶体粒子的直径在1~100 nm(即10-9~10-7m)之间,而不是丁达尔效应。(2)胶体具有介稳性的主要原因是胶体粒子可以通过吸附带电粒子而带有电荷,且同种电荷相互排斥,不易聚集成较大的颗粒。(3)胶体粒子的直径决定了胶体的性质,因胶体粒子较大不能透过半透膜,可用渗析法提纯胶体。
2.胶体(1)胶体的分类①依据分散剂的状态:气溶胶:如______________液溶胶:如_______水溶胶固溶胶:如烟水晶、________玻璃②依据分散质粒子的大小:粒子胶体:如Fe(OH)3胶体;分子胶体:如淀粉溶液、蛋白质溶液。
(2)胶体的性质与应用
(1)丁达尔效应是物理变化而不是化学变化。(2)胶体不带电,胶体中的胶粒能够吸附体系中的带电粒子而使胶粒带电荷,但整个分散系仍呈电中性。
(1)不能用自来水制备Fe(OH)3胶体,因为自来水中有电解质会使胶体发生聚沉,应用蒸馏水。(2)不能过度加热,否则Fe(OH)3胶体会聚沉生成Fe(OH)3沉淀。(3)书写制备胶体的化学方程式时,生成的胶体不加沉淀符号“↓”,应注明“胶体”二字。(4)Fe(OH)3胶体粒子是多个“Fe(OH)3”的集合体,因此,1 ml Fe3+完全水解得到Fe(OH)3胶体粒子数小于NA。
1.判断正误,正确的打“√”,错误的打“×”。(1)稀豆浆、硅酸、氯化铁溶液均为胶体。( )(2)明矾溶于水产生Al(OH)3胶体:Al3++3H2O═══Al(OH)3↓+3H+。( )(3)丁达尔效应是胶体与溶液的本质区别。( )(4)含0.1 ml FeCl3的饱和溶液配制成胶体后,将得到胶体粒子0.1 ml。( )
(5)FeCl3溶液和Fe(OH)3胶体都呈红褐色。( )(6)可用过滤的方法将胶体粒子与分散剂分开。( )(7)沸水中滴加少量饱和FeCl3溶液形成带电的胶体,导电能力增强。( )(8)通过丁达尔效应可以鉴别稀豆浆和氢氧化铁胶体。( )[提示] 稀豆浆属于胶体。
(9)明矾净水时发生了化学及物理变化,能起到杀菌、消毒作用。( )[提示] 明矾净水只是把浑水变为清水,无杀菌消毒的作用,错误。(10)按照分散质和分散剂所处的状态,可分为9种分散系。( )(11)胶体的丁达尔效应是发生了化学变化。( )(12)为除去淀粉溶液中混有的NaCl,可以采取渗析的方法。( )
(13)将Fe(OH)3胶体装入U形管,两端通直流电,与直流电源负极相连的一极颜色变深。( )(14)胶体不一定是液态,胶体的丁达尔效应属于物理变化。( )(15)将1 mL 1 ml·L-1的FeCl3溶液滴入沸水中制备Fe(OH)3胶体,若FeCl3完全水解,则可制得Fe(OH)3胶体粒子少于0.001NA个。( )
2.深度思考:(1)向Fe(OH)3胶体中滴入过量稀硫酸,现象是什么?其原因是什么?(2)胶体与其他分散系的本质区别是什么?怎样提纯胶体?
[提示] (1)先出现红褐色沉淀,后沉淀溶解。开始加入稀硫酸时,胶体发生聚沉生成氢氧化铁沉淀,当酸过量时发生酸碱中和反应沉淀又溶解。(2)胶体粒子的直径在1~100 nm之间,这是胶体区别于其他分散系的本质特征,同时也决定了胶体的性质。由于胶体粒子较大不能透过半透膜,而离子、分子较小可以透过半透膜,可用渗析法将胶体粒子和溶液中的离子、分子分开。
微考点1 胶体的性质与用途(2022·山东潍坊高三检测)胶体在工业生产及日常生活中有着广泛应用。下列事实与胶体性质无关的是( )①土壤中离子的吸附和交换过程,有保肥作用 ②将植物油倒入水中用力搅拌形成油水混合物 ③一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路 ④氢氧化铁胶体中滴入稀硫酸,先看到红褐色沉淀生成而后沉淀溶解 ⑤由肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 ⑥水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 ⑦明矾和FeCl3可用作净水剂 ⑧O3、H2O2均可用于水的净化杀菌A.①④⑧ B.③④⑦ C.②⑤⑧ D.②⑧
[解析] ①土壤胶体中胶粒带有电荷,对离子有吸附和交换作用,可起到保肥的效果;②植物油倒入水中用力搅拌形成的油水混合物属于乳浊液,静置后分层,油层在水层的上面,可以用分液的方法分离;③蛋白质溶液属于胶体,可产生丁达尔效应;④氢氧化铁胶体中滴入稀硫酸(电解质溶液),会发生胶体的聚沉生成氢氧化铁沉淀,继续滴加的稀硫酸能与氢氧化铁发生酸碱中和反应:2Fe(OH)3+3H2SO4═══Fe2(SO4)3+6H2O,沉淀溶解;⑤血液透析的原理是利用渗析净化血液胶体;⑥静电除尘的原理是电泳现象;⑦明矾、FeCl3净水的原理是生成胶体,胶体吸附杂质而净水;⑧O3、H2O2的净水是利用强氧化性氧化细菌蛋白质而杀菌。
[易错警示] (1)胶体不带电荷,胶体粒子(分散质)可能带电荷,但淀粉胶体的胶体粒子不带电荷。(2)胶体属于分散系,是混合物,而很多纳米级物质的微粒直径也是在1~100 nm之间,但不属于胶体,因为这些物质属于纯净物,如纳米铜等。(3)在Fe(OH)3胶体中,Fe(OH)3胶体粒子的数目要远远小于原FeCl3溶液中Fe3+的数目。
〔对点集训1〕 (1)(2022·浙江金华调研)下列关于胶体的说法,正确的是( )A.“霾尘积聚难见路人”,雾霾所形成的气溶胶没有丁达尔效应B.工厂静电除尘装置利用了胶体的电泳原理C.将NaOH浓溶液滴加到饱和FeCl3溶液中制备Fe(OH)3胶体D.将植物油倒入水中用力搅拌可得到胶体分散系
[解析] 雾霾所形成的气溶胶属于胶体,胶体能够产生丁达尔效应,所以雾霾所形成的气溶胶可以产生丁达尔效应,A错误;胶体中的胶粒带电,故可以在电场中向着某一极移动,可以用于工厂除尘,B正确;将NaOH浓溶液滴加到饱和FeCl3溶液中得到Fe(OH)3沉淀,C错误;将植物油倒入水中用力搅拌,可得到乳浊液,D错误。
(2)(2021·山东滨州高三检测)用白磷还原法可制得一种金的分散系,该分散系在临床诊断及药物检测等方面有着广泛的应用。具体操作步骤如下:①取20%白磷的乙醚溶液0.5 mL,加蒸馏水60 mL。②先滴加1%氯化金水溶液0.75 mL,再滴加1%的K2CO3溶液0.6 mL,振荡变成棕红色。③加热煮沸至液体变成透明红色。④分离提纯,除去无机溶质。所得分散系中金颗粒直径为5~12 nm。
请回答下列问题:(ⅰ)该分散系属于________,其分散质是__________。(ⅱ)用一束强光照射该分散系,从侧面可看到______________________。(ⅲ)继续加热所得红色透明液体,________(填“能”或“不能”)保持其性质不变。
[解析] (ⅰ)所得分散系中金颗粒的直径在1~100 nm,所以该分散系属于胶体,其分散质是金颗粒。(ⅱ)该分散系属于胶体,胶体具有丁达尔效应,所以用一束强光照射该分散系,从侧面能看到一条光亮的“通路”。(ⅲ)若将所得红色液体继续加热,则会发生聚沉,不能保持其性质不变。
[解析] 过滤法可分离固体和液体,故A错误;X是FeCl3溶液,分散质是Cl-和Fe3+,Z是Fe(OH)3胶体,分散质是Fe(OH)3胶粒,故B正确;CaCO3能与H+结合生成H2O和CO2,促进Fe3+的水解,故C正确;Z是Fe(OH)3胶体具有胶体的性质,能产生丁达尔效应,故D正确。
胶体与溶液的分离和鉴别鉴别:利用丁达尔效应鉴别胶体和溶液。分离:利用渗析操作来分离胶体和溶液。
〔对点集训2〕 (1)(2022·山东青岛高三检测)向含有c(FeCl3)=0.2 ml·L-1、c(FeCl2)=0.1 ml·L-1的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其分散质粒子是直径约为9.3 nm的金属氧化物,下列有关说法中正确的是( )A.该分散系的分散质为Fe2O3B.该分散系属于溶液C.加入NaOH时发生的反应可能为Fe2++2Fe3++8OH-═══Fe3O4+4H2OD.可用过滤的方法将黑色金属氧化物与Na+分离开
[解析] 本题考查从宏观角度辨识不同的分散系,从微观角度探析不同分散系性质的成因。氧化铁为红棕色,由题意知得到一种黑色分散系,A项错误;该分散系中分散质粒子是直径约为9.3 nm的金属氧化物,则该分散系为胶体,B项错误;氯化亚铁、氯化铁与氢氧化钠反应生成四氧化三铁、水和氯化钠,离子方程式为Fe2++2Fe3++8OH-═══Fe3O4+4H2O,C项正确;胶体、溶液都可以透过滤纸,不能用过滤方法分离,D项错误。
(2)(2022·河北衡水高三检测)硫代硫酸钠(Na2S2O3)溶液与盐酸混合,生成单质硫并沉淀出来。若将硫代硫酸钠溶液先与界面活性剂(不参与反应)均匀混合于烧杯中,再加入盐酸并立刻搅拌、静置后无沉淀产生,得到含硫单质的胶体(硫分散在体系中)。下列叙述错误的是( )A.界面活性剂减缓了硫生成的速率B.加入界面活性剂后生成的单质硫颗粒直径约为1~100 nmC.硫代硫酸钠与盐酸反应中,盐酸作氧化剂D.用光束照射烧杯中液体,将观察到光亮的“通路”
[解析] A.加入界面活性剂,反应变慢,故A正确;B.该分散系是含硫单质的胶体,胶体分散质粒子直径在1~100 nm,则单质硫颗粒直径约为1~100 nm,故B正确;C.反应前后HCl中各元素没有化合价变化,不是氧化剂,故C错误;D.该分散系是胶体,有丁达尔效应,能观察到光亮的“通路”,故D正确。
(3)(2022·河北衡水高三检测)某校课外小组同学制备Fe(OH)3胶体,并研究该胶体的性质。①该小组同学采用了以下操作制备胶体,请将空白处填写完整。取一个烧杯,加入20 mL蒸馏水,加热至沸腾,然后向烧杯中滴加1~2 mL饱和_________溶液,继续煮沸,待________________后,停止加热。②将制得的胶体放入半透膜制成的袋内,如图甲所示,放置2 min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察______(填“有”或“无”)丁达尔效应,再向烧杯中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为__________________。
③将半透膜内的液体倒入U形管中,如图乙所示,在液体上方加入少量电解液以保护胶体,接通直流电后,观察到的现象是______(填“阴”或“阳”)极附近颜色逐渐变深,其原因是_________________________________。
Fe(OH)3胶体粒子带正电荷
[解析] ①制备氢氧化铁胶体应该将新制的饱和氯化铁溶液滴入沸水中,继续煮沸至液体呈红褐色,停止加热。②胶体不能透过半透膜,而溶液中的离子能透过半透膜,所以半透膜外的液体不能产生丁达尔效应,由于溶液中含有Cl-,因此能和Ag+反应生成不溶于稀硝酸的氯化银白色沉淀。③氢氧化铁胶体的胶粒带正电荷,通电时向阴极移动,故阴极附近溶液颜色加深。
胶体聚沉属于物理变化。如蛋白质的盐析就属于胶体聚沉现象,但蛋白质的变性不属于胶体的聚沉,此过程属于化学变化。不是所有胶体都有电泳现象,如淀粉胶体粒子不带电荷。有电泳现象的胶体是因为胶粒吸附带电荷的粒子而带电。
书写Fe(OH)3胶体制备的化学方程式的五个易错点:①用“═══”而不是“”;②Fe(OH)3后不标“↓”;③反应条件是“△”;④HCl后不能标“↑”符号。⑤Fe(OH)3胶体中逐滴加入稀硫酸的现象是先沉淀后溶解。同理,在Al(OH)3胶体中加入稀NaOH溶液,现象也是先沉淀后溶解。
胶体知识易错“4”提醒
1.牢记一个范围:胶体分散质粒子直径在1~100 nm。2.熟知两种分类方法:交叉分类法和树状分类法。3.物理变化和化学变化的判断方法
4.明确三种分散系及本质区别:溶液、浊液和胶体,本质区别是分散质粒子直径的大小。5.胶体的三性质:丁达尔效应、聚沉和电泳。6.聚沉三方法:加入电解质溶液、加热或搅拌、与胶粒带相反电荷的胶体混合。7.认识八种常见的胶体:雾、蛋白质溶液、淀粉溶液、牛奶、豆浆、墨水、Fe(OH)3胶体、Al(OH)3胶体。8.辨析一个易错问题:胶体是电中性的,但胶体粒子因吸附作用可能带有电荷。
第04讲 物质的组成、性质和分类(课件)-备战2024年高考化学一轮复习讲练测: 这是一份第04讲 物质的组成、性质和分类(课件)-备战2024年高考化学一轮复习讲练测,共60页。PPT课件主要包含了复习目标,网络构建,知识梳理题型归纳,真题感悟,内容索引,考情分析,PARTONE等内容,欢迎下载使用。
新高考化学一轮复习课件 第1章 第1讲 物质的组成、性质和分类: 这是一份新高考化学一轮复习课件 第1章 第1讲 物质的组成、性质和分类,共60页。PPT课件主要包含了高考化学一轮复习策略,物质的组成与分类,归纳整合,专项突破,物质的性质与变化,分散系胶体,真题演练明确考向,课时精练等内容,欢迎下载使用。
(新高考)高考化学大一轮复习课件第1章第1讲物质的组成、性质和分类(含解析): 这是一份(新高考)高考化学大一轮复习课件第1章第1讲物质的组成、性质和分类(含解析),共60页。PPT课件主要包含了复习目标,物质的组成与分类,物质的组成1,不同种单质,金属氧化物,碱性氧化物,两性氧化物,非金属氧化物,酸性氧化物,不成盐氧化物等内容,欢迎下载使用。












