

















2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算专项
展开
这是一份2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算专项,文件包含2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算困难题③docx、2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算困难题②docx、2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算困难题①docx、2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算提升题①docx、2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算提升题②docx、2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算提升题③docx、2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算基础题①docx、2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算基础题②docx、2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算基础题③docx等9份试卷配套教学资源,其中试卷共133页, 欢迎下载使用。
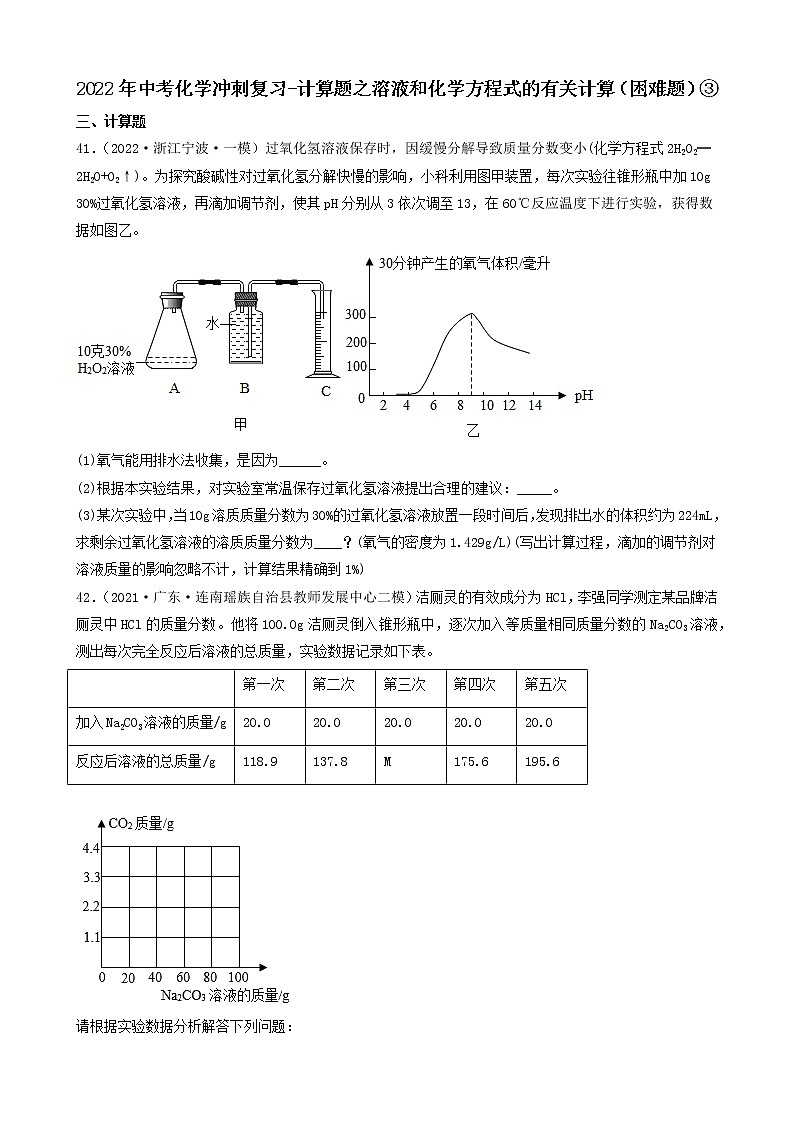
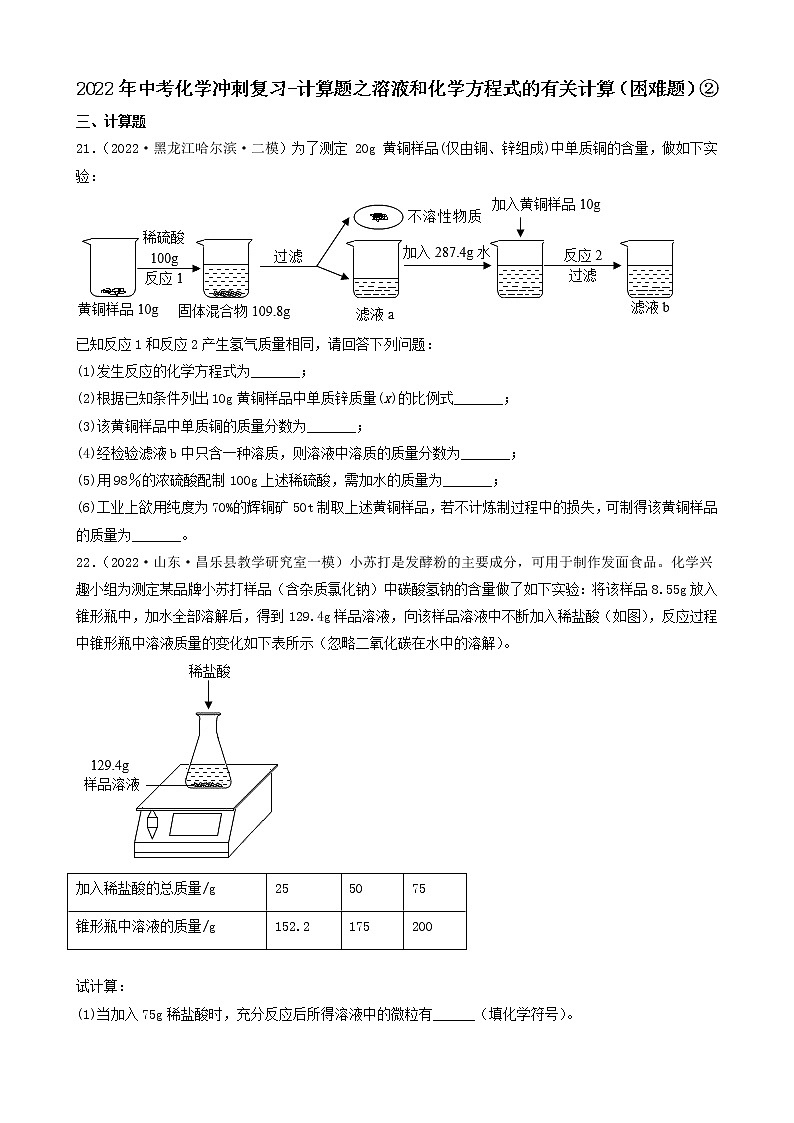
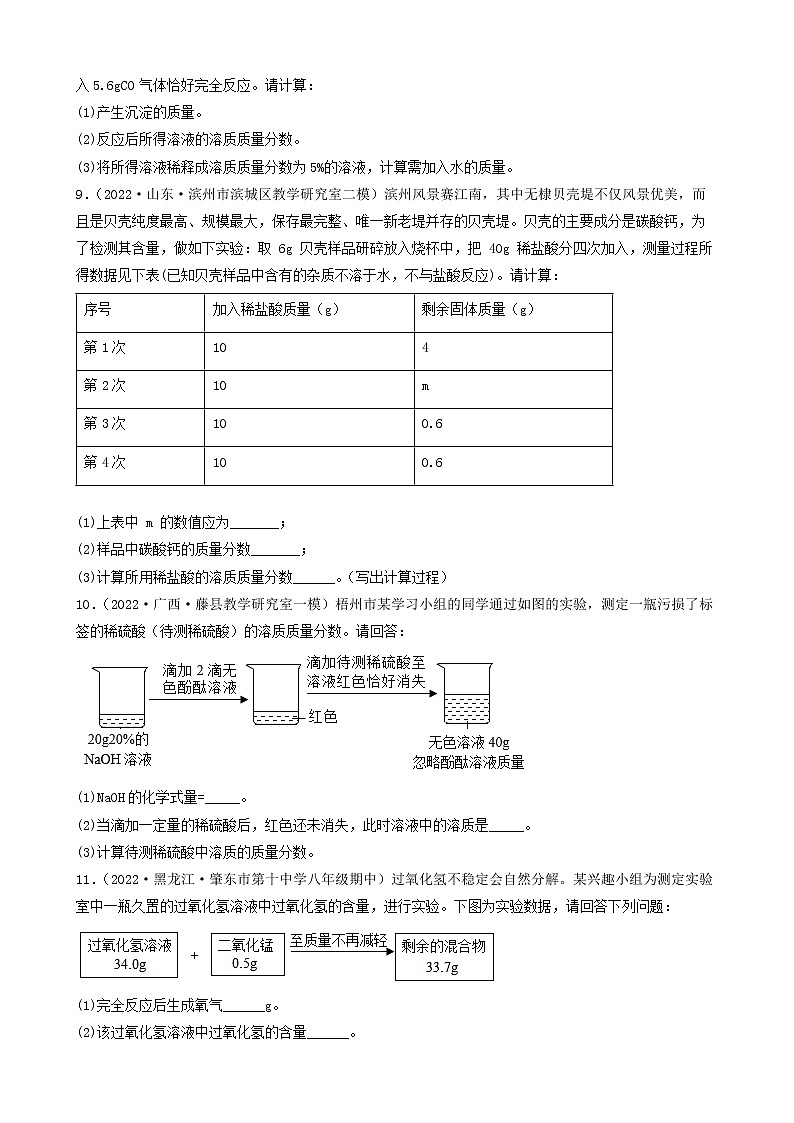
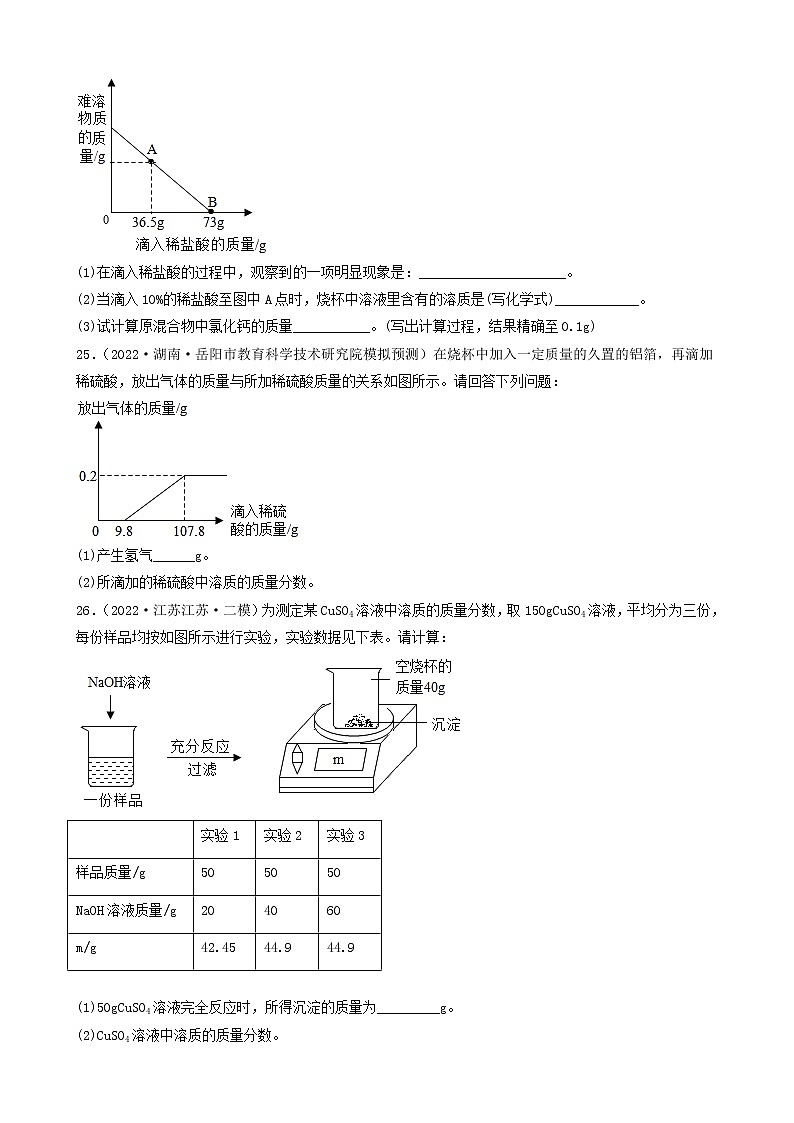
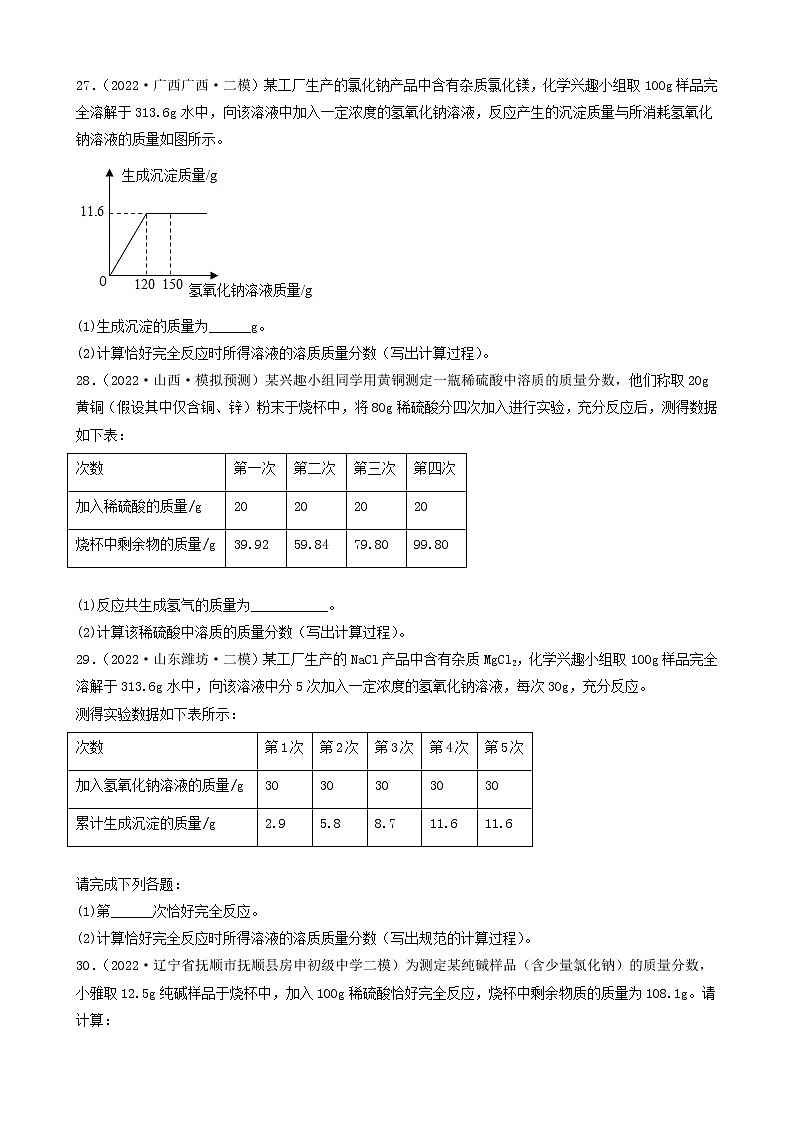
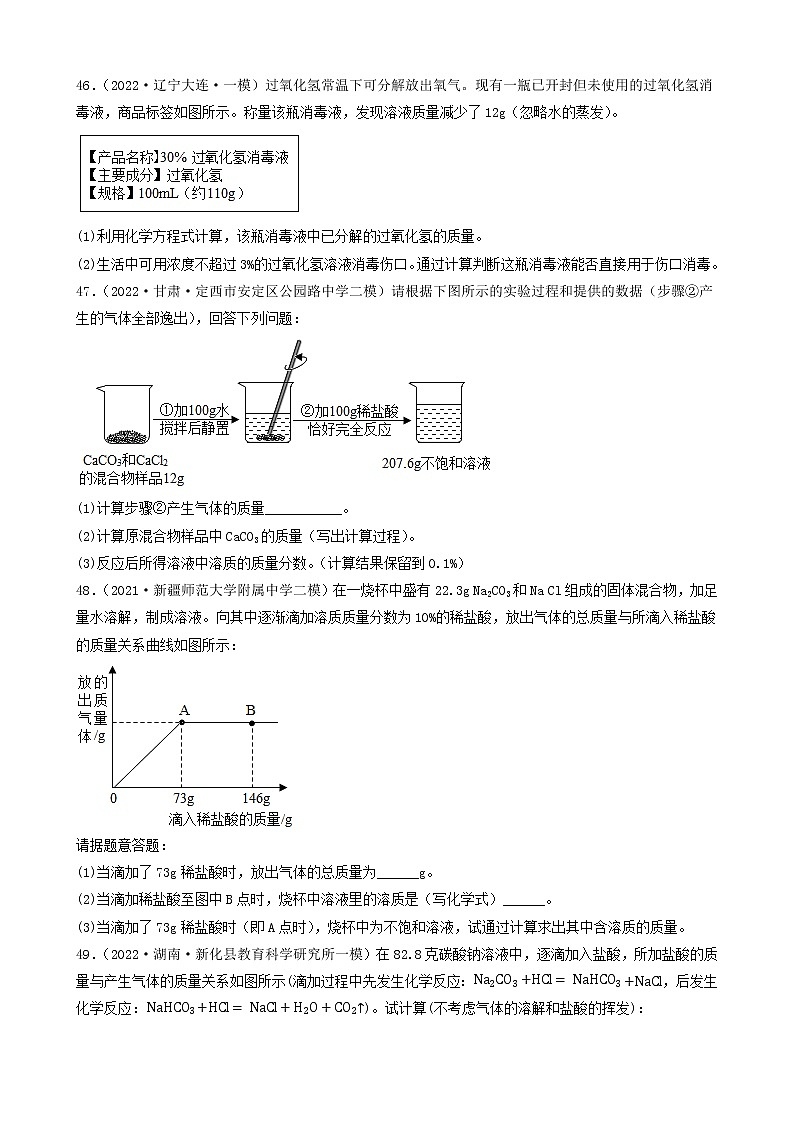
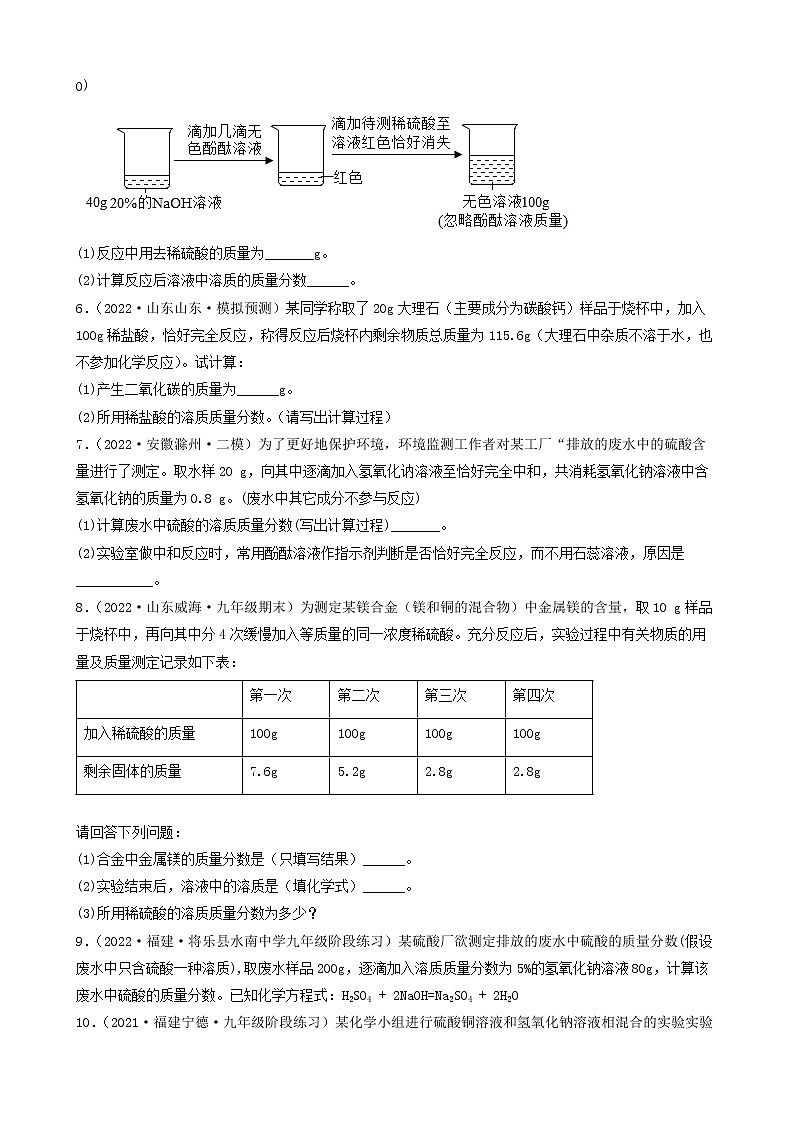
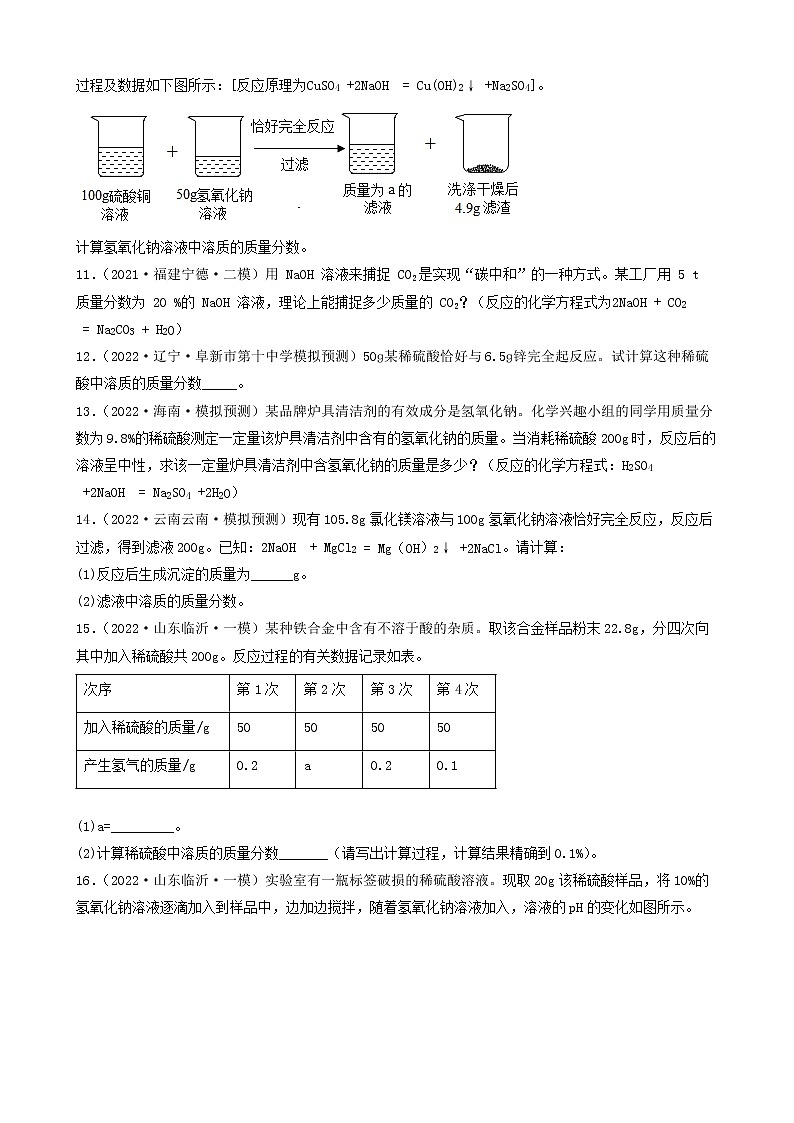
2022年中考化学冲刺复习-计算题之溶液和化学方程式的有关计算(提升题)③四、计算题41.(2022·甘肃定西·九年级期中)现有50g氯化钙溶液与100g碳酸钠溶液恰好完全反应,将反应后的混合液过滤后得到溶液的质量为140g。(1)生成沉淀的质量是______。(2)过滤后所得溶液的溶质质量分数是多少?(保留一位小数)42.(2022·安徽合肥·二模)某氯碱工厂用电解饱和食盐水制取氢氧化钠,原理为:2H2O+ 2NaCl2NaOH +H2↑+Cl2↑,现将107.3 kg的氯化钠溶液电解(忽略水的挥发和气体的溶解),共收集到H2为0.2kg。请计算电解后所得溶液中氢氧化钠的溶质质量分数_______?43.(2022·湖南·宁远县教研室九年级学业考试)某同学想测定某赤铁矿石中Fe2O3含量,取一个洁净的烧杯,放入25g赤铁矿石,然后往烧杯中滴加稀硫酸(样品中杂质不溶于水,也不与硫酸反应),实验数据如图所示。请回答下列问题。(1)25g赤铁矿石中Fe2O3的质量为_________g。(2)计算恰好完全反应时所得溶液中溶质的质量分数。(写出详细的解题过程)44.(2022·湖南·宁远县教研室模拟预测)某化学兴趣小组的同学为测定假黄金(铜锌合金)中锌的质量,取20g假黄金置于烧杯中,取100g稀盐酸恰好充分反应,剩余固体质量为13.5g,求:(1)假黄金(铜锌合金)中锌的质量是_______g.(2)所用稀盐酸中溶质的质量分数是多少?(写出计算过程)45.(2021·四川省荣县中学校九年级期中)某混合溶液中含有氯化铜和稀盐酸,向其中慢慢滴入20%的氢氧化钠溶液并振荡,所加氢氧化钠溶液的质量与生成沉淀的质量的关系如图所示:(1)当加入的氢氧化钠溶液为20g时,所得溶液的溶质是______;(2)反应最终生成的沉淀质量是多少?(3)当加入氢氧化钠溶液为60g时,溶液中溶质的质量是多少?(写出具体计算步骤)46.(2022·辽宁大连·一模)过氧化氢常温下可分解放出氧气。现有一瓶已开封但未使用的过氧化氢消毒液,商品标签如图所示。称量该瓶消毒液,发现溶液质量减少了12g(忽略水的蒸发)。(1)利用化学方程式计算,该瓶消毒液中已分解的过氧化氢的质量。(2)生活中可用浓度不超过3%的过氧化氢溶液消毒伤口。通过计算判断这瓶消毒液能否直接用于伤口消毒。47.(2022·甘肃·定西市安定区公园路中学二模)请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:(1)计算步骤②产生气体的质量___________。(2)计算原混合物样品中CaCO3的质量(写出计算过程)。(3)反应后所得溶液中溶质的质量分数。(计算结果保留到0.1%)48.(2021·新疆师范大学附属中学二模)在一烧杯中盛有22.3g Na2CO3和Na Cl组成的固体混合物,加足量水溶解,制成溶液。向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:请据题意答题:(1)当滴加了73g稀盐酸时,放出气体的总质量为______g。(2)当滴加稀盐酸至图中B点时,烧杯中溶液里的溶质是(写化学式)______。(3)当滴加了73g稀盐酸时(即A点时),烧杯中为不饱和溶液,试通过计算求出其中含溶质的质量。49.(2022·湖南·新化县教育科学研究所一模)在82.8克碳酸钠溶液中,逐滴加入盐酸,所加盐酸的质量与产生气体的质量关系如图所示(滴加过程中先发生化学反应:,后发生化学反应:)。试计算(不考虑气体的溶解和盐酸的挥发):(1)m的值为__________。(2)刚好不再产生气体时,溶液中溶质的质量分数(写出化学方程式及计算过程)。__________。50.(2022·辽宁抚顺·模拟预测)黄铜是铜和锌的合金,可以用来制造机器零件及日常用品。为了测定某黄铜样品中铜的质量分数,取20g该样品向其中加入一定量的10%的稀硫酸,恰好完全反应,产生氢气的质量为0.2g。请计算。(写出计算过程)(1)该黄铜样品中铜的质量分数。(2)恰好完全反应时,消耗稀硫酸的质量。51.(2022·陕西西安·二模)环保部门对某造纸厂排放的污水进行检测,发现其主要污染物为氢氧化钠。为测定污水中氢氧化钠的含量,取100g污水于烧杯中,逐滴加入10%的稀硫酸至49g时恰好完全反应(污水中的其它成分不与硫酸反应)。试分析并计算:(1)将10g溶质质量分数为98%的浓硫酸稀释为质量分数为10%的稀硫酸,所需水的质量是__g。(2)计算该污水中NaOH的质量分数_____。52.(2022·黑龙江绥化·九年级期末)将一定质量的NaCl和Na2SO4固体混合物20g完全溶于145.3g水后,加入一定质量分数的BaCl2溶液208g恰好完全反应,过滤,得到23.3g沉淀,计算:(1)原固体中的Na2SO4质量是______。(2)反应后所得溶液中溶质质量分数是多少?53.(2022·山东临沂·一模)某补钙片的主要成分为CaCO3,取钙片10g(假设钙片中其他成分不含钙元素,不溶于水且不与任何物质发生反应)。化学兴趣小组为测定钙片中钙元素的含量,进行了如图实验:根据图示信息,完成下列各题:(1)钙片中碳酸钙的质量分数为______。(2)求恰好完全反应时所得溶液的溶质质量分数?(要求写出计算过程)54.(2022·山东泰安·九年级学业考试)某补钙片的主要成分为CaCO3,每片钙片重0.5 g(假设钙片中其他成分不含钙元素,不溶于水且不与任何物质发生反应)。化学兴趣小组为测定钙片中钙元素的含量,进行了如图实验:根据图示信息,完成下列各题:(1)研碎的20片钙片中含有CaCO3的质量为______g。(2)钙片中钙元素的质量分数为______(结果精确到1%)(3)求恰好完全反应时所得溶液的溶质质量分数? (写出计算过程,结果精确到1%)55.(2022·福建省厦门集美中学九年级阶段练习)某课外活动小组同学取一定量的铜与氧化铜的粉末固体混合物放入烧杯中,加入 50 g 稀硫酸, 恰好完全反应,烧杯中固体的质量随收集变化情况如图所示。(1)反应结束后,剩余的固体是_________。(2)计算所用稀硫酸的溶质质量分数。56.(2022·陕西师大附中模拟预测)向100gMgC12溶液中,不断加入一定溶质质量分数的KOH溶液,实验数据如下表:KOH溶液的质量/g5.611.222.433.6生成Mg(OH)2沉淀的质量/g0.1450.290.580.58 (1)当滴加氢氧化钾溶液的质量为33.6g时,所得溶液的pH_____(填“<”“=”或“>”)7。(2)选择合理的数据,计算该氯化镁溶液中溶质的质量分数_____。57.(2022·陕西·西安高新第一中学初中校区模拟预测)某化学兴趣小组的同学为测定某赤铁矿样品中氧化铁的含量,进行如下图所示实验(杂质不溶于水也不与酸反应)。请完成下列分析及计算:(1)写出滤液中的阳离子符号______。(2)计算所得滤液的溶质质量分数______。58.(2022·广西百色·一模)某造纸厂的废液中含有一定量的氢氧化钠,可用硫酸中和,已知废液中NaOH的质量分数为4%,现用H2SO4的质量分数为9.8%的废硫酸10t将其处理至恰好完全反应,可以处理的废液质量是____?(写出计算过程)59.(2022·安徽·马鞍山二中实验学校一模)实验室常用过氧化氢溶液和二氧化锰混合制取氧气。(1)用136g溶质质量分数为5%的过氧化氢溶液理论上可以制取氧气质量是多少?(2)用排水法收集的氧气质量一定小于理论值,原因可能是__________(写一条即可)。60.(2022·宁夏·吴忠市第三中学九年级期中)某纯碱样品中含有少量氯化钠,某同学称取11g样品放入烧杯中,向烧杯中加入73g稀盐酸。恰好完全反应后烧杯中剩余的总质量为79.6g(假设产生的气体全部逸出)(计算结果精确到0.1%)。(1)反应生成气体的质量为_______g。(2)样品中碳酸钠的质量分数是____?(3)所用盐酸溶液的溶质质量分数_____?
参考答案:41.(1)10g(2)8.4%解:设生成氯化钠的质量为x,过滤后所得溶液的溶质质量分数为;答:过滤后所得溶液的溶质质量分数为8.4%。【解析】(1)根据质量守恒定律,溶液质量减少的质量为生成沉淀的质量,生成沉淀的质量为50g+100g-140g=10g,故填:10g;(2)见答案。42.解:设生成氢氧化钠的质量为,生成氯气的质量为。解得:故电解后所得溶液中氢氧化钠的溶质质量分数为答:电解后所得溶液中氢氧化钠的溶质质量分数8%。【解析】【详解】见答案。43.(1)16g(2)20%解:设恰好完全反应时,生成硫酸铁的质量为x, x=40g根据质量守恒定律,反应前后溶液总质量不变,恰好完全反应时溶液质量为:184g+16g=200g所得溶液中溶质质量分数为:。答:所得溶液中溶质质量分数为20%。【解析】(1)样品中杂质不溶于水,也不与硫酸反应,根据图像可知,25g赤铁矿石中Fe2O3的质量为:25g-9g=16g。(2)见答案。44.(1)6.5(2)解:设反应的稀盐酸中HCl的质量为x。 所用稀盐酸中溶质的质量分数×100%=7.3%;答:所用稀盐酸中溶质的质量分数是7.3%。【解析】(1)锌能与盐酸反应,铜不能与盐酸反应,固体减少的质量即为参加反应的锌的质量,则锌的质量为20g-13.5g=6.5g,故填:6.5;(2)见答案。45.(1)氯化铜和氯化钠##氯化钠和氯化铜(2)设:反应最终生成的沉淀质量是。答:反应最终生成的沉淀质量是9.8g。(3)设:当加入氢氧化钠溶液为60g时,溶液中溶质的质量是。答:当加入氢氧化钠溶液为60g时,溶液中溶质的质量是11.7g。【解析】(1)据图可知,当加入的氢氧化钠溶液为20g时,氢氧化钠正好与稀盐酸反应,生成氯化钠和水。所以,当加入的氢氧化钠溶液为20g时,所得溶液的溶质是生成的氯化钠和没反应的氯化铜。(2)按照根据化学方程式计算步骤进行即可,详见答案。(3)按照根据化学方程式计算步骤进行即可,详见答案。46.(1)溶液质量减少的质量为反应生成氧气的质量,故生成氧气的质量为12g解:设该瓶消毒液中已分解的过氧化氢的质量为x x=25.5g答:该瓶消毒液中已分解的过氧化氢的质量为25.5 (2)这瓶消毒液中剩余的过氧化氢的质量为:110g×30%-25.5g=7.5g故这瓶消毒液中过氧化氢的溶质质量分数为:大于3%,故这瓶消毒液不能直接用于伤口消毒【解析】(1)见答案;(2)见答案。47.(1)4.4(2)解:原混合物样品中CaCO3的质量为x,生成氯化钙的质量为y答:原混合物样品中CaCO3的质量10g;(3)答:反应后所得溶液中溶质的质量分数6.3%。【解析】(1)碳酸钙和稀盐酸反应生成二氧化碳气体逸出,反应中生成二氧化碳的质量为:;(2)见答案。(3)见答案。48.(1)解:设当滴加了73g稀盐酸时,放出气体的总质量为xx=4.4g答:当滴加了73g稀盐酸时,放出气体的总质量为4.4g(2)NaCl、HCl(3)解:设当滴加了73g稀盐酸时,生成氯化钠的质量为y,固体混合物中碳酸钠的质量为zy=11.7gz=10.6g故当滴加了73g稀盐酸时(即A点时),溶液中溶质的质量为:11.7g+(22.3g-10.6g)=23.4g答:当滴加了73g稀盐酸时(即A点时),溶液中溶质的质量为23.4g【解析】(1)见答案;(2)当滴加稀盐酸至图中B点时,稀盐酸过量,碳酸钠和稀盐酸反应生成氯化钠、二氧化碳和水,故此时烧杯中溶液里的溶质是:NaCl、HCl;(3)见答案。49.(1)6.6(2)解:设反应生成氯化钠质量为x,由、可知:x=23.4g刚好不再产生气体时,溶液中溶质的质量分数是: 答:刚好不再产生气体时,溶液中溶质的质量分数是10%【解析】(1)由图可知,每加入20g稀盐酸,产生气体的质量为2.2g,故加入60g稀盐酸,产生气体的质量为:2.2g×3=6.6g,故m的值为6.6;(2)见答案。50.(1)解:设参加反应的锌质量为x x=6.5g故样品中铜的质量分数为: 答:样品中铜的质量分数为67.5%(2)解:设恰好完全反应时,消耗稀硫酸的质量为y y=98g答:恰好完全反应时,消耗稀硫酸的质量为98g。 【解析】(1)见答案;(2)见答案。51.(1)解:设需水的质量为x,根据稀释前后,溶质的质量不变,可得:10g×98%=(10g+x)×10%,x=88g(2)解:设该污水中NaOH的质量分数为y y=4%答:该污水中NaOH的质量分数为4%见答案。52.(1)14.2g或14.2克(2)解:设反应后生成氯化钠的质量为y, y=11.7g反应后所得溶液中溶质质量分数为:。答:反应后所得溶液中溶质质量分数是5%。【解析】(1)解:设原固体混合物中硫酸钠的质量为x, x=14.2g答:原固体混合物中硫酸钠的质量为14.2g。(2)见答案。53.(1)50%(2)解:设:恰好完全反应时所得溶液的溶质质量分数为答:恰好完全反应时所得溶液的溶质质量分数为5%。【解析】(1)钙片中碳酸钙的质量为:10g-(116g-111g)=5g,钙片中碳酸钙的质量分数为:;(2)见答案。54.(1)5(2)20%(3)设反应生成氯化钙质量为x,生成二氧化碳质量为y, x=5.55g, y=2.2g,恰好完全反应时所得溶液的溶质质量分数是:×100%5%;答:恰好完全反应时所得溶液的溶质质量分数是5%。【解析】(1)研碎的20片钙片中含有CaCO3的质量为碳酸钙质量:0.5g×20-5g=5g;(2)钙片中钙元素质量:5g××100%=2g,钙元素的质量分数为:×100%=20%;(3)见答案。55.(1)(2)解:设参加反应的硫酸质量为x稀硫酸的溶质质量分数为答:稀硫酸的溶质质量分数为19.6%。【解析】(1)铜的活动性比氢弱,不能与稀硫酸反应,氧化铜能与稀硫酸反应生成硫酸铜和水,反应后剩余的固体是铜;(2)见答案。56.(1)>(2)解:设该氯化镁溶液中溶质的质量分数为xx=0.95%答:该氯化镁溶液中溶质的质量分数为0.95%【解析】(1)根据前三组数据可知,每加入5.6g氢氧化钾溶液可生成0.145g氢氧化镁沉淀;则22.4g氢氧化钾溶液和100g氯化镁溶液恰好完全反应生成0.58g氢氧化镁沉淀,所以滴加氢氧化钾溶液的质量为33.6g时,氢氧化钾剩余,所得溶液显碱性,pH>7。(2)见答案。57.(1)Fe3+(2)解:氧化铁的质量为20g-4g=16g设生成氯化铁的质量为x答:所得滤液的溶质质量分数为10%。【解析】(1)氧化铁和盐酸反应生成氯化铁和水,且两者恰好反应,则滤液中的阳离子为铁离子Fe3+;(2)杂质不溶于水也不与酸反应,则剩余滤渣为杂质4g,则氧化铁的质量为20g-4g=16g;过程见答案。58.20t解:设可以处理的废液质量是x,答:可以处理的废液质量是20t。【解析】【详解】见答案。59.(1)解:设理论上可以制取氧气质量是x x=3.2g答:理论上可以制取氧气质量是3.2g(2)少量氧气溶于水或装置中部分氧气未排出【解析】(1)见答案;(2)用排水法收集的氧气质量一定小于理论值,原因可能是少量氧气溶于水或装置中部分氧气未排出。60.(1)4.4(2)设参加反应碳酸钠的质量为x,氯化氢的质量为y, x=10.6g, y=7.3g,样品中碳酸钠的质量分数是(3)所用盐酸溶液的溶质质量分数为【解析】(1)根据题意可得,反应生成二氧化碳质量为:11g+73g-79.6g=4.4g;
相关试卷
这是一份2022年中考化学冲刺复习-计算题之化学式的基本计算专项,文件包含2022年中考化学冲刺复习-计算题之化学式的基本计算困难题③docx、2022年中考化学冲刺复习-计算题之化学式的基本计算困难题②docx、2022年中考化学冲刺复习-计算题之化学式的基本计算中档题④docx、2022年中考化学冲刺复习-计算题之化学式的基本计算中档题②docx、2022年中考化学冲刺复习-计算题之化学式的基本计算中档题①docx、2022年中考化学冲刺复习-计算题之化学式的基本计算中档题③docx、2022年中考化学冲刺复习-计算题之化学式的基本计算中档题⑤docx、2022年中考化学冲刺复习-计算题之化学式的基本计算困难题①docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础提升题④docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础提升题⑤docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础提升题②docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础题⑤docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础提升题③docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础题③docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础题④docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础提升题①docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础题②docx、2022年中考化学冲刺复习-计算题之化学式的基本计算基础题①docx等18份试卷配套教学资源,其中试卷共138页, 欢迎下载使用。
这是一份2022年中考化学冲刺复习-计算题之某元素的质量分数计算专项,文件包含2022年中考化学冲刺复习-计算题之某元素的质量分数计算困难题③docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算中档题②docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算中档题③docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算困难题①docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算困难题②docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算中档题①docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算基础提升题④docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算基础提升题⑤docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算基础提升题②docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算基础提升题③docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算基础题docx、2022年中考化学冲刺复习-计算题之某元素的质量分数计算基础提升题①docx等12份试卷配套教学资源,其中试卷共106页, 欢迎下载使用。
这是一份2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算专项,文件包含2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算困难题②docx、2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算困难题③docx、2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算困难题①docx、2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算中档题①docx、2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算中档题③docx、2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算中档题②docx、2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算基础题②docx、2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算基础题③docx、2022年中考化学冲刺复习-计算题之混合物的化学方程式有关计算基础题①docx等9份试卷配套教学资源,其中试卷共130页, 欢迎下载使用。









