

精品解析:2020年全国统一考试化学试题(新课标Ⅰ)(原卷版)
展开
2020年普通高等学校招生全国统一考试
理科综合能力测试 化学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 P 31 S 32 Cl 35.5 V 51 Fe 56
一、选择题:本题共13个小题,每小题6分。共78分,在每小题给出的四个选项中,只有一项是符合题目要求的。
1.国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、过氧乙酸(CH3COOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错误的是
A. CH3CH2OH能与水互溶
B. NaClO通过氧化灭活病毒
C. 过氧乙酸相对分子质量为76
D. 氯仿的化学名称是四氯化碳
2.紫花前胡醇可从中药材当归和白芷中提取得到,能提高人体免疫力。有关该化合物,下列叙述错误的是
A. 分子式C14H14O4
B. 不能使酸性重铬酸钾溶液变色
C. 能够发生水解反应
D. 能够发生消去反应生成双键
3.下列气体去除杂质的方法中,不能实现目的的是
| 气体(杂质) | 方法 |
A | SO2(H2S) | 通过酸性高锰酸钾溶液 |
B | Cl2(HCl) | 通过饱和的食盐水 |
C | N2(O2) | 通过灼热的铜丝网 |
D | NO(NO2) | 通过氢氧化钠溶液 |
A. A B. B C. C D. D
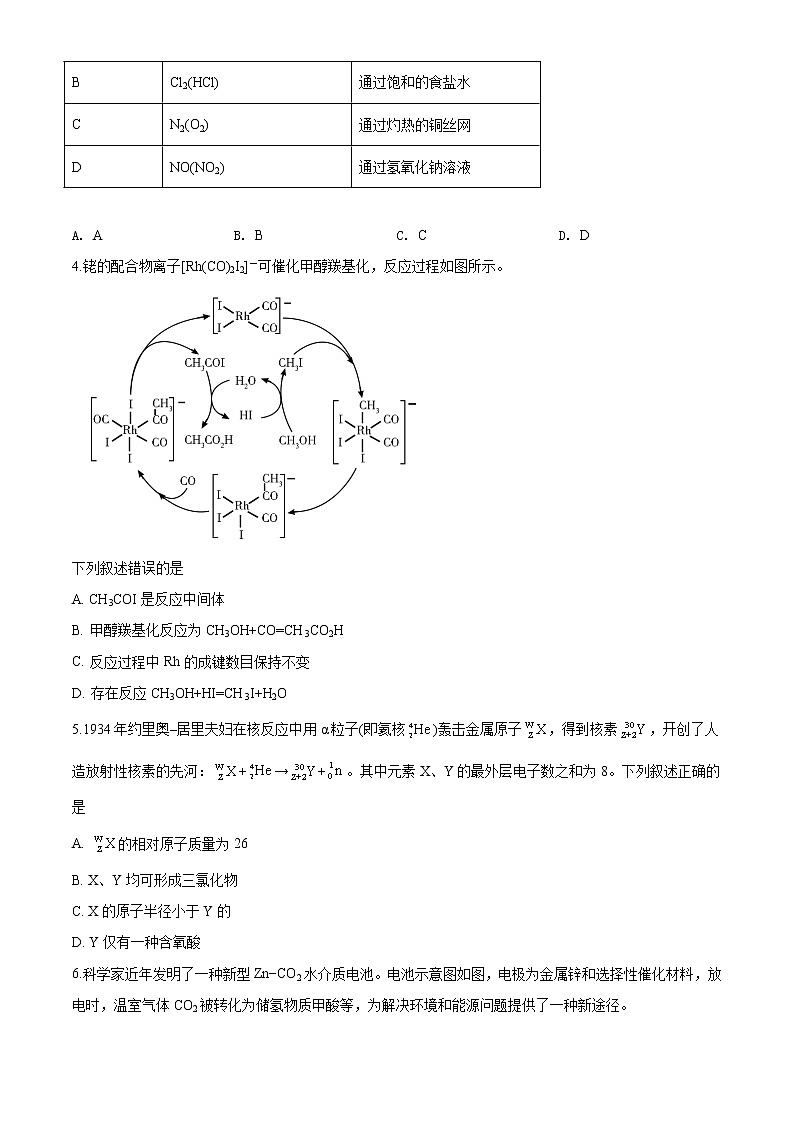
4.铑的配合物离子[Rh(CO)2I2]-可催化甲醇羰基化,反应过程如图所示。
下列叙述错误的是
A. CH3COI是反应中间体
B. 甲醇羰基化反应为CH3OH+CO=CH3CO2H
C. 反应过程中Rh的成键数目保持不变
D. 存在反应CH3OH+HI=CH3I+H2O
5.1934年约里奥–居里夫妇在核反应中用α粒子(即氦核)轰击金属原子,得到核素,开创了人造放射性核素的先河:+→+。其中元素X、Y的最外层电子数之和为8。下列叙述正确的是
A. 的相对原子质量为26
B. X、Y均可形成三氯化物
C. X的原子半径小于Y的
D. Y仅有一种含氧酸
6.科学家近年发明了一种新型Zn−CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A. 放电时,负极反应为
B. 放电时,1 mol CO2转化为HCOOH,转移的电子数为2 mol
C. 充电时,电池总反应为
D. 充电时,正极溶液中OH−浓度升高
7.以酚酞为指示剂,用0.1000 mol·L−1的NaOH溶液滴定20.00 mL未知浓度的二元酸H2A溶液。溶液中,pH、分布系数随滴加NaOH溶液体积VNaOH的变化关系如图所示。[比如A2−的分布系数:]
下列叙述正确的是
A. 曲线①代表,曲线②代表
B. H2A溶液的浓度为0.2000 mol·L−1
C. HA−电离常数Ka=1.0×10−2
D. 滴定终点时,溶液中
三、非选择题:共174分,第22~32题为必考题,每个试题考生都必须作答。第33~38题为选考题,考生根据要求作答。
(一)必考题:共129分。
8.钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
回答下列问题:
(1)“酸浸氧化”需要加热,其原因是___________。
(2)“酸浸氧化”中,VO+和VO2+被氧化成,同时还有___________离子被氧化。写出VO+转化为反应的离子方程式___________。
(3)“中和沉淀”中,钒水解并沉淀为,随滤液②可除去金属离子K+、Mg2+、Na+、___________,以及部分___________。
(4)“沉淀转溶”中,转化为钒酸盐溶解。滤渣③的主要成分是___________。
(5)“调pH”中有沉淀生产,生成沉淀反应的化学方程式是___________。
(6)“沉钒”中析出NH4VO3晶体时,需要加入过量NH4Cl,其原因是___________。
9.为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol·L−1 FeSO4溶液,需要仪器有药匙、玻璃棒、_________(从下列图中选择,写出名称)。
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择____________作为电解质。
阳离子 | u∞×108/(m2·s−1·V−1) | 阴离子 | u∞×108/(m2·s−1·V−1) |
Li+ | 4.07 | 4.61 | |
Na+ | 5.19 | 7.40 | |
Ca2+ | 6.59 | Cl− | 7.91 |
K+ | 7.62 | 8.27 |
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入________电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L−1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=________。
(5)根据(3)、(4)实验结果,可知石墨电极电极反应式为_______,铁电极的电极反应式为_______。因此,验证了Fe2+氧化性小于________,还原性小于________。
(6)实验前需要对铁电极表面活化。在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是_______。
10.硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO2的催化氧化:SO2(g)+O2(g)SO3(g) ΔH=−98 kJ·mol−1。回答下列问题:
(1)钒催化剂参与反应的能量变化如图所示,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:_________。
(2)当SO2(g)、O2(g)和N2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α 随温度的变化如图所示。反应在5.0MPa、550℃时的α=__________,判断的依据是__________。影响α的因素有__________。
(3)将组成(物质的量分数)为2m% SO2(g)、m% O2(g)和q% N2(g)的气体通入反应器,在温度t、压强p条件下进行反应。平衡时,若SO2转化率为α,则SO3压强为___________,平衡常数Kp=___________(以分压表示,分压=总压×物质的量分数)。
(4)研究表明,SO2催化氧化的反应速率方程为:v=k(−1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图所示。
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。t<tm时,v逐渐提高;t>tm后,v逐渐下降。原因是__________________________。
(二)选考题:共45分。请考生从2道物理题、2道化学题、2道生物题中每科任选一题作答。如果多做,则每科按所做的第一题计分。
11.Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为_________。
(2)Li及其周期表中相邻元素的第一电离能(I1)如表所示。I1(Li)> I1(Na),原因是_________。I1(Be)> I1(B)> I1(Li),原因是________。
(3)磷酸根离子的空间构型为_______,其中P的价层电子对数为_______、杂化轨道类型为_______。
(4)LiFePO4的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO4的单元数有____个。
电池充电时,LiFeO4脱出部分Li+,形成Li1−xFePO4,结构示意图如(b)所示,则x=_______,n(Fe2+ )∶n(Fe3+)=_______。
12.有机碱,例如二甲基胺()、苯胺(),吡啶()等,在有机合成中应用很普遍,目前“有机超强碱”的研究越来越受到关注,以下为有机超强碱F的合成路线:
已知如下信息:
①H2C=CH2
②+RNH2
③苯胺与甲基吡啶互为芳香同分异构体
回答下列问题:
(1)A的化学名称为________。
(2)由B生成C的化学方程式为________。
(3)C中所含官能团的名称为________。
(4)由C生成D的反应类型为________。
(5)D的结构简式为________。
(6)E的六元环芳香同分异构体中,能与金属钠反应,且核磁共振氢谱有四组峰,峰面积之比为6∶2∶2∶1的有________种,其中,芳香环上为二取代的结构简式为________。
《高考真题》2014年全国统一高考化学试卷(新课标ⅱ)(原卷版): 这是一份《高考真题》2014年全国统一高考化学试卷(新课标ⅱ)(原卷版),共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
《高考真题》2017年全国统一高考化学试卷(新课标ⅱ)(原卷版): 这是一份《高考真题》2017年全国统一高考化学试卷(新课标ⅱ)(原卷版),共7页。试卷主要包含了选择题,解答题等内容,欢迎下载使用。
《高考真题》2016年全国统一高考化学试卷(新课标ⅱ)(原卷版): 这是一份《高考真题》2016年全国统一高考化学试卷(新课标ⅱ)(原卷版),共7页。试卷主要包含了选择题,非选择题,选考题等内容,欢迎下载使用。












