

2022北京朝阳区高三下学期一模化学试卷含答案
展开北京市朝阳区2022届高三下学期质量检测一
化学试题
(考试时间90分钟 满分100分)
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Cl 35.5
第一部分(选择题,共42分)
每小题只有一个选项符合题意。共14个小题,每小题3分,共42分。
1. 下列变化属于物理变化的是
A. 液氨汽化 B. 火炬中的燃烧
C. 煤转化为汽油 D. 聚乳酸塑料袋降解为和
【1题答案】
【答案】A
2. 下列物质的应用中,利用了氧化还原反应的是
A. 用固体制备纯碱
B. 用作为潜水艇或呼吸面具的氧气来源
C. 用净化含少量泥土的浑浊水
D. 用除去粗盐中的钙离子
【2题答案】
【答案】B
3. 下列化学用语或图示表达不正确的是
A. 的结构示意图:
B. 2—甲基丁烷的结构模型:
C. 乙醇的核磁共振氢谱:
D. 的电子式:
【3题答案】
【答案】C
4. 干冰(固态二氧化碳)在-78℃时可直接升华为气体,其晶胞结构如图所示。下列说法不正确的是
A. 干冰晶体是共价晶体
B. 每个晶胞中含有4个分子
C. 每个分子周围有12个紧邻的分子
D. 干冰升华时需克服分子间作用力
【4题答案】
【答案】A
5. 下列性质的比较,不正确的是
A. 酸性: B. 电负性:
C. 热稳定性: D. 第一电离能:
【5题答案】
【答案】C
6. 下列方程式与所给事实不相符的是
A. 通入氯水中,溶液褪色:
B. 酚酞滴入溶液中变为浅红色:
C. 冷凝气体得到液体:
D. 制备时,需除去溶液中的氧气,防止发生:
【6题答案】
【答案】B
7. 某同学进行如下实验:
实验 | 操作和现象 |
Ⅰ | 向溴水中滴加少量,振荡,层显橙色 |
Ⅱ | 向碘水中滴加少量,振荡,层显紫色 |
Ⅲ | 向、的混合液中加入。滴加氯水,振荡后层显紫色;再滴加氯水,振荡后紫色褪去;继续滴加氯水,振荡后层变为橙色 |
下列分析不正确的是
A. Ⅰ中层显橙色,说明层含
B. Ⅱ中的现象说明在中的溶解性大于在水中的溶解性
C. Ⅲ中层显紫色,说明的氧化性强于
D. Ⅲ中层变为橙色时,水层中仍含有大量
【7题答案】
【答案】D
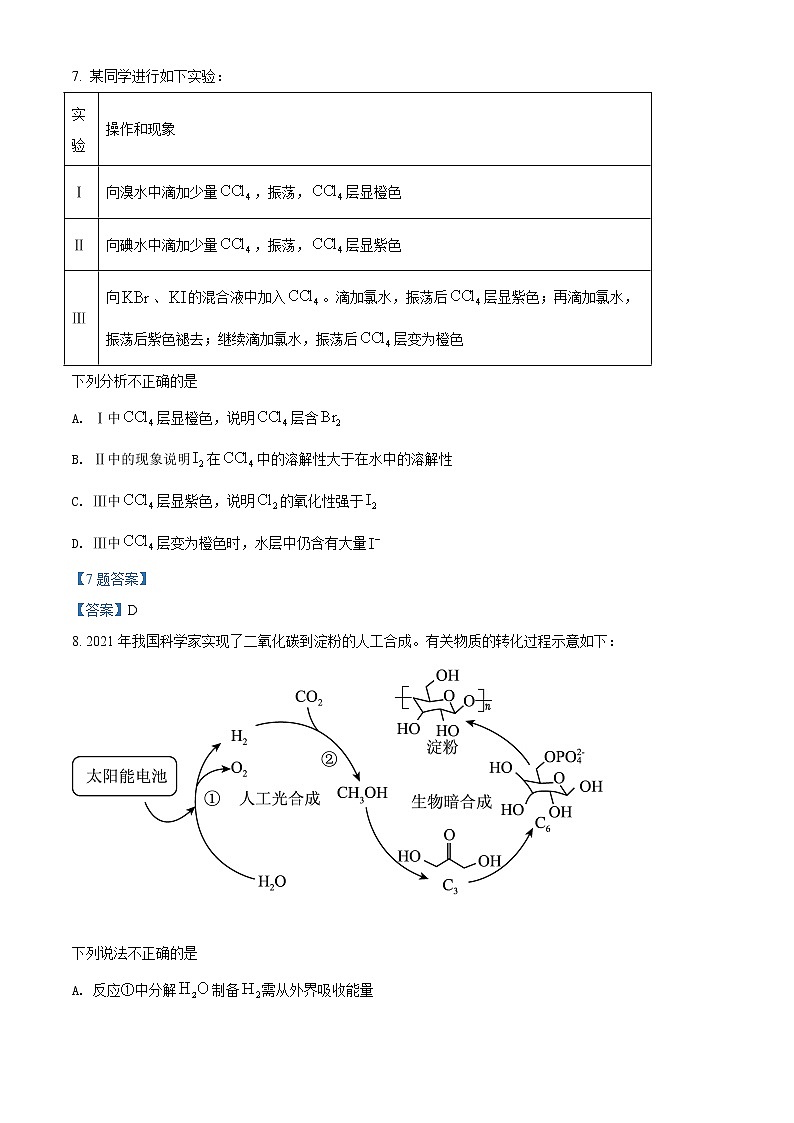
8. 2021年我国科学家实现了二氧化碳到淀粉的人工合成。有关物质的转化过程示意如下:
下列说法不正确的是
A. 反应①中分解制备需从外界吸收能量
B. 反应②中,碳原子的杂化方式发生了变化
C. 核磁共振、X射线衍射等技术可检测合成淀粉与天然淀粉的组成结构是否一致
D. C6→淀粉的过程中只涉及O-H键的断裂和形成
【8题答案】
【答案】D
9. 下列做法或实验(图中部分夹持略),不能达到目的的是
防止铁管道被腐蚀 | 检验产生的 | 制备并收集 | 精炼粗铜 |
A | B | C | D |
A. A B. B C. C D. D
【9题答案】
【答案】A
10. 测量汽车尾气中氮氧化物(、)含量的方法如下:
i.在高温、催化剂作用下,分解为和
ii.再利用与反应,产生激发态的(用表示),当回到基态时,产生荧光。通过测量荧光强度可获知的浓度,二者呈正比
下列说法不正确的是
A. 基态与具有的能量不同
B. 在大气中形成酸雨:
C. 与发生反应:
D. 测得荧光强度越大,说明汽车尾气中含量越高
【10题答案】
【答案】D
11. 聚碳酸酯(L)是滑雪镜镜片的主要材料,透明性好、强度高、不易碎,能够给运动员提供足够的保护,其结构简式如图。
已知:2R'OH++2R"OH。L可由两种链状单体经这反应制备。下列关于L的说法不正确的是
A. 制备L的反应是缩聚反应
B. 制备L的每个单体分子中均含两个苯环
C. L中的官能团是酯基和醚键
D. 通过蒸馏出苯酚可促进L的合成
【11题答案】
【答案】C
12. 在T℃,气体通过铁管时,发生腐蚀反应(X):(K=0.33),下列分析不正确的是
A. 降低反应温度,可减缓反应X的速率
B. 在气体中加入一定量能起到防护铁管的作用
C. 反应X的可通过如下反应获得:、
D. T℃时,若气体混合物中,铁管被腐蚀
【12题答案】
【答案】D
13. 探究溶液的性质,进行如下实验。(已知:的)
实验 | 装置 | 气体a | 现象 |
Ⅰ | 溶液立即变黄,产生乳白色沉淀 | ||
Ⅱ | 一段时间后,溶液略显浑浊 |
下列分析或解释正确的是
A 溶液呈碱性:
B. 实验Ⅰ、Ⅱ的现象说明,的氧化性强于
C. 两个实验中,通入气体后,试管中溶液的均降低
D. 实验Ⅰ中,溶液能促进气体的溶解
【13题答案】
【答案】D
14. 溶于一定量水中,溶液呈浅棕黄色(a)。加入少量浓黄色加深(b)。已知:(黄色);浓度较小时(用表示)几乎无色,取溶液进行如下实验,对现象的分析不正确的是
A. 测溶液a的,证明发生了水解
B. 加入浓HCl,H+与Cl-对溶液颜色变化、Fe3+浓度大小的影响是一致的
C. 向b中加入后,黄色褪去,说明能抑制水解
D. 将溶液a滴入沸水中,加热,检测有丁达尔效应,说明加热能促进水解
【14题答案】
【答案】B
第二部分(非选择题,共58分)
15. 以、和为主要成分的镀液可在某些材料上镀铜,原理如下:
(1)基态原子的价层电子排布式为_______。
(2)根据反应原理分析
①镀铜反应中,利用了的_______性。
②选择进行化学镀铜的原因之一是它易溶于水。下列分析正确的是_______
a.、均属于极性分子
b.与之间能形成氢键
c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的、、三种微粒,空间结构为三角形的是_______。
(4)为防止与形成沉淀,可加入使形成配合物。能电离出和。
(EDTA4-)
中除部分O外,还能与配位的原子是_______。
(5)铜—镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。位于_______区。
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:
上述方法不适合在该聚酰亚胺基材上直接镀铜。原因是:
①_______。
②聚合物有可能与配位。
【15~20题答案】
【答案】(1)3d104s1
(2) ①. 还原 ②. ab
(3)HCHO (4)N
(5)d (6)该聚酰亚胺基材上存在酰胺键,在碱性条件下易发生水解而遭到破
16. 以次氯酸盐为有效成分的消毒剂应用广泛。电解溶液制备溶液的装置示意如下。
资料:i.次氯酸钠不稳定:a. b.
ii.将次氯酸盐转化为次氯酸能更好地发挥消毒功能,次氯酸具有更强的氧化性
[制备]
(1)产生:
①生成的反应包括:、、_______。
②测所得溶液,试纸先变蓝()后褪色,说明溶液具有的性质是_______。
(2)相同温度下,在不同初始下电解溶液,对浓度的影响如下所示。
推测浓度在为3或13时较小的原因:
Ⅰ.时,阳极有放电
Ⅱ.时,的溶解度减小
Ⅲ.时,浓度增大,促使被氧化
①检验电解产物,推测Ⅰ成立。需要检验的物质是_______。
②根据化学平衡移动原理,推测Ⅱ合理。依据的化学平衡是_______。
③经检验,推测Ⅲ合理。用方程式解释:_______。
根据上述实验,电解法制备溶液,初始不宜过小或过大。
(3)同样方法电解溶液制备,由于生成_______覆盖在电极表面,电解难以持续。
[保存]
低温保存、加入、等物质能增强溶液的稳定性。
[测量]
(4)取V1mL所得样液,加水稀释。依次加入溶液、稀。析出的用标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗溶液V2mL。(已知:),样液中_______。
【16~19题答案】
【答案】(1) ①. Cl2+2OH-=Cl-+ClO-+H2O ②. 碱性和漂白性
(2) ①. O2 ②. Cl2+H2OH++Cl-+HClO ③. -4e-+2H2O=+4H+
(3)Ca(OH)2 (4)
17. 从印刷电路板的腐蚀废液(主要含CuCl2、FeCl3、FeCl2等)中回收FeCl3、制备CuSO4·5H2O的流程如下。
(1)上述流程中能加快反应速率的措施有_______。
(2)粗品的主要成分是硫酸铜晶体,而不是硝酸铜晶体,分析有两种可能的原因:
①相对于Cu2+,粗液中浓度过小,原因是_______(用离子方程式表示),不能得到硝酸铜晶体。
②粗液中浓度较大,但由于_______,不能得到硝酸铜晶体。
(3)测量粗品中铁(含、)的含量,评定纯度等级。
Ⅰ.用水溶解一定质量粗品,加入稀和溶液,加热。
Ⅱ.待溶液冷却后,加入试剂X至溶液。过滤、洗涤,得到红褐色沉淀。
Ⅲ.用稀溶解红褐色沉淀,滴入溶液,稀释至一定体积。将溶液红色的深浅与标准色阶对照,确定含量。
已知:完全沉淀的pH为6.7,完全沉淀的pH为2.8
①Ⅰ中将氧化为的离子方程式是_______。
②试剂X是_______。
(4)电解:在不同电压、不同pH(pH<7)条件下电解溶液,研究溶液的再生条件。
序号 | 电压 | 阴极现象 | 阳极产物 | |
i | a | 无气泡,少量金属析出 | 无,有 | |
ii | b | 较多气泡,极少量金属析出 | 无,有 | |
iii | a | 少量气泡,少量金属析出, | 有,有 |
(,)
①iii中产生的原因有、_______。
②溶液再生的合适条件是_______(填实验序号)。
【17~20题答案】
【答案】(1)粉碎、加热、搅拌
(2) ①. 3Cu+8H++2=3Cu2++2NO↑+4H2O ②. Cu(NO3)2的溶解度比CuSO4的大
(3) ①. 2Fe2++2H++H2O2=2Fe3++2H2O ②. CuO、Cu(OH)2、CuCO3等
(4) ①. 2Fe2++Cl2=2Fe3++2Cl- ②. ii
18. 药物Q能阻断血栓形成,它的一种合成路线。
已知:i.
ii.R'CHOR'CH=NR"
(1)→A的反应方程式是_______。
(2)B的分子式为。E的结构简式是_______。
(3)M→P的反应类型是_______。
(4)M能发生银镜反应。M分子中含有的官能团是_______。
(5)J的结构简式是_______。
(6)W是P的同分异构体,写出一种符合下列条件的W的结构简式:_______。
i.包含2个六元环,不含甲基
ii.W可水解。W与溶液共热时,最多消耗
(7)Q的结构简式是,也可经由P与Z合成。已知:,合成Q的路线如下(无机试剂任选),写出X、Y、Z的结构简式:_______。
【18~24题答案】
【答案】(1)+CH3COOH +H2O
(2) (3)酯化反应(或取代反应)
(4)羧基和醛基 (5)
(6) 或者或者或者 (7),,
19. 某小组验证“”(反应A)存在限度,并探究外加试剂对该平衡的影响。
(1)从正反应方向探究实验。取溶液,加入溶液(),溶液呈棕黄色,不再发生变化。
①通过检测出_______,证实反应A存在限度。
②加入,振荡,平衡向_______移动。
③除反应A外,还发生_______(写方程式),促进与的反应。
(2)从逆反应方向探究实验:向碘水(含淀粉)中加入酸性溶液,无明显变化。未检出。
①甲同学认为加入溶液可增大与的反应程度。甲同学依据的原理是_______。
②验证:加入溶液,产生沉淀a,溶液蓝色褪去。能检出。
(3)乙同学认为碘水中含有,加入溶液也可能产生沉淀。做对照实验:直接向碘水(含淀粉)中加入溶液。产生沉淀,溶液蓝色褪去。
查阅资料:
实验验证:
已知:、(微溶)
①Ⅲ中溶液作用是_______。
②Ⅳ中溶液的作用是_______(用离子方程式表示)。
检验、比较沉淀a、b的成分,可明确的作用。
(4)问题思考:向与碘水的混合液中加入溶液,可能发生如下反应:
i.与在的促进下发生的氧化还原反应
ii.与在促进下发生的反应
iii.与的反应
确认是否发生反应iii,设计实验:将反应后混合物过滤,_______。
供选择试剂:稀、溶液、溶液
已知:、溶于溶液;难溶于稀
【19~22题答案】
【答案】(1) ①. ②. 正反应方向 ③.
(2)生成AgI沉淀,降低,逆向进行(生成AgI沉淀,提高了I2的氧化能力)
(3) ①. 还原 ②.
(4)方法一:取滤渣,加入足量Na2S2O3溶液,过滤,若有固体剩余,加入稀HNO3,产生的气体遇空气变红棕色,说明滤渣中含银,iii成立
方法二:取滤渣,加入足量KI溶液,过滤,若有固体剩余,加入稀HNO3,产生的气体遇空气变红棕色,说明滤渣中含银,iii成立
北京市朝阳区2023届高三二模化学试卷: 这是一份北京市朝阳区2023届高三二模化学试卷,共10页。
2023北京朝阳区高三下学期一模化学试题含答案: 这是一份2023北京朝阳区高三下学期一模化学试题含答案,共15页。试卷主要包含了5 Fe 56,下列化学用语或图示表达正确的是,我国科学家预言的T-碳已被合成,用圆底烧瓶收集后进行喷泉实验,化学在国防领域发挥着重要作用,将铜棒插入浓、稀溶液中等内容,欢迎下载使用。
北京市朝阳区2022-2023学年高三下学期一模考试化学试卷(word版,含答案): 这是一份北京市朝阳区2022-2023学年高三下学期一模考试化学试卷(word版,含答案),共11页。试卷主要包含了5 Fe 56,0×10−12,Ksp=1,2 ml·L−1,21等内容,欢迎下载使用。












