






初中鲁教版第三节 海水“制碱“课文课件ppt
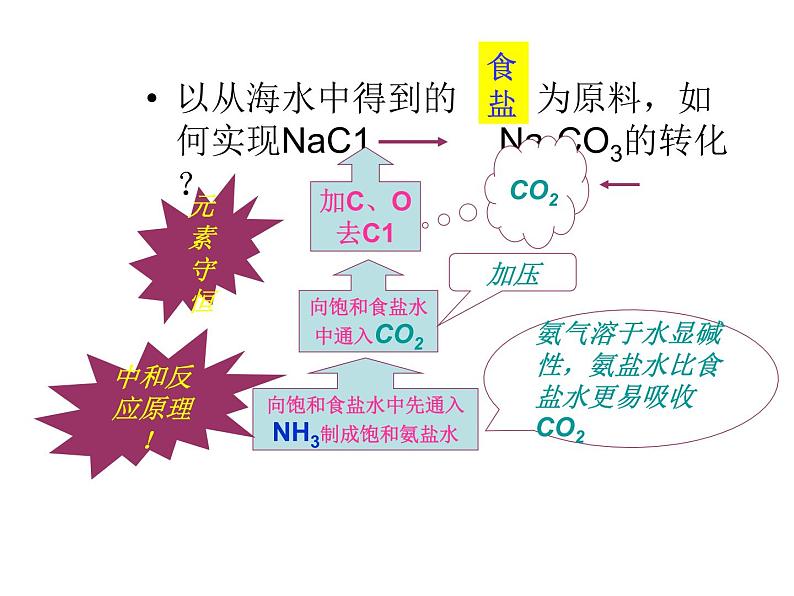
展开第三节 海水“制碱”一、教学目标: 知识与能力: 1。了解氨碱法制纯碱的原料和步骤 2。知道氨碱法制纯碱的化学反应原理 3.纯碱的性质4.复分解反应的条件过程与方法: 了解纯碱在日常生活和工农业生产中的应用 情感态度价值观:通过了解侯德榜的事迹,激发爱国热情,树立正确的科学观和人生价值观。 教学重点:氨碱法制纯碱的化学反应原理 教学难点:树立元素守恒观 你知道是什么物质让这些食品松软可口吗?天然碱 信息分析 海水中含量最多的盐就是食盐(NaCl),我国海岸线漫长,可采用盐田法晒制而得。原料来源广,成本低,且和纯碱(Na2CO3)都属钠盐,在组成上都含钠元素。提出猜想 ——食盐(NaC1)可以转化为纯碱(Na2CO3)思考以下问题 1、由NaCl转变为Na2CO3,物质的元素组成发生了什么变化?用NaCl制Na2CO3,还需含什么元素的物质? 2、二氧化碳有什么作用? 3、你是如何理解“氨为媒介”的?以从海水中得到的 为原料,如何实现NaC1 Na2CO3的转化? CO2加C、O去C1元素守恒向饱和食盐水中通入CO2向饱和食盐水中先通入NH3制成饱和氨盐水氨气溶于水显碱性,氨盐水比食盐水更易吸收CO2中和反应原理!加压食盐海水制碱的原料: 食盐、水、二氧化碳和氨气 成果共享 食盐、和氨气 ↓CO2↓“输送”CO2,并使之转化为HCO3-CaCO3=CaO+CO2 ↑ CaO+H2O=Ca(OH)2Ca(OH)2+2NH4C1=CaC12+2NH3↑+2H2O氨碱法高温Ca O↑→Ca(OH)2 ↓提供CO2回收氨气氨气可以循环利用氨气起了媒介作用提出方案 ——初步讨论(1)先向饱和食盐水中通入NH3; (2)再通入足量CO2: NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl 1、为什么氨盐水比食盐水更易吸收二氧化碳? 氨水显碱性、二氧化碳溶于水生成碳酸,两者之间能发生中和反应。NaCI+NH3+CO2+H2O=NaHCO3 +NH4CI 2NaHCO3 = Na2CO3+H2O+CO2↑奥秘揭示 同温下NaHCO3 比 NH4C1的溶解度小,易结晶析出。吸氨碳化过滤热解△明确原理——海水制碱的反应方程式(3)过滤 NH4Cl(母液)+NaCl(固体)+NH3, 搅拌,降温结晶得NH4Cl副产品(氮肥) NaCl 、NaHCO3、NH4Cl 和NH4HCO3同时存在于水溶液中。这四种物质在室温条件下, NaHCO3的溶解度最小,因此先析出晶体。(晶体析出后溶液是NaHCO3的饱和溶液)(20℃时,NaCl、NaHCO3 、NH4Cl溶解度分别是36g、9.6g、37.2g)2、氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵, 哪种物质首先结晶析出?为什么?海水“制碱”工业生产的简单流程 一、氨碱法制纯碱 纯碱工业始创于18世纪,在很长一段时间内制碱技术把持在英、法、德、美等西方发达国家手中。1921年正在美国留学的侯德榜先生为了发展我国的民族工业,应爱国实业家范旭东先生之邀毅然回国,潜心研究制碱技术,成功地摸索和改进了西方的制碱方法,发明了将制碱与制氨结合起来的联合制碱法(又称侯氏制碱法)。侯德榜为纯碱和氮肥工业技术的发展做出了杰出的贡献。侯德榜红三角牌纯碱 永利化工厂 联合碱法(候氏制碱法)制纯碱-Na2CO3 原理(步骤): 盐水精盐水精制吸氨碳酸化碳酸氢钠纯碱过滤热解氨盐水碳酸钠、碳酸氢钠1、碳酸钠( 化学式): 俗名:物理性质: 用途: 纯碱、苏打白色粉末状固体,易溶于水,其水溶液呈碱性。纯碱不是碱,是盐。Na2CO3玻璃纤维工业纯碱(Na2CO3)主要用于玻璃、化工、冶金、造纸、印染、合成洗涤剂、石油化工等工业。食用纯碱(Na2CO3)主要用于食品工业。2、碳酸氢钠 (化学式): 俗名:物理性质: 用途:化学性质:NaHCO3白色粉末状固体,易溶于水,其水溶液呈碱性。作食品添加剂、治疗胃酸过多、做灭火剂等。2NaHCO3 == Na2CO3 + H2O + CO2↑NaHCO3 + 2HCl == 2NaCl + H2O + CO2↑小苏打 实验:用试管取适量的碳酸钠溶液,向试管中滴加酚酞试液。现象: .可见,碳酸钠 (难、易)溶于水,溶液呈 性。 溶液颜色变红碱1、与指示剂的作用易二、纯碱的性质2、与盐酸和稀硫酸的反应 2HCl + Na2CO3 = 2NaCl + H2O + CO2↑H2SO4 + Na2CO3 = Na2SO4 + H2O + CO2↑3、与氢氧化钙的反应 Ca(OH)2 + Na2CO3= CaCO3 ↓+ 2NaOH(工业制取氢氧化钠)4、与氯化钡的反应 Na2CO3 + BaCl2 = BaCO3↓+ 2NaCl思考:如何鉴别碳酸根离子 取样品于试管中,滴加稀盐酸,可观察到有气泡产生,将产生的气体通入澄清的石灰水中,若石灰水变浑浊,则样品中有碳酸根离子或碳酸氢根离子。复分解反应1、概念:2、字母表达式:3、酸、碱、盐之间发生的反应为复分解反应,这一类的反应有一个非常重要的特点:由两种化合物互相交换成分,生成另外两种化合物的反应。反应前后各元素的化合价保持不变.4、酸、碱、盐之间在水溶液中发生的反应为复分解反应的实质: 酸、碱、盐所电离出的离子相互结合生成沉淀、气体或水的过程。 AB + CD AB + CDCAAB + CD 多识一点复分解反应的实质H2CO3 5、复分解反应发生的条件:须二者都可溶有沉淀生成或有气体放出或有水生成碱 + 盐盐 + 盐盐 + 酸酸 + 碱酸+金属氧化物盐的溶解性口诀:钾、钠、铵、硝酸盐全都溶;氯化物中银不溶,硫酸盐中钡不溶,硫酸钙、银是微溶;碳酸盐只溶钾、钠、铵。这些你都记住了吗?说明:1、钾、钠、铵、硝酸盐都可溶。 2、盐酸盐只有氯化银不溶。 3、硫酸盐只有硫酸钡不溶。4、碳酸盐只溶钾、钠、铵,碳酸镁微溶,剩下都不溶。1、酸都溶2、可溶性溶碱有五位:钾、钠、铵、钙、钡。1、 判断下列反应能否进行: AgNO3+ FeCl3=AgCl+ NaNO3=CaCO3+ NaOH=Na2SO4+ HCl= Fe(OH)3+ H2SO4=33 AgCl +Fe(NO3)3不反应,盐和盐反应时须均可溶不反应,碱和盐反应时须均可溶生成物中无气体、沉淀或水Fe2(SO4)3 + H2O3622、除去下列物质中的少量杂质1)、Na2CO3固体中混有NaHCO3,方法是 反应方程式是 。 2)、NaCl溶液中混有Na2CO3,方法是反应方程式是 。Na2CO3 + 2HCl = 2NaCl + CO2 ↑ + H2O3、妈妈在洗碗筷时,经常在水中加入一种物质,很快就能将“油乎乎”的菜盘洗得干干净净。妈妈在水中加入的物质可能是( ) A.汽油 B.烧碱 C.纯碱 D.食盐水4、A是一种白色难溶于水的钙盐,由三种元素组成,其相对分子质量为100。(1)用化学式表示:A ________,B ________(2)写出A与盐酸反应的化学方程式: ______________________________________(3)D中一定含有的溶质是 , 可能含有的溶质是 。CaCO3CO2CaOCaCO3CaCO3+2HCl==CaCl2+H2O+CO2↑ Na2CO3或Ca(OH)2NaOHCaCO3CaO(4)为进一步确定D溶液中可能存在的组成,还需设计实验并填写下表(可不填满,也可补充)Na2CO3Ca(OH)2稀盐酸碳酸钠溶液若有气泡产生,D溶液中存在Na2CO3若溶液变浑浊,D溶液中存在Ca(OH)2若上述两实验均无明显现象,Na2CO3和Ca(OH)2都不存在分别进行上述两实验Na2CO3和Ca(OH)2都不存在5.已知可溶性钡盐有毒,而在医院里做胃镜透视时,要用BaSO4造影,俗称“钡餐”,吃下BaSO4无毒是因为( )。但如果无意中误服了BaCO3则会引起中毒,这是因为(用化学方程式表示,下同)( ),误服后, 应立即用泻盐MgSO4解毒,这是因为( )。BaSO4不溶于水,也不与酸反应BaCO3+ 2HCl === BaCl2 + H2O +CO2↑BaCl2 + MgSO4 === BaSO4↓ + MgCl2教学反思 1 通过了解侯德榜的事迹,激发爱国热情,树立正确的科学观和人生价值观。 2 图片强化,理解化学与生活,生产,国防。 3 .纯碱,小苏打在生产,生活中的运用。
初中化学鲁教版九年级下册第三节 海水“制碱“教学ppt课件: 这是一份初中化学鲁教版九年级下册第三节 海水“制碱“教学ppt课件
初中鲁教版第三节 海水“制碱“示范课课件ppt: 这是一份初中鲁教版第三节 海水“制碱“示范课课件ppt,文件包含第八单元第三节海水“制碱”pptx、第八单元第三节海水“制碱”教学设计doc、第八单元第三节海水“制碱”一课一练doc等3份课件配套教学资源,其中PPT共34页, 欢迎下载使用。
初中化学鲁教版九年级下册第三节 海水“制碱“背景图课件ppt: 这是一份初中化学鲁教版九年级下册第三节 海水“制碱“背景图课件ppt,共15页。PPT课件主要包含了讨论交流等内容,欢迎下载使用。













