



热点10 新信息反应机理分析- 高考化学专练【热点·重点·难点】
展开热点10 新信息反应机理分析
【命题规律】
本专题考点为高考热点。主要考查物质变化过程中的能量变化和微粒变化。题型主要为选择题,难度中等。主要考查学生的宏观辨识和微观探析、变化观念和平衡思想素养。
【备考建议】
2021年高考备考应重点关注有关催化剂、中间产物、能量变化、化学键变化方面的信息反应机理。
【限时检测】(建议用时:30分钟)
1.(2020新课标Ⅰ)铑的配合物离子[Rh(CO)2I2]-可催化甲醇羰基化,反应过程如图所示。
下列叙述错误的是
A.CH3COI是反应中间体
B.甲醇羰基化反应为CH3OH+CO=CH3CO2H
C.反应过程中Rh的成键数目保持不变
D.存在反应CH3OH+HI=CH3I+H2O
【答案】C
【解析】
题干中明确指出,铑配合物充当催化剂的作用,用于催化甲醇羰基化。由题干中提供的反应机理图可知,铑配合物在整个反应历程中成键数目,配体种类等均发生了变化;并且也可以观察出,甲醇羰基化反应所需的反应物除甲醇外还需要CO,最终产物是乙酸;因此,凡是出现在历程中的,既非反应物又非产物的物种如CH3COI以及各种配离子等,都可视作中间物种。
A.通过分析可知,CH3COI属于甲醇羰基化反应的反应中间体;其可与水作用,生成最终产物乙酸的同时,也可以生成使甲醇转化为CH3I的HI,A项正确;
B.通过分析可知,甲醇羰基化反应,反应物为甲醇以及CO,产物为乙酸,方程式可写成:,B项正确;
C.通过分析可知,铑配合物在整个反应历程中,成键数目,配体种类等均发生了变化,C项不正确;
D.通过分析可知,反应中间体CH3COI与水作用生成的HI可以使甲醇转化为CH3I,方程式可写成:,D项正确;答案选C。
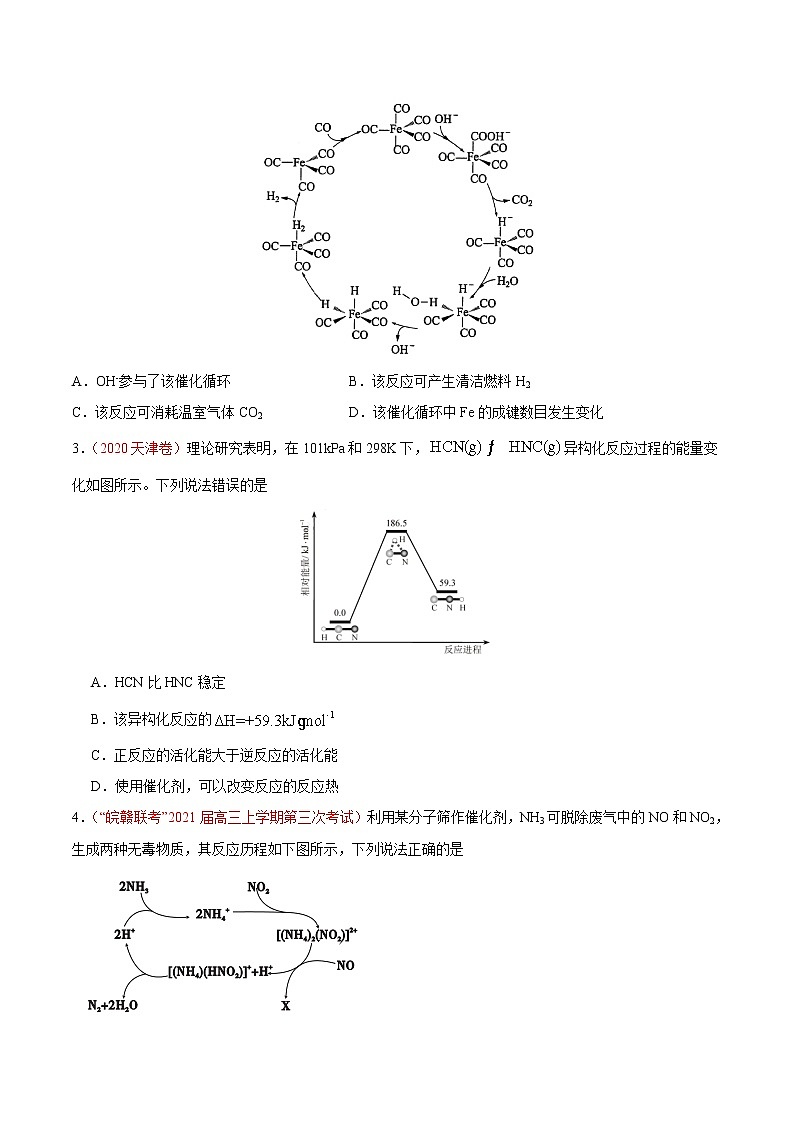
2.(2020新课标Ⅱ)据文献报道:Fe(CO)5催化某反应的一种反应机理如下图所示。下列叙述错误的是
A.OH-参与了该催化循环 B.该反应可产生清洁燃料H2
C.该反应可消耗温室气体CO2 D.该催化循环中Fe的成键数目发生变化
【答案】C
【解析】
题干中明确指出,铁配合物Fe(CO)5充当催化剂的作用。机理图中,凡是出现在历程中,进去的箭头表示反应物,出来的箭头表示生成物,既有进去又有出来的箭头表示为催化剂或反应条件,其余可以看成为中间物种。由题干中提供的反应机理图可知,铁配合物Fe(CO)5在整个反应历程中成键数目,配体种类等均发生了变化;并且也可以观察出,反应过程中所需的反应物除CO外还需要H2O,最终产物是CO2和H2,同时参与反应的还有OH-,故OH-也可以看成是另一个催化剂或反应条件。
A.从反应机理图中可知,OH-有进入的箭头也有出去的箭头,说明OH-参与了该催化循环,故A项正确;
B.从反应机理图中可知,该反应的反应物为CO和H2O,产物为H2和CO2,Fe(CO)5作为整个反应的催化剂,而OH-仅仅在个别步骤中辅助催化剂完成反应,说明该反应方程式为,故有清洁燃料H2生成,故 B项正确;
C.由B项分析可知,该反应不是消耗温室气体CO2,反而是生成了温室气体CO2,故 C项不正确;
D.从反应机理图中可知,Fe的成键数目和成键微粒在该循环过程中均发生了变化,故 D项正确;
答案选C。
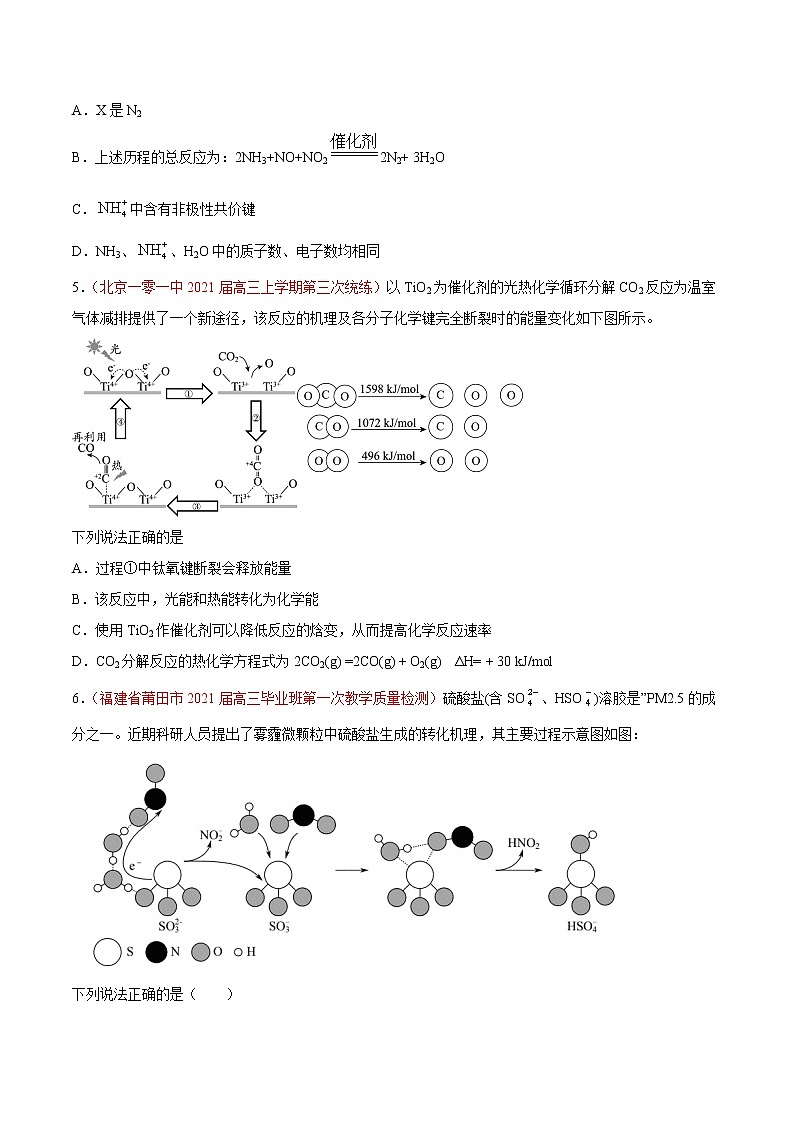
3.(2020天津卷)理论研究表明,在101kPa和298K下,异构化反应过程的能量变化如图所示。下列说法错误的是
A.HCN比HNC稳定
B.该异构化反应的
C.正反应的活化能大于逆反应的活化能
D.使用催化剂,可以改变反应的反应热
【答案】D
【解析】
A.根据图中信息得到HCN能量比HNC能量低,再根据能量越低越稳定,因此HCN比HNC稳定,故A正确;
B.根据焓变等于生成物总能量减去反应物总能量,因此该异构化反应的,故B正确;
C.根据图中信息得出该反应是吸热反应,因此正反应的活化能大于逆反应的活化能,故C正确;
D.使用催化剂,不能改变反应的反应热,只改变反应路径,反应热只与反应物和生成物的总能量有关,故D错误。
综上所述,答案为D。
4.(“皖赣联考”2021届高三上学期第三次考试)利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如下图所示,下列说法正确的是
A.X是N2
B.上述历程的总反应为:2NH3+NO+NO22N2+ 3H2O
C.中含有非极性共价键
D.NH3、、H2O中的质子数、电子数均相同
【答案】B
【详解】
A.由原子个数守恒可知,X是N2和H2O,故A错误;
B.由反应历程可知,在催化剂作用下,NH3与废气中的NO和NO2反应生成无毒的N2和H2O,反应的化学方程式为2NH3+NO+NO22N2+ 3H2O,故B正确;
C.铵根离子的电子式为,离子中含有极性共价键和配位键,不含有非极性共价键,故C错误;
D.分子是电中性的,阳离子是带正电荷的,所含的质子数、电子数不可能均相同,则NH3分子和H2O分子与离子的质子数、电子数不可能均相同,故D错误;
故选B。
5.(北京一零一中2021届高三上学期第三次统练)以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如下图所示。
下列说法正确的是
A.过程①中钛氧键断裂会释放能量
B.该反应中,光能和热能转化为化学能
C.使用TiO2作催化剂可以降低反应的焓变,从而提高化学反应速率
D.CO2分解反应的热化学方程式为2CO2(g) =2CO(g) + O2(g) ΔH= + 30 kJ/mol
【答案】B
【详解】
A. 化学键断裂需要吸收能量,过程①中钛氧键断裂会吸收能量,故A错误;
B. 根据图示,该反应中,光能和热能转化为化学能,故 B正确;
C. 催化剂通过降低反应的活化能提高化学反应速率,催化剂不能降低反应的焓变,故C错误;
D. 反应物总能量-生成物总键能=焓变,CO2分解反应的热化学方程式为2CO2(g) =2CO(g) + O2(g) ΔH=1598×2- 1072×2-496=+ 556 kJ/mol,故D错误。
6.(福建省莆田市2021届高三毕业班第一次教学质量检测)硫酸盐(含SO、HSO)溶胶是”PM2.5的成分之一。近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
下列说法正确的是( )
A.H2O没有参与该过程 B.NO2是生成硫酸盐的还原剂
C.硫酸盐气溶胶呈酸性 D.该过程中没有共价键生成
【答案】C
【详解】
A.根据图示中各微粒的构造可知,该过程有H2O参与,A错误;
B.根据图示的转化过程,NO2转化为HNO2,N元素的化合价由+4价变为+3价,化合价降低,得电子被还原,做氧化剂,则NO2的是生成硫酸盐的氧化剂,B错误;
C.硫酸盐(含SSO、HSO)气溶胶中含有HSO,转化过程有水参与,则HSO在水中可电离生成H+和,则硫酸盐气溶胶呈酸性,C正确;
D.根据图示转化过程中,由转化为HSO,根据图示对照,有硫氧共价键生成,D错误;
答案选C。
7.(广东省惠州市2021届高三上学期第一次调研)自然界中时刻存在着氮的转化。实现氮气按照一定方向转化一直是科学领域研究的重要课题,如图为N2分子在催化剂的作用下发生的一系列转化示意图。下列叙述正确的是
A.N2→NH3,NH3→NO均属于氮的固定
B.在催化剂b作用下,O2发生了氧化反应
C.使用催化剂a、b均可以提高单位时间内生成物的产量
D.催化剂a、b表面均发生了极性共价键的断裂
【答案】C
【详解】
A.把游离态的氮转化为氮的化合物,称为氮的固定, N2→NH3属于氮的固定,NH3→NO不属于氮的固定,故A错误;
B.在催化剂b作用下,O2→NO,O元素的化合价由0价变为-2价,化合价降低,发生了还原反应,故B错误;
C.催化剂可以提高化学反应速率,可以提高单位时间内生成物的产量,故C正确;
D.催化剂a作用下,N2→NH3,断裂非极性共价键N≡N键,催化剂b作用下,NH3→NO,断裂极性共价键N−H键,故D错误;
答案选C。
8.(广东省肇庆市2021届高三毕业班第一次统一检测)二氧化碳甲烷化对缓解能源危机意义重大,二氧化碳在催化剂的作用下与氢气作用制备甲烷的反应机理如下图所示。下列说法错误的是
A.Ni和是该反应的催化剂
B.的过程为放热过程
C.催化剂不能改变该反应的总体热效应
D.该反应的总反应方程式为
【答案】B
【详解】
A.由图可知该循环中Ni和是该反应的催化剂,故A正确;
B.为断键的过程,该过程为吸热过程,故B错误;
C.催化剂可以降低反应的活化能,但不能改变该反应的总体热效应,故C正确;
D.根据图中信息得到该反应的总反应方程式为,故D正确。
综上所述,答案为B。
9.(河北省“五个一名校联盟”2021届高三上学期第一次诊断)某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2和H2O的历程,该历程示意图如下(图中只画出了HAP的部分结构)。下列说法错误的是
A.HAP能提高HCHO与O2的反应速率的原因是降低了反应的活化能
B.HCHO在反应过程中,有C—H键的断裂和C=O键形成
C.根据图示信息,CO2分子中的氧原子全部来自O2
D.HCHO和CO2中碳原子的杂化方式不同
【答案】C
【详解】
A.由图示可知,HAP在反应过程中起催化剂的作用,能降低反应的活化能,加快反应速率,故A正确;
B.HCHO在反应中有C-H断裂和C=O键形成,所以甲醛被氧化生成二氧化碳和水,故B正确;
C.根据图知,CO2分子中的氧原子一部分还来自于甲醛,故C错误;
D.HCHO中C连有一个碳碳双键,采用SP2杂化,而CO2中C连有两个碳碳双键,采用SP杂化,故D正确。
答案选C。
10.(上海市虹口区2021届高三一模)异丁烯与氯化氢发生加成反应过程体系能量变化如图所示,下列叙述正确的是
A.产物②比产物①更稳定
B.此过程中只发生了非极性键的断裂
C.异丁烯与氯化氢的加成反应为吸热反应
D.1 mol 产物①或②中均含有7 mol共价键
【答案】A
【详解】
A.能量越低,物质越稳定,根据图示可知,产物②比产物①的能量更低,故产物②比产物①更稳定,A正确;
B.根据反应原理可知,反应过程中有碳碳键的断裂和氢氯键的断裂,故B错误;
C.根据图示可知,反应物的总能量高于生成物的总能量,该反应为放热反应,C错误;
D.根据产物结构式可知,1 mol 产物①或②中均含有13mol共价键,D错误;
答案选A。
11.(上海市金山区2021届高三一模)CFCl3破坏臭氧层的过程如图所示,下列说法错误的是( )
A.过程Ⅰ:断裂C-Cl键
B.过程Ⅱ:O3+Cl=ClO+O2
C.过程Ⅲ:发生了O2=O+O反应
D.整个过程中氯原子是破坏臭氧层的催化剂
【答案】C
【详解】
A.过程Ⅰ中转化为和氯原子,断裂极性键C-Cl键,故A正确;
B.根据题图信息可知,过程Ⅱ是氯原子与O3反应生成氧气和氧化氯,可用方程式表示为O3+Cl=ClO+O2,故B正确;
C.过程Ⅲ是原子结合成分子的过程中发生的反应为:,故C错误;
D.上述过程说明氟利昂中氯原子参与反应,整个反应前后仍旧为氯原子,则氯原子是破坏O3的催化剂,故D正确;
故答案为:C。
12.(上海市松江区2021届高三一模)在汽车尾气处理过程中存在反应:,该反应过程及能量变化如图所示。下列说法正确的是
A.升高温度,平衡正向移动 B.改变压强,反应速率不变
C.反应过程中吸收的热量小于放出的热量 D.使用催化剂可以有效提高反应物的平衡转化率
【答案】C
【详解】
A.由图可知,反应物总能量高于生成物总能量,正反应为放热反应,所以升高温度,平衡逆向移动,A不正确;
B.改变压强,虽然平衡不发生移动,但反应物和生成物的浓度将发生相应的改变,所以反应速率改变,B不正确;
C.因为正反应为放热反应,所以反应物转化为生成物的过程中,吸收的热量小于放出的热量,C正确;
D.使用催化剂可以提高反应速率,缩短反应到达平衡的时间,但不能使平衡发生移动,不能改变反应物的平衡转化率,D不正确;
故选C。
13.(四川省乐山市2021届高三12月第一次调研)磁性纳米Fe3O4颗粒具有超顺磁性,做固相萃取剂时能很好从水体中分离。我国科学家利用这一特性,研究出在纳米Fe3O4外包覆多巴胺聚合层,除去水体污染物多环芳烃的方法,模拟过程如下,下列有关说法正确的是
A.Fe3O4是一种碱性氧化物
B.Fe3O4纳米颗粒粒径越小、水体pH越小除污效果越好
C.多环芳烃在乙腈中的溶解度小于在聚多巴胺中的溶解度
D.处理完成后,Fe3O4纳米颗粒可利用磁铁回收,经加热活化可重复使用
【答案】D
【详解】
A.Fe3O4不是碱性氧化物,碱性氧化物定义是与酸反应生成盐和水的氧化物,四氧化三铁和酸反应生成两种盐,故A错误;
B.水体pH越小,酸性越强,则Fe3O4会与酸反应,则会失去除污效果,故B错误;
C.根据题中信息,乙腈萃取了多环芳烃,说明多环芳烃在乙腈中的溶解度大于在聚多巴胺中的溶解度,故C错误;
D.处理完成后,Fe3O4纳米颗粒具有磁性,可以利用磁铁回收,经加热活化可重复使用,故D正确。
综上所述,答案为D。
14.(浙江省重点中学2021届高三11月选考模拟)三级溴丁烷在乙醇中溶剂解的反应进程中的能量变化如图所示。下列说法错误的是
A.三级溴丁烷在乙醇中溶剂解的总反应速率由反应 III决定
B.三级溴丁烷在乙醇中溶剂解的总反应属于取代反应
C.若三级氯丁烷在乙醇中发生相似的溶剂解,则反应I 的焓变△H1 将增大
D.适当升温,三级溴丁烷在乙醇中溶剂解正反应速率的增大程度小于其逆反应速率的增大程度
【答案】A
【详解】
A.总反应的速率有慢反应,反应I的正反应活化能最大,反应速率最慢,即三级溴丁烷在乙醇中溶剂解的总反应速率由反应I决定,故A错误;
B.三级溴丁烷在乙醇中溶剂解的总反应为(CH3)3CBr +CH3CH2OH→(CH3)3COCH2CH3+HBr,反应类型为取代反应,故B正确;
C.氯的非金属性比溴强,C-Cl键比C-Br键稳定,说明起始时三级氯丁烷的能量比三级溴丁烷能量低,则三级氯丁烷反应I 的焓变△H1 比三级溴丁烷反应I 的焓变△H1 大,故C正确;
D.总反应为放热反应,升高温度,平衡逆移动,则适当升温,三级溴丁烷在乙醇中溶剂解正反应速率的增大程度小于其逆反应速率的增大程度,故D正确;
故答案为D。
15.(福建省宁德市2021届普通高中毕业班第一次质量检查)在金属Pt、Cu和Ir(铱)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮()以达到消除污染的目的,其工作原理如图所示。下列说法错误的是( )
A.Ir表面反应的反应物是H2和N2O气体
B.导电基体中Pt上既发生氧化反应又发生还原反应
C.若导电基体上只有Cu,难以消除含氮污染物
D.若导电基体上的Cu颗粒增多,能提高硝态氮()的平衡转化率
【答案】D
【详解】
A.根据图像可知,Ir表面反应的反应物是H2和N2O气体,生成物为N2和H2O,A说法正确;
B.导电基体中Pt上氢气失电子生成氢离子,发生氧化反应,NO得电子生成N2O,硝酸根离子得电子生成NO,发生还原反应,则Pt上既发生氧化反应又发生还原反应,B说法正确;
C.根据图像可知,硝酸根离子得电子与氢离子反应生成氮的氧化物和水,则若导电基体上只有Cu,氢气不能失电子生成氢离子,难以消除含氮污染物,C说法正确;
D.若导电基体上的Cu颗粒增多,消耗硝酸根离子的速率增大,但对硝态氮()的平衡转化率无影响,D说法错误;
答案为D。
热点06 化学反应机理(反应历程)图像分析-2024年高考化学【热点·重点·难点】专练(新高考专用): 这是一份热点06 化学反应机理(反应历程)图像分析-2024年高考化学【热点·重点·难点】专练(新高考专用),文件包含热点06化学反应机理反应历程图像分析-2024年高考化学热点·重点·难点专练新高考专用原卷版docx、热点06化学反应机理反应历程图像分析-2024年高考化学热点·重点·难点专练新高考专用解析版docx等2份试卷配套教学资源,其中试卷共68页, 欢迎下载使用。
重点2 氧化还原反应- 高考化学专练【热点·重点·难点】: 这是一份重点2 氧化还原反应- 高考化学专练【热点·重点·难点】,文件包含重点2氧化还原反应-高考化学专练热点·重点·难点解析版doc、重点2氧化还原反应-高考化学专练热点·重点·难点原卷版doc等2份试卷配套教学资源,其中试卷共15页, 欢迎下载使用。
重点1 离子反应- 高考化学专练【热点·重点·难点】: 这是一份重点1 离子反应- 高考化学专练【热点·重点·难点】,文件包含重点1离子反应-高考化学专练热点·重点·难点解析版doc、重点1离子反应-高考化学专练热点·重点·难点原卷版doc等2份试卷配套教学资源,其中试卷共15页, 欢迎下载使用。












