




2022年中考化学第一轮系统复习第七讲溶液课时1溶液的形成及定量表示课件PPT
展开这是一份2022年中考化学第一轮系统复习第七讲溶液课时1溶液的形成及定量表示课件PPT,共53页。PPT课件主要包含了一定温度,不能继续,还能继续,饱和溶液,增加溶剂,增加溶质,混合物,均一性,稳定性,无明显变化等内容,欢迎下载使用。
饱和溶液与不饱和溶液(烟台2考,淄博:2018.14)
1.概念(1)饱和溶液:在__________下,在一定量的溶剂里_________溶解某种溶质的溶液。(2)不饱和溶液:在一定温度下,在一定量的溶剂里__________溶解某种溶质的溶液。
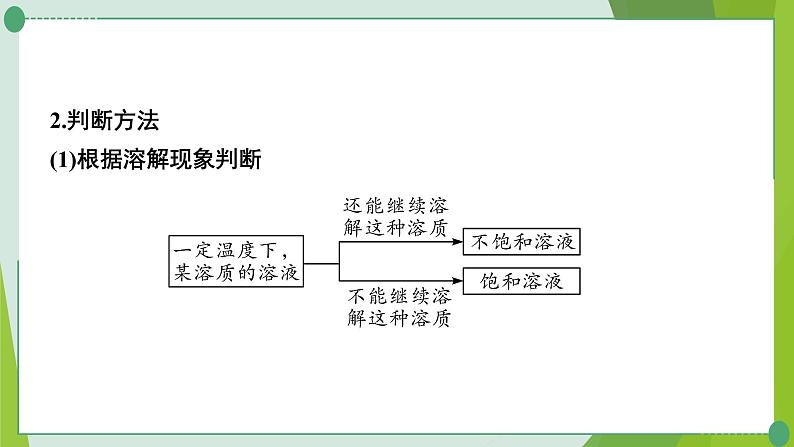
2.判断方法(1)根据溶解现象判断
(2)根据析出固体情况判断①有固体析出,则溶液为该温度下该物质的__________;②无固体析出,溶液有两种情况:a. 该温度下该物质的恰好饱和溶液;b. 该温度下该物质的不饱和溶液。
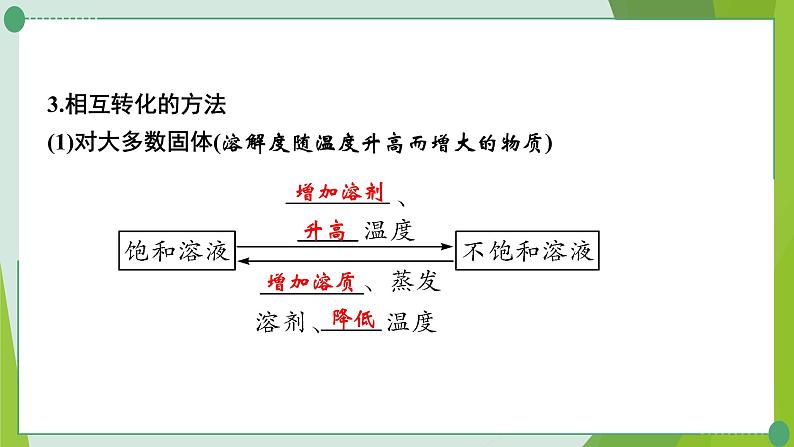
3.相互转化的方法(1)对大多数固体(溶解度随温度升高而增大的物质)
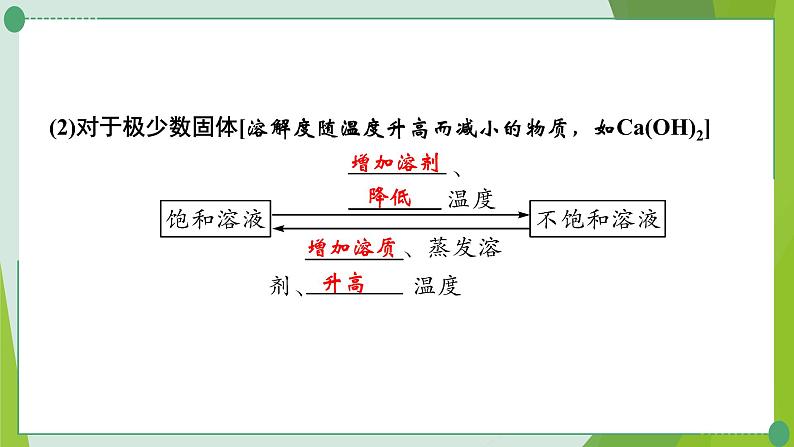
(2)对于极少数固体[溶解度随温度升高而减小的物质,如Ca(OH)2]
溶解过程、乳化现象(烟台4考,淄博:2019.10,东营3考,济宁:2018.15)
2.溶解过程中的吸放热现象(1)溶解的过程:所有溶质分散到溶剂中形成溶液的过程均会发生两种变化:扩散过程,此过程______热量;水合过程,此过程______热量。(2)物质溶解过程中通常伴随着________的变化。
几种常见物质在水中溶解时溶液温度的变化
3.乳化现象(1)定义:洗洁精、洗衣粉和洗发液等物质可以使食用油以_________的形态分散在水中,形成不易分层、比较稳定的混合物的现象。
(2)溶解、乳化、化学反应的去污原理比较
配制一定溶质质量分数的溶液(详见实验突破栏目)
注:判断下列有关说法是否正确,正确的打“√”,错误的打“×”。(1)一种溶液中可以存在多种溶质,但只能有一种溶剂( )(2)硝酸钾的饱和溶液不能再继续溶解其他溶质( )(3)饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液( )(4)析出晶体后的溶液一定是该物质在该温度下的饱和溶液( )(5)有晶体析出的溶液溶质质量分数一定减小( )
(6)硝酸铵固体溶于水形成溶液仅发生扩散吸热的过程( )(7)溶液具有均一性和稳定性,是因为溶液中的各种粒子都静止不动( )(8)溶液是均一、稳定的混合物,所以均一、稳定的物质就是溶液( )(9)饱和溶液降温一定有晶体析出( )
溶液组成的定量表示[烟台:2019.5D,东营:2017.11(3),济宁:2018.6]
1.溶质质量分数(1)概念:溶质质量分数是溶质与溶液的质量之比。
1. 实验用品(1)仪器:托盘天平、烧杯、________、药匙、量筒(10、100 mL)。(2)药品:氯化钠、蒸馏水。2. 实验装置及流程
配制一定溶质质量分数的溶液(烟台4考,东营2考)
3. 实验步骤(烟台:2020.2D)(1)用固体药品配制溶液(配制80 g溶质质量分数为10%的氯化钠溶液)
(2)用浓溶液配制稀溶液用配制好的10%的氯化钠溶液(密度约为1.04 g/cm3 )配制80 g质量分数为5%的氯化钠溶液①计算:所需质量分数为10%的氯化钠溶液_____g(体积约为_____mL),水____g。公式:根据稀释前后_________不变,则浓溶液的质量=
水的质量=稀溶液的质量-浓溶液的质量浓溶液的体积=②量取;③混匀;④装瓶。
【特别提醒】溶液配制完后,在转移过程中,若将溶液洒出,溶质质量分数不发生改变。
例 如图是配制50 g溶质质量分数为6%的氯化钠溶液的操作图。回答下列问题:(1)配制溶液过程中所需的玻璃仪器有玻璃棒、_____________________,其中玻璃棒的作用是________________。
(2)需配制的溶液中溶质和溶液的质量比为_______。(3)图中操作不规范的步骤是________(填序号); 将图中的不规范操作改正后,图示实验的正确操作顺序是_____________。
(4)量取水时,应选择____mL的量筒最合适,读数时视线应与__________________________保持水平。(5)将配制好的溶液存放在_______(填“广口瓶”或 “细口瓶”)后贴上标签,在标签上填写:________________。
(6)在其他操作无误的前提下,用量筒量取水时按图所示操作,会使所配制溶液的溶质质量分数______(填“偏大”“偏小”或“不变”)。(7)称量氯化钠时如果发现指针偏向右侧,正确的操作是___________________,如果称量时氯化钠和砝码位置放反了,其它操作步骤均正确,则所配置的溶液的溶质质量分数_____(填“大于”“等于”或“小于”)20%。(8)取配制好的该溶液10 g,将其配制成3%的溶液,需要水的质量为____g。
(9)[偏差分析](2019山西)配制50 g质量分数为5%的KNO3溶液,作为无土栽培所需的营养液。溶解过程中KNO3的质量分数随时间的变化关系如图所示,观察图像,分析形成这种结果的原因是____(填字母序号)。A. 所用KNO3固体中含有水分B. 量筒量水时俯视刻度线C. KNO3固体溶解前所用烧杯内有水D. 配好的溶液装瓶时部分液体洒落到试剂瓶外
1. [2020日照14(4)题2分]如图所示,20 ℃时,将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是_____(填写字母标号)。①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体A. ①③④ B. ②⑤⑥C. ①③⑤ D. ②④⑥
物质溶解时的吸放热现象(烟台:2020.13B)
若加入某物质后,发现试管中未溶解的固体增多,该物质是_____(填字母序号)。
2. (2019德州21题6分)将NaOH、NaCl、NH4NO3固体各10 g分别放入盛有100 mL水的烧杯中充分溶解。在不同时间测量溶液的温度,绘制成如图图像:
分析图像,回答问题:(1)在NaOH、NaCl、NH4NO3三种物质中,溶解时出现吸热现象的是________________(写名称)。(2)对NaOH而言,a点右侧曲线表示:在一定时间段内,溶液温度随时间推移而________(填“升高”或“降低”),其原因是______________________。
3. 向下列物质中分别加入适量水,充分搅拌,不能得到溶液的是( )A. 硝酸钾 B. 蔗糖 C. 花生油 D. 酒精
4. 下列与洗涤有关的做法不合理的是( )A. 用洗洁精洗去餐具上的油污B. 用汽油洗去沾在衣服上的油渍C. 用白醋洗去水壶中的水垢(水垢的主要成分是碳酸钙和氢氧化镁)D. 用纯碱溶液洗去铁制品表面的铁锈
5. 胆矾晶体放置在空气中不能溶解,在水中能溶解得到蓝色溶液。下列说法正确的是( )A. 胆矾晶体溶于水得到的溶液,溶质是胆矾B. 胆矾晶体在水中获得能量,在空气中没有能量C. 胆矾晶体在水中能解离成离子,扩散到水中形成溶液D. 胆矾晶体在水中与水分子有相互作用,在空气中与空气中的分子无相互作用
6. (山东真题组合)对下列有关溶液的说法进行判断,正确的打“√”,错误的打“×”。(1)物质的溶解过程通常会伴随着能量的变化(青岛:2017.15B)( )(2)溶液是溶质的粒子分散在溶剂中形成的均一、稳定的混合物(青岛:2020.17A)( )(3)溶液中各部分的性质相同[淄博:2018.20(1)A]( )(4)外界条件不改变,溶质不会从溶液中分离出来(青岛:2017.15A)( )
7. (2018济宁15题2分)洗洁精是家庭必备的清洁用品,可迅速分解油腻、去污、除菌,有味道淡雅、洁净温和、泡沫柔细、低残留的优点。洗洁精的有效成分是表面活性剂,还含有泡沫剂、香精、水、色素等多种成分。请回答:(1)洗洁精去除油污的有效成分是__________。(2)洗洁精去除油污的原理是__________。
8. (山东真题组合)判断下列说法是否正确,正确的打“√”,错误的打“×”。(1)饱和溶液不一定比不饱和溶液溶质多(聊城:2019.2C)( )(2)NaCl的饱和溶液不能再溶解KNO3(莱芜:2017.3B)( )(3)饱和溶液溶质的质量分数一定大于不饱和溶液溶质的质量分数(烟台:2019.5D)( )
饱和溶液与不饱和溶液((烟台2考,淄博:2018.14)
(4)升高温度可使大多数固体物质的饱和溶液变为不饱和溶液(滨州:2020.4C)( )(5)浓溶液不一定是饱和溶液[淄博:2018.20(1)C]( )(6)饱和溶液就是不能再溶解任何物质的溶液(烟台:2021.5D)( )
9. (2021济宁6题2分)为探究硝酸钾的溶解性,进行了下面实验(见图Ⅰ),结合KNO3溶解度曲线(见图Ⅱ)判断,
下列说法错误的是( )A. 溶液②、溶液④一定是饱和溶液B. 溶液①、溶液③一定是不饱和溶液C. 溶液②、溶液③的质量:③>②D. 溶液②、溶液③、溶液④的溶质质量分数:③>②=④
10. [2020泰安22(3)题2分]在某温度下,分别向盛有等质量蒸馏水的两烧杯中逐渐加入固体溶质甲和乙,图中x表示所加固体的质量,y表示溶液中溶质与水的质量比。a点对应的乙物质的溶液为________(选填“饱和”或“不饱和”)溶液;该温度时甲物质的溶解度为_____g。
11. (2021东营19题9分)实验室常用溶质质量分数为10%的过氧化氢溶液制取氧气。
溶质质量分数的计算[烟台:2019.5D,东营:2017.11(3),济宁:2018.6]
(1)某兴趣小组打算用如图所示的整瓶溶液配制溶质质量分数为10 %的过氧化氢溶液,需加水______g。(2)在配制过程中,他们发现试剂瓶内壁附着不少气泡,由此推断该瓶过氧化氢溶液的溶质质量分数小于30%,依据是__________________________________。
过氧化氢溶液常温下即可分解产生氧气
(3)为测定该瓶溶液的溶质质量分数,他们取35 g该溶液放入锥形瓶中并加入一定量的二氧化锰。不同时间电子秤的读数如下表所示(不考虑H2O逸出):
请回答:①反应生成氧气的总质量为________g。②该瓶过氧化氢溶液的溶质质量分数是多少? (写出计算过程,结果保留到0.1%)
12. (2020泰安17题1分)农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100 g该溶液的过程如下图所示。下列说法不正确的是( )A. 实验操作顺序为④②①⑤③B. ②中需称量NaCl的质量为16.0 gC. 选用100 mL量筒量取所需水的体积D. 用量筒量取水时仰视读数所得溶液的溶质质量分数偏大
溶液的配制(烟台4考,东营2考)
13. (2018滨州11题3分)小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的称量氯化钠、量取水的操作规程进行操作(图示为小芳操作时的读数,其它操作都正确)。小芳实际配制的氯化钠溶液的溶质质量分数(水的密度为1 g/cm3)约为( )A. 12.4% B. 17.2%C. 16.9% D. 12.5%
14. (2019滨州3题3分)某同学选用氢氧化钠固体与水配制20 g溶质质量分数为10%的氢氧化钠溶液,下列说法错误的是( )①需称取氢氧化钠固体2.0 g②称量前托盘天平应先检查游码是否归零,并调节平衡③用托盘天平称量氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量④选用250 mL量筒量取18 mL的水⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配制溶液封存A. ①④ B. ③④⑤C. ④⑤ D. ②③⑤
(1)若配制上述氢氧化钠溶液的过程中,量取水时俯视读数,会使配制的溶液溶质质量分数______(填“偏大”“偏小”或“不变”)。(2)用上述配制好的氢氧化钠溶液配制质量分数为5%的氢氧化钠溶液,则配制的氢氧化钠溶液的质量为____ g,需加入水的质量为____ g。
15. [2020威海11(5)题2分]配制1 L溶质质量分数为0.5%的过氧乙酸溶液。现有以下物品:水、溶质质量分数20%的过氧乙酸溶液、量筒(规格分别为1000 mL、50 mL)、塑料桶、铁桶、木棍、口罩、护目镜、橡皮手套。①需要20%的过氧乙酸溶液_____mL(计算时,将水、20%和0.5%过氧乙酸溶液的密度都近似为1 g/cm3)。②戴好防护用品,用_____mL量筒量取所需20%的过氧乙酸溶液倒入塑料桶中,按比例兑水,用木棍搅拌后,盖好桶盖备用。
16. (2019威海9题2分)下列关于溶液的说法错误的是( )A. 与乳化作用相比,溶解能使物质混合得更均匀B. 20 ℃时,50 g水中溶解了15 g硝酸钾,则20 ℃时硝酸钾的溶解度是30 gC. 一定温度下,固体物质的溶解度不随水的质量改变而改变D. 硝酸钾的饱和溶液恒温蒸发部分水后,剩余溶液溶质质量分数不变
17. (2017聊城4题2分)下列关于溶液说法正确的是( )A. 把氯化钠和植物油放入水中,充分搅拌后都能形成溶液B. 把20%的蔗糖溶液均分成两份,每份溶液的溶质质量分数为10%C. 向20 ℃时的蔗糖饱和溶液中加入食盐,食盐不再溶解D. 配制50 g 16%的氯化钠溶液一般经过计算、称量(或量取)、溶解、装瓶存放等步骤
18. (2018淄博19题4分)溶液对于自然界中的生命活动和人类生产活动具有重要的意义,多角度认识溶液有助于指导我们的生活。(1)关于溶液的说法,正确的是____(填写标号)。A. 溶液中各部分的性质相同B. 均一、稳定的液体一定是溶液C. 浓溶液不一定是饱和溶液D. 溶液加水稀释后溶质的质量变小
(2)表Ⅰ是部分物质在20 ℃时的溶解性,表Ⅱ是氯化钠、碳酸钠在不同温度时的溶解度。
表Ⅰ空格中应填写_____;分析表Ⅱ可知,氯化钠和碳酸钠的饱和溶液溶质质量分数相同时的温度是________。
相关课件
这是一份初中化学鲁教版九年级上册第二节 溶液组成的定量表示公开课ppt课件,文件包含第三单元第二节第1课时课件PPTpptx、第三单元第二节第1课时教案含练习docx等2份课件配套教学资源,其中PPT共16页, 欢迎下载使用。
这是一份鲁教版 (五四制)九年级全册1 溶液的形成复习课件ppt,共56页。PPT课件主要包含了分子或离子,一种或几种,硝酸铵,氢氧化钠,氯化钠,洗洁精,洗衣粉,洗发液,细小液滴,纯碱或氢氧化钠等内容,欢迎下载使用。
这是一份2022年中考化学第一轮系统复习第五讲定量研究化学反应课件PPT,共58页。PPT课件主要包含了化学式,化学反应,2意义,客观事实,质量守恒定律,2最小公倍数法,元素种类,元素质量,原子种类,原子数目等内容,欢迎下载使用。












