

- 专题05 非金属及其化合物(基础卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(原卷版) 试卷 1 次下载
- 专题05 非金属及其化合物(提升卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(解析版) 试卷 1 次下载
- 专题06 金属及其化合物(基础卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(解析版) 试卷 1 次下载
- 专题06 金属及其化合物(基础卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(原卷版) 试卷 1 次下载
- 专题06 金属及其化合物(提升卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(解析版) 试卷 1 次下载
专题05 非金属及其化合物(提升卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(原卷版)
展开2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)
专题05 非金属及其化合物(提升卷)
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
第Ⅰ卷(选择题)
一、选择题(每小题3分,共48分)
1. (2019·河北省沧州市·月考试卷)天然气因含有少量H2S等气体开采应用受限。T.F菌在酸性溶液中可实现天然气的催化脱硫,其原理如图所示。下列说法错误的是( )
A. 该脱硫过程需要不断添加Fe2(SO4)3溶液
B. 脱硫过程O2间接氧化H2S
C. 亚铁是血红蛋白重要组成成分,FeSO4可用于治疗缺铁性贫血
D. 天然气脱硫具有保护环境、保护设备、管线免受腐蚀的作用
2. (2021·云南省·月考试卷)化学在生产生活和科学研究中具有重要的作用.下列说法正确的是( )
①硅石的主要成分是二氧化硅
②三峡大坝使用了大量水泥,水泥是硅酸盐材料
③嫦娥二号卫星上所用的太阳能电池采用硅材料制作,太阳能电池在生活中的应用有利于环保、节能
④二氧化硅的熔点高,硬度大,可用来制造电子部件和光学器件
⑤水晶项链和餐桌上的瓷盘都是硅酸盐制品.
A. ①②③ B. ②④⑤ C. ③④⑤ D. ①②③④
3. (2021·湖北省黄石市·月考试卷)结合氮及其化合物“价一类”二维图及氧化还原反应的基本规律,下列分析或预测正确的是( )
A. N2O3、NO2、N2O5均能与水反应生成酸,三者均为酸性氧化物
B. HNO3、HNO2、NaNO3、NH3的水溶液均可以导电,四者均属于电解质
C. 联氨(N2H4)可能被亚硝酸(HNO2)氧化生成氢叠氮酸HN3
D. 硝酸具有较强的氧化性,可用稀硝酸溶解Au、Ag、Cu
4. (2021·山西省·单元测试)下列有关硅及其化合物的说法中正确的是( )
A. 硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中
B. 反应①Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓,反应②Na2CO3+SiO2Na2SiO3+CO2↑,两反应是相互矛盾的,不可能都发生
C. 普通玻璃、石英玻璃、水泥等均属于硅酸盐材料
D. 虽然SiO2能与HF、NaOH反应,但SiO2不是两性氧化物
5. (2021·河南省焦作市·期中考试)实验室用O2氧化NH3制备硝酸的装置如图所示(夹持装置略),下列说法不正确的是 ( )
A. 球形干燥管B中可以填充碱石灰或五氧化二磷
B. 实验过程中,若熄灭酒精灯,装置C中的氧化铬继续保持红热,说明装置C中的反应放热
C. 球形干燥管D中的无水氯化钙可吸收尾气中的氨气和水蒸气
D. 装置E中的石蕊试液最终变红,说明锥形瓶中有硝酸产生
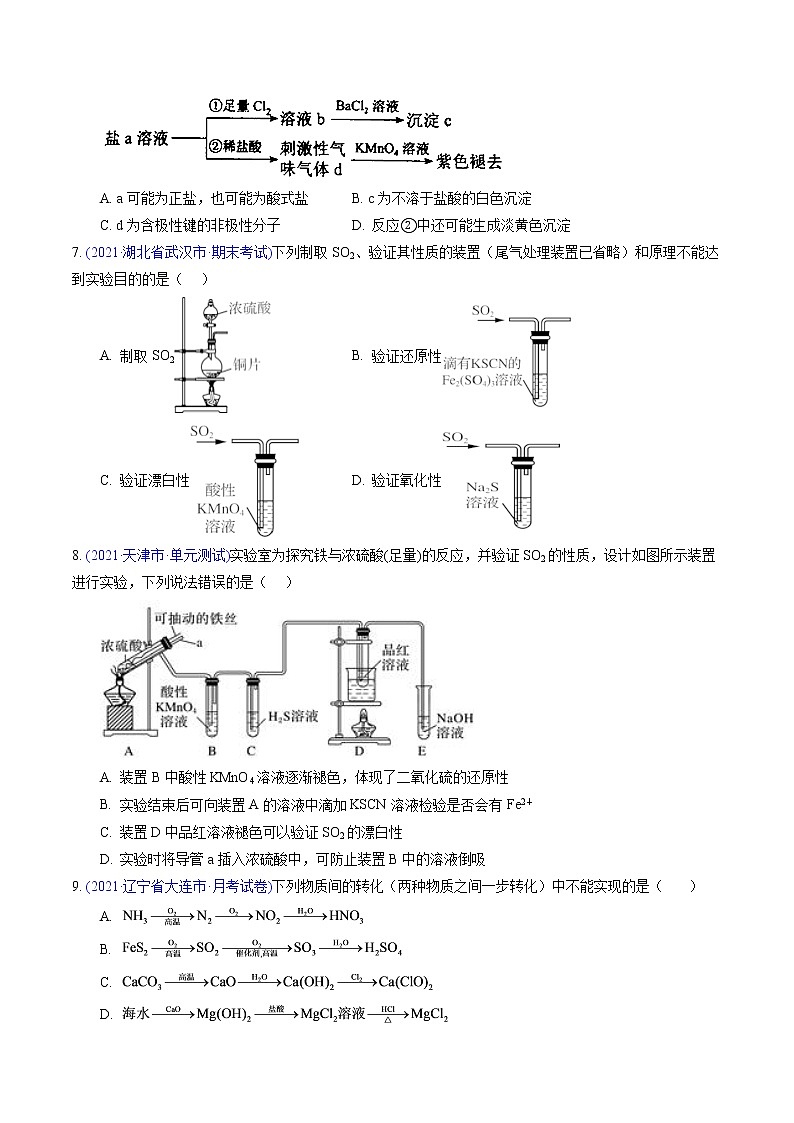
6. (2021·辽宁省·历年真题)含S元素的某钠盐a能发生如图转化。下列说法错误的是( )
A. a可能为正盐,也可能为酸式盐 B. c为不溶于盐酸的白色沉淀
C. d为含极性键的非极性分子 D. 反应②中还可能生成淡黄色沉淀
7. (2021·湖北省武汉市·期末考试)下列制取SO2、验证其性质的装置(尾气处理装置已省略)和原理不能达到实验目的的是( )
A. 制取SO2 B. 验证还原性
C. 验证漂白性 D. 验证氧化性
8. (2021·天津市·单元测试)实验室为探究铁与浓硫酸(足量)的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法错误的是( )
A. 装置B中酸性KMnO4溶液逐渐褪色,体现了二氧化硫的还原性
B. 实验结束后可向装置A的溶液中滴加KSCN溶液检验是否会有Fe2+
C. 装置D中品红溶液褪色可以验证SO2的漂白性
D. 实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
9. (2021·辽宁省大连市·月考试卷)下列物质间的转化(两种物质之间一步转化)中不能实现的是( )
A.
B.
C.
D.
10. (2021·全国·单元测试)某无色混合气体,可能含有CO、H2、SO2、Cl2、HCl中的一种或几种,把此混合气体通过少量澄清石灰水,无沉淀生成;再通过少量品红溶液,完全褪色;随后将该气体通过足量的氢氧化钠溶液后,再通过足量红热的CuO粉末,粉末变成红色;最后通入CaCl2溶液中,无沉淀生成,则下列关于此混合气体的叙述正确的是( )
A. 澄清石灰水中无沉淀,说明一定不含有SO2
B. 品红褪色,可能是Cl2导致的
C. 氧化铜粉末变红,说明CO和H2中至少有一种
D. CaCl2溶液中无沉淀,说明通过CuO后得到的气体中一定不含有CO2
11. (2021·广东省·专项测试)通过一步反应不能直接完成的是( )
①N2→NO2 ②NO2→NO ③NH3→NO ④NH3→N2
⑤Cu→Cu(NO3)2 ⑥HNO3→NO2
A. ①④ B. ②⑤ C. ③④⑥ D. ①
12. (2021·安徽省·单元测试)下列从海洋中获取物质的方案不合理的是( )
A. 粗盐先通过除杂、精制得到饱和食盐水,然后电解得到氯气,最后和石灰乳反应制得漂白粉
B. 苦卤酸化后通入氯气得到溴水,然后用热空气将其通入到水溶液中,最后通入氯气后蒸馏得粗溴
C. 干海带灼烧后加水浸取,然后加入得到碘水,最后通过萃取、分液、蒸馏得到碘单质
D. 向海水中加入石灰乳得到,加入盐酸得到溶液,最后电解该溶液得到镁单质
13. (2021·安徽省蚌埠市·单元测试)由下列实验操作、实验现象得出的实验结论错误的是( )
选项 | 实验操作 | 实验现象 | 实验结论 |
A、 | 将浓硫酸加入蔗糖中并搅拌 | 蔗糖逐渐变黑,形成“黑面包”并伴有刺激性气味的气体产生 | 体现了浓硫酸的脱水性和氧化性 |
B、 | 将铁片和锌粉分别加入到同浓度的稀盐酸中 | 产生气泡的速度:锌粉>铁片 | 活泼性:锌>铁 |
C、 | 将SO2通入含HCl、BaCl2的FeCl3溶液中 | 有白色沉淀产生 | SO2具有还原性 |
D、 | 将Cl2依次通过干燥有色布条和湿润有色布条 | 干燥有色布条不褪色,湿润有色布条褪色 | Cl2没有漂白性,Cl2与H2O反应的产物有漂白性 |
A. A B. B C. C D. D
14. (2021·天津市·单元测试)向CuSO4溶液中逐渐加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色;再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色,下列分析正确的是( )
A. 滴加KI溶液时,转移2 mole-时生成1 mol白色沉淀
B. 上述实验条件下,物质的氧化性:Cu2+>I2>SO2
C. 通入SO2时,SO2与I2反应,I2作还原剂
D. 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性
15. (2021·福建省厦门市·月考试卷)表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )
选项 | X | Y | Z |
A | SiO2 | Na2SiO3 | H2SiO3 |
B | NaCl | NaHCO3 | Na2CO3 |
C | N2 | NO2 | HNO3 |
D | C | CO | CO2 |
A. A B. B C. C D. D
16. (2020·山东省德州市·月考试卷)漂白粉和漂粉精是常用的消毒清洁用品,有效成分均为Ca(ClO)2,相应的生产流程如图。下列说法不正确的是( )
A. ①中阳极的电极反应式为2Cl--2e-=Cl2↑
B. ②中反应的化学方程式为2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
C. 上述过程涉及氧化还原反应、化合反应、复分解反应
D. 制备漂粉精过程中,Cl2转化为Ca(ClO)2时,Cl的原子利用率为100%
第Ⅱ卷(非选择题)
二、非选择题(共52分)
17. (2021·山东省济宁市·月考试卷)下列A~J十种物质之间的转化关系如图所示,其中部分生成物或反应条件已略去A为正盐;常温、常压下,B、C、D、E、G、H、I均为气体,其中D、G、H为单质,H为黄绿色气体,I通常为红棕色气体,I的相对分子质量比E的大16:F在常温下是一种无色液体;G能在H中燃烧,发出苍白色火焰,产物C易溶于水;是一元含氧强酸。
回答下列问题:
(1)A的化学式为______。
(2)一定条件下,B和D反应生成E和F的化学方程式为__________________。
(3)J和金属Cu反应生成E的化学方程式为__________________。
(4)H和石灰乳反应的化学方程式为__________________。
(5)在I和F的反应中,氧化剂和还原剂的质量之比为____________。
18. (2021·全国·历年真题)化学小组实验探究SO2与AgNO3溶液的反应。
(1)实验一:用如下装置(夹持、加热仪器略)制备SO2,将足量SO2通入AgNO3溶液中,迅速反应,得到无色溶液A和白色沉淀B。
①浓H2SO4与Cu反应的化学方程式是_____________________________。
②试剂a是____________。
(2)对体系中有关物质性质分析得出:沉淀B可能为Ag2SO3、Ag2SO4或二者混合物。(资料:Ag2SO4微溶于水;Ag2SO3难溶于水)
实验二:验证 B的成
①写出Ag2SO3溶于氨水的离子方程式:__________________________。
②加入盐酸后沉淀D大部分溶解,剩余少量沉淀F。推断D中主要是BaSO3,进而推断B中含有Ag2SO3。向滤液E中加入一种试剂,可进一步证实B中含有Ag2SO3。所用试剂及现象是___________________。
(3)根据沉淀F的存在,推测的产生有两个途径:
途径1:实验一中,SO2在AgNO3溶液中被氧化生成Ag2SO4,随沉淀B进入D。
途径2:实验二中,被氧化为进入D。
实验三:探究的产生途径
①向溶液A中滴入过量盐酸,产生白色沉淀,证明溶液中含有________,取上层清液继续滴加BaCl2溶液,未出现白色沉淀,可判断B中不含Ag2SO4。做出判断的理由:_____________________。
②实验三的结论:____________________________________________。
(4)实验一中SO2与AgNO3溶液反应的离子方程式是_____________________。
(5)根据物质性质分析,SO2与AgNO3溶液应该可以发生氧化还原反应。将实验一所得混合物放置一段时间,有Ag和生成。
(6)根据上述实验所得结论:___________________________________。
19. (2021·全国·历年真题)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
(1)I2的一种制备方法如图所示:
①加入Fe粉进行转化反应的离子方程式为______________________________,生成的沉淀与硝酸反应,生成______后可循环使用。
②通入Cl2的过程中,若氧化产物只有一种,反应的化学方程式为__________________;若反应物用量比=1.5时,氧化产物为___________;当>1.5后,单质碘的收率会降低,原因是________________。
(2)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2。上述制备I2的总反应的离子方程式为_______________________________。
(3)KI溶液和CuSO4溶液混合可生成CuI沉淀和I2,若生成1mol I2,消耗的KI至少为_________mol。I2在KI溶液中可发生反应:I2+I-I3-。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是 ____________________________________。
20. (2021·江苏省泰州市·同步练习)皮革厂的废水中含有一定量的氨氮(以NH3、NH形式存在),通过沉淀和氧化两步处理后可使水中氨氮达到国家规定的排放标准。
(1)沉淀:向酸性废水中加入适量Fe2(SO4)3溶液,废水中的氨氮转化为NH4Fe3(SO4)2(OH)6沉淀。
①该反应的离子方程式为 。
②废水中氨氮去除率随pH的变化如图-1所示,当1.3< pH<1.8时,氨氮去除率随pH升高而降低的原因是 。
(2)氧化:调节经沉淀处理后的废水pH约为6,加入NaClO溶液进一步氧化处理。
①NaClO将废水中的氨氮转化为N2,该反应的离子方程式为 。
②研究发现,废水中氨氮去除率随温度升高呈先升后降趋势。当温度大于30℃时,废水中氨氮去除率随着温度升高而降低,其原因是 。
③n(ClO-)/n(氨氮)对废水中氨氮去除率和总氮去除率的影响如图-2所示。
当n(ClO-)/n(氨氮)>1.54后,总氮去除率下降的原因是 。
21. (2021·湖北省·模拟题)多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制品的主要原料。
(1)已知多晶硅第三代工业制取流程如图1所示。
| 发生的主要反应 |
电弧炉 | SiO2+2CSi+CO↑ |
流化床 | Si+3HCl SiHCl2+H2 |
①物质Z的名称是______。
②用石英砂和焦在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为 ____________。
③在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和 __________________________。
物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
沸点/C | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
(2)利用晶体硅的粉末与干燥的氮气在1300~1400℃下反应,可制取结构陶瓷材料氮化硅(Si3N4)。现用如图所示装置(部分仪器已省略)制取少量氮化硅。
①装置Ⅱ中所盛试剂为______。
②装置Ⅰ和装置Ⅲ均需要加热,实验中应先_______。(填“Ⅲ”或“Ⅰ”)的热源。
(3)由晶体硅制成的n型半导体、p型半导体可用于太阳能电池。一种太阳能储能电池的工作原理如图2所示,已知锂离子电池的总反应为:Li1-xNiO2+xLiC6LiNiO2+xC6。完成下列问题。
①该锂离子电池充电时,n型半导体作为电源______(填“正”或“负”)极。
②该锂离子电池放电时,b极上的电极反应式为________________________。
专题09 物质结构与性质(提升卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(原卷版): 这是一份专题09 物质结构与性质(提升卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(原卷版),共13页。试卷主要包含了选择题的作答,非选择题的作答等内容,欢迎下载使用。
专题05 非金属及其化合物(提升卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(解析版): 这是一份专题05 非金属及其化合物(提升卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(解析版),共20页。试卷主要包含了选择题的作答,非选择题的作答等内容,欢迎下载使用。
专题05 非金属及其化合物(基础卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(解析版): 这是一份专题05 非金属及其化合物(基础卷)-2022届高三化学【精准提升·二轮】专题训练卷(新高考专用)(解析版),共20页。试卷主要包含了选择题的作答,非选择题的作答等内容,欢迎下载使用。












