



精品解析:2020年广西梧州市中考二模化学试题(解析版+原卷版)
展开2020年梧州市初中学考第二次抽样调研测试
化学(试题卷)
说明:1.本试卷共8页(试题卷6页,答题卡2页),满分100分,考试时间90分钟。
2.答题前,请将准考证号、姓名、座位号写在答题卡指定位置,答案涂、写在答题卡相应的区域内,在试题卷上答题无效。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Ca-40
第I卷(选择题,共60分)
一、选择题(本题含20小题,每小题3分,共60分。每小题只有一个符合题意的选项)
1. 保护地球是我们每个公民应尽的义务和责任,下列举措不符合这一主题的是( )
A. 使用节能电器
B. 减少使用一次性餐盒
C. 回收废旧电池
D. 燃放烟花炮竹
2. 下列图标表示“禁止吸烟”的是( )
A. B.
C. D.
3. 空气中体积分数约占78%的气体是
A. 二氧化碳 B. 氮气 C. 氧气 D. 稀有气体
4. “一畦春韭绿,十里稻花香”,人们远远就能闻到稻花香,主要说明( )
A. 分子在不断运动
B. 分子之间有间隔
C. 分子的质量和体积都很小
D. 化学变化中分子能分裂
5. 下列变化中,属于化学变化的是( )
A. 酒精挥发
B. 冰雪融化
C 蜡烛燃烧
D. 干冰升华
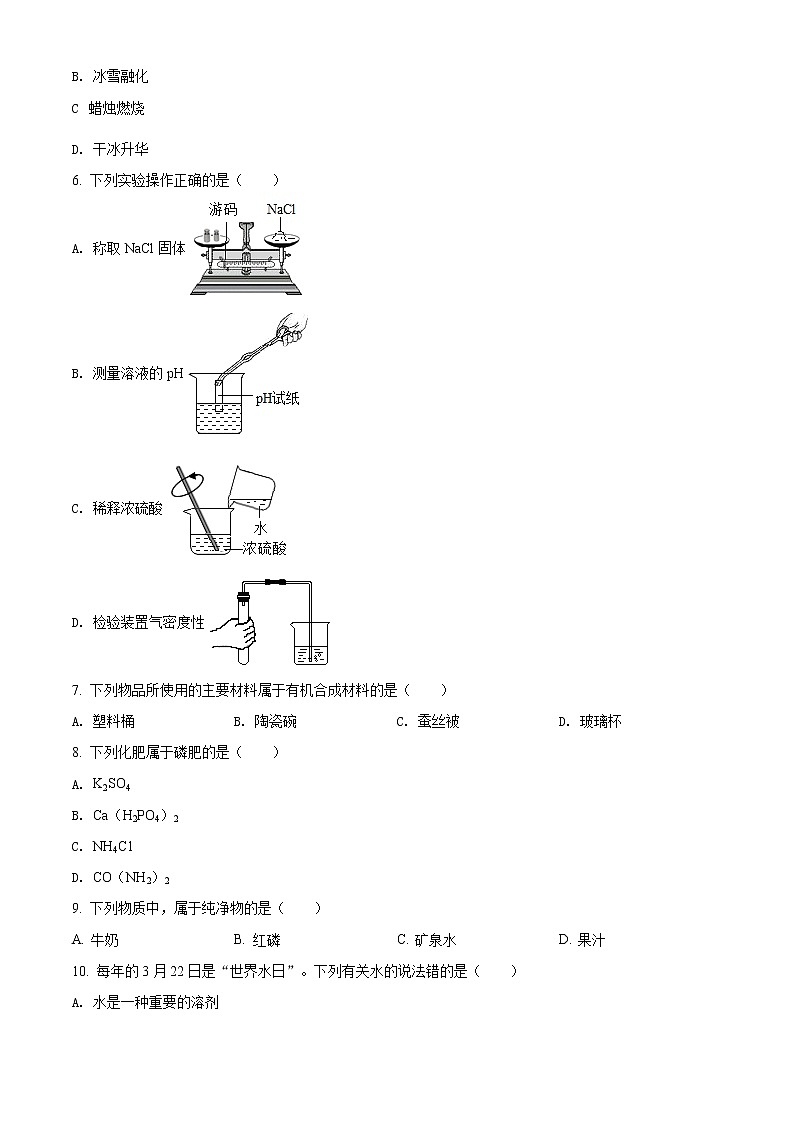
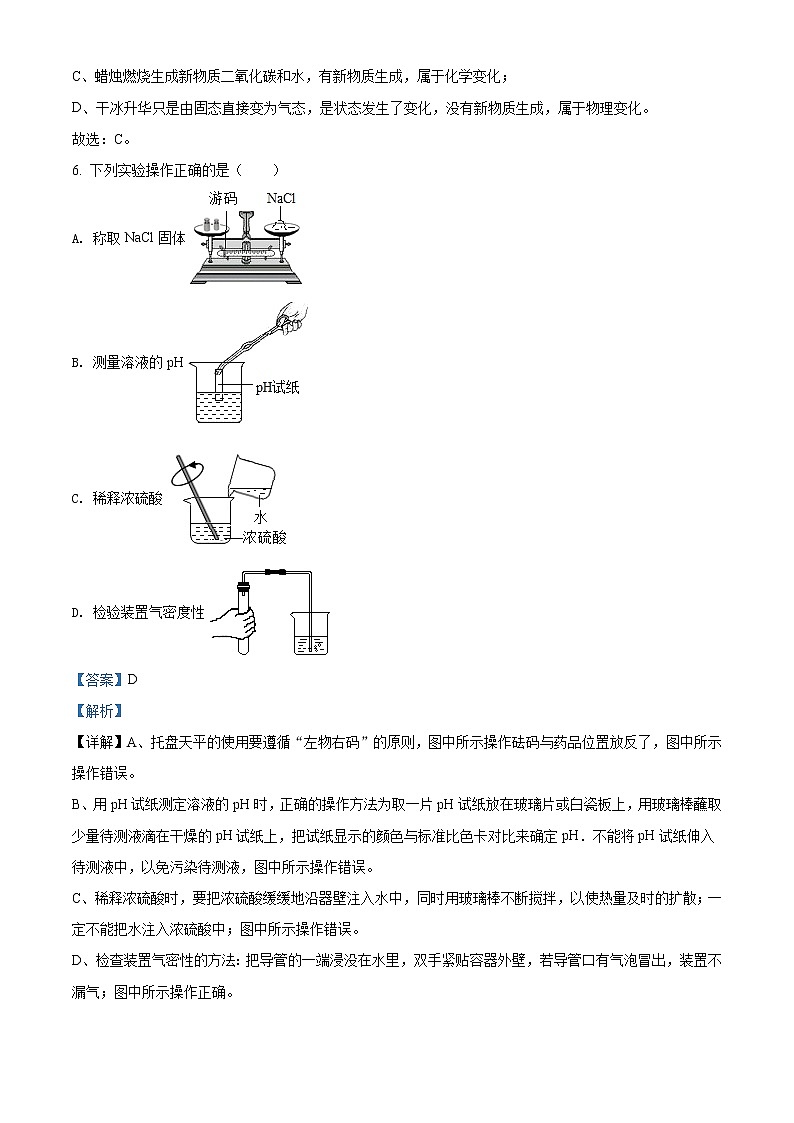
6. 下列实验操作正确的是( )
A. 称取NaCl固体
B. 测量溶液的pH
C. 稀释浓硫酸
D. 检验装置气密度性
7. 下列物品所使用的主要材料属于有机合成材料的是( )
A. 塑料桶 B. 陶瓷碗 C. 蚕丝被 D. 玻璃杯
8. 下列化肥属于磷肥的是( )
A. K2SO4
B. Ca(H2PO4)2
C. NH4C1
D. CO(NH2)2
9. 下列物质中,属于纯净物的是( )
A. 牛奶 B. 红磷 C. 矿泉水 D. 果汁
10. 每年的3月22日是“世界水日”。下列有关水的说法错的是( )
A. 水是一种重要的溶剂
B. 通过煮沸可以降低水的硬度
C. 用蒸馏的方法可以将海水淡化
D. 电解水生成氧气、氢气,说明水是由氢气和氧气组成
11. 下列物质中能由金属与稀酸反应直接得到的是
A. AgCl B. CuSO4 C. ZnSO4 D. FeCl3
12. 下列反应中属于复分解反应的是( )
A. 4Al+3O2=2Al2O3 B. Ca(HCO3)2CaCO3↓+CO2↑+H2O
C. Zn+H2SO4=ZnSO4+H2↑ D. Ca(OH)2+H2SO4=CaSO4+2H2O
13. 下列描述不正确的是
A. CO有毒且无色无气味,使用燃气时要注意室内通风
B. CO2作为气体肥料在农业生产中有广泛应用
C. N2充入食品包装袋中可起防腐作用
D. 空气中的稀有气体没有任何用途
14. 生活中处处蕴含着化学知识,下列说法错误的是( )
A. 用白醋除水壶中的水垢
B. 家用电器着火,使用水灭火
C. 增大氧气的浓度能促进可燃物的燃烧
D. 生铁和钢都是铁的合金
15. 下列实验现象描述正确的是( )
A. 木炭在氧气中燃烧发出白光,生成黑色固体
B. 铁丝在空气中燃烧时,火星四射,生成红色固体
C. 氢气在空气中燃烧,发出淡蓝色火焰
D. 硫在氧气中燃烧,发出微弱的淡蓝色火焰,产生无色无味的气体
16. 用括号中的试剂除去下列物质中的杂质,所用试剂错误的是( )
A. 除去 CO2中的 CO(灼热的 CuO)
B. 除去 Fe 粉中的 Zn 粉(稀硫酸)
C. 除去 NaCl 溶液中的 Na2CO3(适量 CaCl2溶液)
D. 除去 O2中的水蒸气(CaO)
17. 我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破。如图为该转化的微观示意图,下列有关转化的说法错误的是( )
A. 反应前后原子的种类发生了变化
B. 生成物之一为H2
C. 反应前后分子的种类发生了变化
D. 催化剂改变了反应速率
18. 近期新型冠状病毒在全球蔓延。过氧乙酸消毒液可有效杀灭新型冠状病毒。过氧乙酸(化学式为C2H4O3)是弱酸性无色液体,溶解性与醋酸相似。下列叙述错误的是
A 过氧乙酸由C、H、O三种元素组成 B. 过氧乙酸难溶于水
C. 过氧乙酸具有酸性 D. 过氧乙酸是一种有机物
19. 甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A. 甲和丙的溶解度相等
B. 降温可使丙物质的不饱和溶液变成饱和溶液
C. t1℃时,甲、乙和丙各 30g 分别加入 100g 水中,均形成饱和溶液
D. t2℃时,将 30g 甲物质加入 100g 水中,再降温到 t1℃时,所得溶液溶质的质量分数不变
20. 有一瓶久置的氢氧化钠溶液,为了探究该溶液是否变质以及变质的程度,设计了如下方案,根据方案流程,下列说法错误的是( )
A. 由步骤①的现象可知该氢氧化钠溶液已经变质
B. 若步骤②中的“现象Ⅰ”为:生成白色沉淀,则结论是该氢氧化钠溶液部分变质
C. 若步骤②中的“现象Ⅰ”为:无明显现象,则结论是该氢氧化钠溶液完全变质
D. 步骤①中的CaCl2溶液也可以用Ca(OH)2溶液代替
第Ⅱ卷(非选择题,共40分)
二、填空题(本题含4小题,每空1分,共18分)
21. 请用化学用语填写下列空白,注意按示例要求书写大小写。示例:
(1)钾离子_____。
(2)氧化钠_____。
(3)甲烷分子_____。
(4)2个二氧化硫分子_____。
22. 化学就在我们身边,它与我们的生产和生活联系紧密。
(1)请从以下选项中选择适当的物质填空。
A 熟石灰 B 小苏打 C 钙元素
①焙制糕点所用发酵粉的主要成分之一是_____(填字母,下同)。
②农业上常用_____来改良酸性土壤。
③人体缺乏_____会引起佝偻病。
(2)炒菜时油锅着火,可用锅盖盖灭,其灭火原理是_____。
23. 元素周期表是我们学习化学的重要工具。下表是小华绘制的元素周期表的局部,依据此表回答问题:
(1)第14号元素的元素符号为_____。
(2)地壳中含量最多的元素为_____(填元素符号),在化学反应中它易_____(填“得到”或“失去”)电子。
(3)钠元素在元素周期表中位于第_____周期。
24. 氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿的空气中易变质。CuCl的制备流程如下:
(1)CuCl中铜元素的化合价是_______________;“操作a”的名称是_________________。
(2)“滤液1”中除了含有Na+、Cl-、SO42-外,还含有较多的离子是_________________。
(3)“反应”中发生反应的化学方程式是 ,产生的X迅速与水化合生成一种酸,该反应的化学方程式为_________________。
(4)本流程中可以循环利用的物质(水除外)是______________ (填化学式);醇洗的目的是_________________。
三、实验题(本题含2小题,化学方程式2分,除有特殊说明外每空1分,共16分)
25. 结合下图实验常用装置,回答有关问题:
(1)指出图中仪器a的名称_____。
(2)若用高锰酸钾(KMnO4)固体制取并收集一瓶氧气,应选用的装置是_____(填序号),反应的化学方程式为_____。
(3)实验室制取二氧化碳时,若选C装置制取该气体,其优点是_____,用E装置收集二氧化碳时,气体应从_____(填序号)口进。
26. 化学兴趣小组在探究金属与酸的反应时,观察到镁、锌、铁分别与稀盐酸反应产生气泡速率不同。某同学提出问题:影响化学反应速率的因素有哪些?化学兴趣小组运用以下试剂对影响化学反应速率的因素开展探究活动。
提供试剂:15%的稀盐酸、15%的稀盐酸、铝粉、铁粉、铝片
【提出问题】影响化学反应速率的因素有哪些?
猜想与假设】
猜想1:物质的性质;猜想2:反应的温度;
猜想3:反应物的浓度;猜想4:___________。
【实验探究】(实验中只能使用提供的试剂)
实验 | 实验操作 | 实验现象 | 实验结论 |
验证猜想1 | 分别向盛有等体积的______两支试管中加入等体积的 15%的稀盐酸 | 盛有_______的试管中产气泡更快 | 物质的性质影响反应速率 |
验证猜想2 | 分别向盛有等体积的铁粉的两支试管中加入等体积的15%的稀盐酸,加热其中一支试管 | 加热试管中产生气泡更快 | 温度越_____,反应速率越快 |
验证猜想3 | 向盛有等质量铁粉的两支试管分别加入__________ | 加入_____试管中产生气泡更快 | 反应物的浓度越大,反应速率越快 |
验证猜想4 | 分别向盛有等质量铝粉和铝片试管中加入等体积5%的稀盐酸 | 盛有铝粉的试管中产生气泡更快 | ________,应速率越快 |
【实验拓展】兴趣小组将未打磨的铝片和稀盐酸放入密闭容器中,用传感器探究反应过程中温度和压强的变化(如下图所示)。下列有关说法正确的是___(填序号)。
A 铝与盐酸反应吸收热量 B 50s时,溶液中的溶质为AlCl3
C 0~50 s,铝与盐酸反应 D 100~140s,压强减小因为温度降低
四、计算题(本题共6分)
27. 向10g大理石样品中分两次加入一定溶质质量分数的稀盐酸(杂质不溶于水,也不与稀盐酸反应) ,充分反应后烧杯内物质总质量的变化如图所示。
请计算:
(1)生成二氧化碳的质量为 g。
(2)所用稀盐酸的溶质质量分数。(写出计算过程)
精品解析:广西崇左2018年中考化学试题(解析版+原卷板): 这是一份精品解析:广西崇左2018年中考化学试题(解析版+原卷板),文件包含精品解析广西崇左2018年中考化学试题解析版doc、精品解析广西崇左2018年中考化学试题原卷版doc等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。
精品解析:2020年广西贵港市覃塘区中考二模化学试题(解析版+原卷版): 这是一份精品解析:2020年广西贵港市覃塘区中考二模化学试题(解析版+原卷版),文件包含精品解析2020年广西贵港市覃塘区中考二模化学试题解析版doc、精品解析2020年广西贵港市覃塘区中考二模化学试题原卷版doc等2份试卷配套教学资源,其中试卷共22页, 欢迎下载使用。
精品解析:2020年广西梧州市岑溪市中考二模化学试题(解析版+原卷版): 这是一份精品解析:2020年广西梧州市岑溪市中考二模化学试题(解析版+原卷版),文件包含精品解析2020年广西梧州市岑溪市中考二模化学试题解析版doc、精品解析2020年广西梧州市岑溪市中考二模化学试题原卷版doc等2份试卷配套教学资源,其中试卷共25页, 欢迎下载使用。












