

山东省临沂市临沭县2021-2022学年九年级上学期期末化学试题(word版 含答案)
展开一、单选题
1.下列过程中一定发生了化学变化的是( )
A.蔗糖溶于水B.开采可燃冰C.生石灰变质D.金属拉成丝
2.下列几种常见的物质中,属于纯净物的是
A.酸奶B.氧化钙C.碘酒D.生铁
3.将少量下列物质分别放入水中,充分搅拌,可以得到无色溶液的是
A.高锰酸钾
B.菜籽油
C.面粉
D.白糖
4.下列物质露置在空气中一段时间后,因为发生化学变化而质量增加的是( )
A.浓硫酸B.浓盐酸C.氢氧化钠D.石灰石
5.元素化合价和物质类别是认识物质的两个重要维度。如图表示疏元素的化合价与含硫物质类别之间的关系,己知A点表示SO3,则下列说法错误的是
A.B点表示的物质在空气中燃烧产生淡蓝色火焰
B.C点表示的物质是大气污染物之一
C.D点表示的物质和氢氧化钠在溶液中不能大量共存
D.E点表示的物质的化学式为Na2SO3
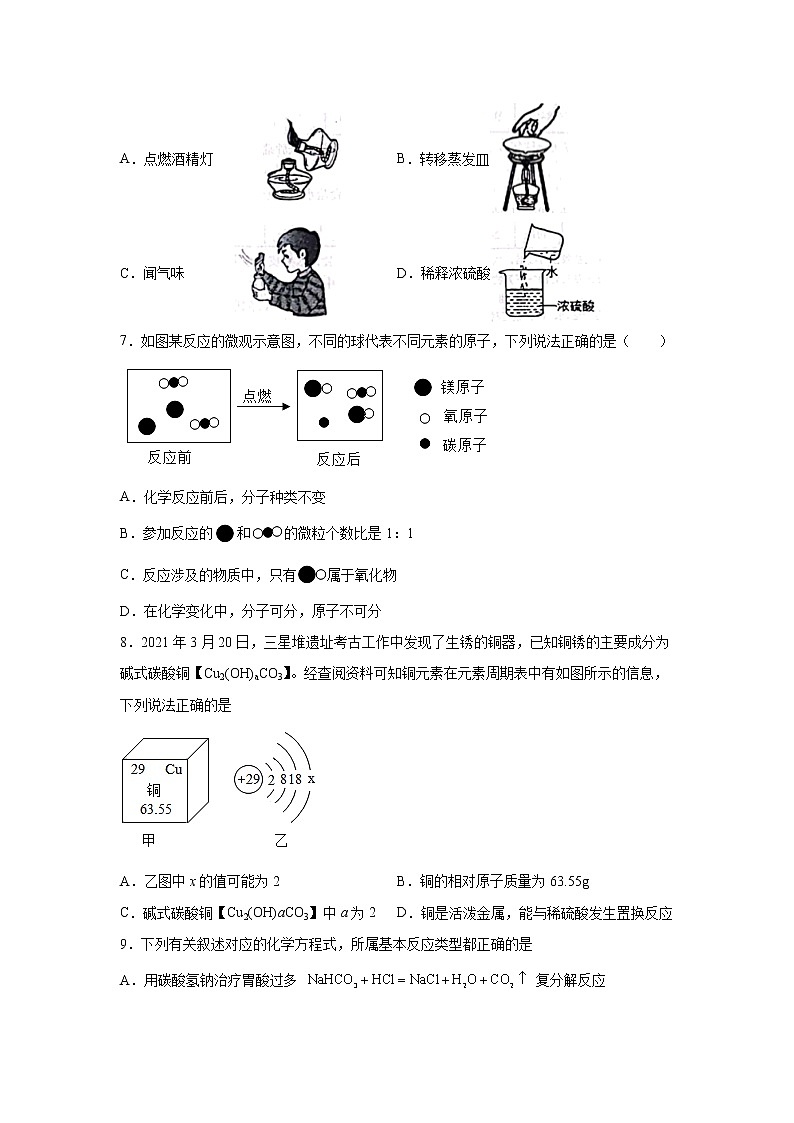
6.“操作千万条,安全第一条”。化学实验是形成科学探究素养的必要手段。下列实验操作符合安全要求的是
A.点燃酒精灯 B.转移蒸发皿
C.闻气味 D.稀释浓硫酸
7.如图某反应的微观示意图,不同的球代表不同元素的原子,下列说法正确的是( )
A.化学反应前后,分子种类不变
B.参加反应的和的微粒个数比是1:1
C.反应涉及的物质中,只有属于氧化物
D.在化学变化中,分子可分,原子不可分
8.2021年3月20日,三星堆遗址考古工作中发现了生锈的铜器,已知铜锈的主要成分为碱式碳酸铜【Cu2(OH)aCO3】。经查阅资料可知铜元素在元素周期表中有如图所示的信息,下列说法正确的是
A.乙图中x的值可能为2B.铜的相对原子质量为63.55g
C.碱式碳酸铜【Cu2(OH)aCO3】中a为2D.铜是活泼金属,能与稀硫酸发生置换反应
9.下列有关叙述对应的化学方程式,所属基本反应类型都正确的是
A.用碳酸氢钠治疗胃酸过多 复分解反应
B.细铁丝在氧气中燃烧 氧化反应
C.铝与硫酸铜溶液反应 置换反应
D.二氧化碳与澄清石灰水 中和反应
10.家庭中一些常见物质的pH如下表所示:
夏天我们被蚊虫叮咬后,蚊虫会在人的皮肤内分泌蚁酸(一种酸),从而使皮肤肿痛。要减轻痛痒,可在叮咬处涂抹下列物质中的A.食醋B.酱油C.肥皂水D.食盐水
11.某同学为验证铁、铜、银三种金属的活动性搬序,他设计了以下四种实验方案,其中能达到目的是
A.将Fe丝、Cu丝分别放入AgNO3溶液中
B.将Fe丝、Cu丝、Ag丝分别放入稀盐酸中
C.将Fe丝分别放入CuSO4溶液、AgNO3溶液中
D.将Fe丝、Ag丝分别放入CuSO4溶液中
12.“证据推理与模型认知”是化学学科核心素养的重要组成部分,以下推理正确的是
A.中和反应生成盐和水,所以生成盐和水的反应都是中和反应
B.单质只含有一种元素,所以只含有一种元素的物质一定是单质1
C.燃烧都伴随有发光放热现象,所以有发光放热现象的一定是燃烧
D.化学反应伴随能量变化,所以金属腐蚀过程中一定伴随能量变化
13.甲、乙两种固体物质的溶解度曲线如图所示。下列说法错误的是
A.甲中混有少量的乙,可用降温结晶的方法提纯甲
B.当温度大于t1℃时,甲的溶解度大于乙的溶解度
C.t1℃时,甲、乙两物质的溶液的溶质质量分数一定相等
D.t2℃时,向30g甲中加入50g水,充分溶解,所得溶液质量为75g
14.过氧乙酸是生活中常用的消毒剂,其分子结构如图所示。下列有关过氧乙酸的叙述正确的是
A.过氧乙酸化学式为C2H4O3,属于氧化物
B.过氧乙酸是由碳、氢、氧原子构成的
C.过氧乙酸显酸性,可以滴加酚酞溶液进行检验
D.过氧乙酸中氧元素的质量分数最大
15.实验室用氯化钠固体配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是
A.实验的步骤为计算、称量、量取、溶解
B.量取水时,用规格为100mL的量筒
C.若用量筒量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8%
D.溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解
16.向CuSO4溶液中加入一定质量的Zn粉,反应后过滤,得滤渣和蓝色滤液,下列说法正确的是
A.滤液中一定有CuSO4和ZnSO4B.滤液中一定有CuSO4,可能有ZnSO4
C.向滤渣中滴加稀盐酸,一定有气泡产生D.滤渣中一定有Cu,可能有Zn
17.除去下列各物质中的少量杂质,所选用的试剂和方法均正确的是
A.AB.BC.CD.D
18.下列所示的四个图像,能正确反映对应变化关系的是
A.电解水
B.向两份完全相同的稀盐酸中分别加入锌粉和铁粉
C.加热一定质量的高锰酸钾
D.向一定量的氢氧化钠溶液中加水稀释
19.用下图装置进行实验。升温至60℃的过程中,仅①燃烧;继续升温至260℃的过程中,仅③燃烧。下列分析不正确的是( )
A.①燃烧,说明白磷是可燃物
B.对比①③,可说明红磷的着火点比白磷的高
C.对比②③,可验证燃烧需可燃物与氧气接触
D.④未燃烧,说明无烟煤不是可燃物
二、填空题
20.现有①水;②干冰;③熟石灰;④一氧化碳:⑤铝;⑥金刚石等物质,请选用以上合适的物质,用其化学式填空。
(1)用来裁玻璃的是___________。
(2)改良酸性土壤的是___________。
(3)地壳中含量最高的金属元素___________。
(4)被誉为生命之源的物质是___________。
(5)用于人工降雨的是___________。
21.中国古代化学和化学工艺历史悠久、成就卓越,是劳动人民生产、生活智慧的结晶。东汉《神农本草经》曾记载石胆“能化铁为铜”。叙述的是用硫酸铜和铁反应制取铜,这是湿法炼铜的最早记载,反应的化学方程式为___________,基本反应类型属于___________。
22.氢氧化钠、氢氧化钙是两种常见的碱。
(1)它们有一些相似的化学性质,其原因是溶液中都含有______________。
(2)可作某些气体干燥剂的是_____________。
23.根据下图所示的实验回答问题。
A.粉尘爆炸实验
B.空气与呼出气体的比较
C.稀释浓硫酸
D.石墨性质实验
(1)A实验说明可燃物与氧气______,燃烧越剧烈。
(2)B实验可以比较空气与呼出气体中______含量的不同。
(3)C使用玻璃棒搅拌的目的是______。
(4)D实验说明石墨具有______性。
24.实验是科学探究的重要方式,请结合图示回答下列问题:
(1)装置1常用于实验室测定空气中氧气含量。请写出红磷燃烧的化学方程式___________。
(2)装置2中的活性炭有___________性,可用于净化水:常用___________区别硬水和软水,生活中常用煮沸的方法降低水的硬度。
(3)装置3常用于实验室电解水,此实验可以证明水是由___________组成的。
(4)装置4可用于研究CO2与NaOH溶液的反应。关闭弹簧夹K,将NaOH溶液全部挤入烧瓶,振荡;然后打开弹簧夹K。观察到的实验现象:水倒吸入烧瓶,变为红色形成美丽喷泉,写出该反应的化学方程式___________。
25.在人们担心化石能源将被耗尽时,科学家发现海底埋藏着大量可燃烧的“冰”—“可燃冰”。可燃冰外观像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等气体。可燃冰在低温和高压条件下形成,1体积可燃冰可储载100~200倍体积的甲烷气体,具有能量高,燃烧值大等优点。可燃冰将成为未来新能源。目前,我国在可燃冰的开采技术上处于世界领先水平。
回答下列问题:
(1)可燃冰属于_________。(填字母序号)
A.纯净物 B.混合物
(2)甲烷在空气中完全燃烧的化学方程式为_________。
(3)甲烷中氢为+1价,碳为_______价。
(4)从环境保护的角度考虑,下列燃料中最理想的是_________。(填字母序号)
A.氢气 B.可燃冰 C.酒精 D.汽油
26.下图是某营养药品的部分说明。
(1)说明中的“铁”指的是____(填“单质”、“元素”或“分子”);丙酸钠是由______种元素组成。
(2)该化合物中碳元素与氧元素的质量比为9∶8则x=_____________。
三、流程题
27.超细碳酸钙可用于生产钙片、牙膏等产品。利用碳化法生产超细碳酸钙的主要流程示意如下:
(1)石灰石主要成分的化学式为______。
(2)乳化池中,生石灰与水发生反应,其化学方程式为______。
(3)过筛的目的是拦截______(填“大于”或“小于”)筛孔直径的颗粒。
(4)碳化塔中反应的化学方程式为______。
四、推断题
28.已知甲、乙、丙、X、Y、Z均为初中化学常见物质,甲、乙、丙为氧化物,X、Y、Z为单质,Z为紫红色金属,其转化关系如下图所示,其中乙→Y在工业上用于赤铁矿冶炼生铁,部分反应物、反应条件和生成物己略去。
回答下列问题:
(1)MnO2的作用是___________。
(2)有毒气体乙的化学式为___________。
(3)甲→X的化学反应方程式为___________,基本反应类型为___________。
(4)丙为有磁性的黑色固体,则X→丙的化学反应方程式为___________。
五、实验题
29.下列图示中,A-E为实验装置或仪器,请结合所学知识回答有关问题:
(1)B图中仪器的名称是___________;E图中仪器①的名称是___________;
(2)实验室里用A装置制备氧气的化学方程式是___________;
(3)实验室里制备二氧化碳的化学方程式是___________,请选择图中装置或仪器,组装一套实验室里制取二氧化碳的装置该装置从左至右的顺序是___________(填字母序号)。
六、科学探究题
30.某实验小组的同学用氢氧化钠溶液和盐酸做中和反应的实验,当他们向盛有氢氧化钠溶液的烧杯中滴加一定量的稀盐酸后,发现忘记了滴加指示剂。他们停止滴加稀盐酸,对烧杯内溶液中的溶质成分进行探究。
(1)写出该中和反应的化学方程式:_________。
(2)探究烧杯内溶液中溶质的成分。
【猜想】猜想一:可能是NaCl和NaOH;猜想二:可能只有NaCl;
猜想三:_________。
【进行实验】
七、计算题
31.某公司生产出的纯碱经检测只含有氯化钠杂质。为测定该纯碱样品中碳酸钠的质量分数,称取26.5g该样品,加入到盛有一定质量稀盐酸的烧杯中,恰好完全反应。反应过程中测得烧杯内混合物的质量(m)与反应时间(t)的关系如图所示。
试分析并计算:
(1)生成CO2的质量为___________。
(2)该纯碱样品中Na2CO3的质量分数。
物质
食醋
酱油
食盐水
牙膏
肥皂
pH
2~3
4~5
7
8~9
9~10
编号
物质
杂质
试剂
除杂操作方法
A
CuO
C(木炭)
足量稀盐酸
过滤、洗涤、干燥
B
CaCl2溶液
HCl
过量CaCO3粉末
过滤
C
CO2
CO
O2
点燃
D
NaNO3溶液
NaCl
过量AgNO3溶液
过滤
营养成分
每片含量
每100g含量
铁Fe
6.70mg
1.12g
丙酸钠C3H5OxNa
0.23mg
45.50mg
实验步骤
实验操作
实验现象
结论
①
取少量烧杯内的溶液于试管中,滴入几滴酚酞溶液,振荡
_________
猜想一不成立
②
取少量烧杯内的溶液于另一支试管中,滴加碳酸钠溶液
_________
猜想三成立
参考答案:
1.C
2.B
3.D
4.C
5.D
6.C
7.D
8.C
9.A
10.C
11.D
12.D
13.C
14.D
15.C
16.A
17.B
18.C
19.D
20.(1)C
(2)Ca(OH)2
(3)Al
(4)H2O
(5)CO2
21. Fe+CuSO4=FeSO4+Cu 置换反应
22. OH- 氢氧化钠
23. 接触越充分(或接触面积越大等,合理即可) O2(或氧气) 散热(合理即可) 导电
24.(1)
(2) 吸附 肥皂水
(3)氢元素和氧元素
(4)2NaOH+CO2=Na2CO3+H2O
25. B
-4 A
26. 元素 4 2
27. CaCO3 CaO+H2O=Ca(OH)2 大于 Ca(OH)2+CO2=CaCO3↓+H2O
28.(1)催化作用
(2)CO
(3) 分解反应
(4)
29.(1) 试管 集气瓶
(2)
(3) BDC
30. NaOH + HCl═NaCl + H2O 可能是NaCl和HCl 溶液不变色 有气泡产生
31.解:(1)根据质量守恒定律可得,生成的二氧化碳的质量为:172.5g﹣163.7g=8.8g;
(2)设纯碱样品中Na2CO3的质量为x
x=21.2g
×100%=80%。
答:该纯碱样品中Na2CO3的质量分数为80%;
2022年山东省临沂市临沭县中考二模化学试题: 这是一份2022年山东省临沂市临沭县中考二模化学试题,共8页。
山东省临沂市费县2021-2022学年九年级上学期期末化学试题(word版 含答案): 这是一份山东省临沂市费县2021-2022学年九年级上学期期末化学试题(word版 含答案),共13页。试卷主要包含了单选题,填空题,科学探究题,流程题,实验题,计算题等内容,欢迎下载使用。
山东省临沂市蒙阴县2021-2022学年九年级上学期期中化学试题(word版 含答案): 这是一份山东省临沂市蒙阴县2021-2022学年九年级上学期期中化学试题(word版 含答案),共11页。试卷主要包含了单选题,填空题,流程题,简答题,实验题,计算题等内容,欢迎下载使用。













