





初中化学人教版九年级下册课题2 酸和碱的中和反应教课ppt课件
展开1.会用pH试纸检验溶液的酸碱性。2.了解溶液的酸碱度在实际中的意义。
1.溶液的酸碱性用 鉴别,溶液的酸碱度用 测定。
2.pH的范围在 之间。pH<7,溶液呈 性;pH=7,溶液呈 性;pH>7,溶液呈 性。
3.了解溶液酸碱度的意义:(1)化工生产中要控制pH范围;(2)农作物适宜在pH为7或接近7的土壤中生长;(3)测定雨水的pH,正常雨水pH约为 ,pH小于5.6的雨水为 ;(4)测定人体内液体的pH,了解人体健康状况。
知识点1 溶液酸碱度的表示方法
利用酚酞溶液能否将不同浓度的两瓶硫酸和不同浓度的两瓶氢氧化钠溶液鉴别出来?
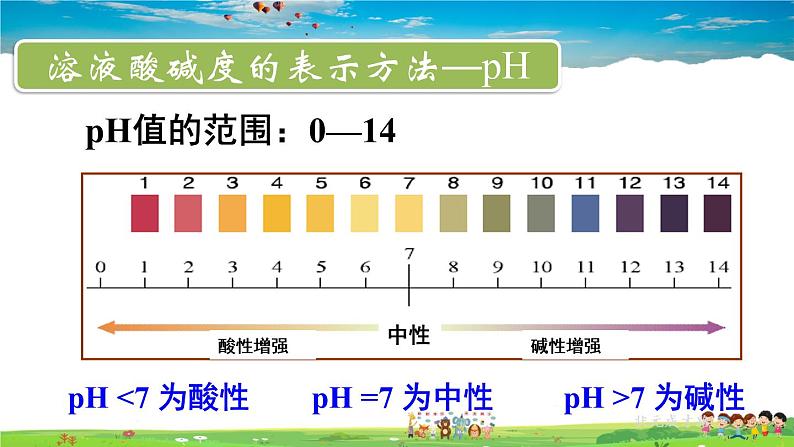
pH值的范围:0—14
pH <7 为酸性 pH =7 为中性 pH >7 为碱性
溶液酸碱度的表示方法—pH
pH试纸 精确到整数
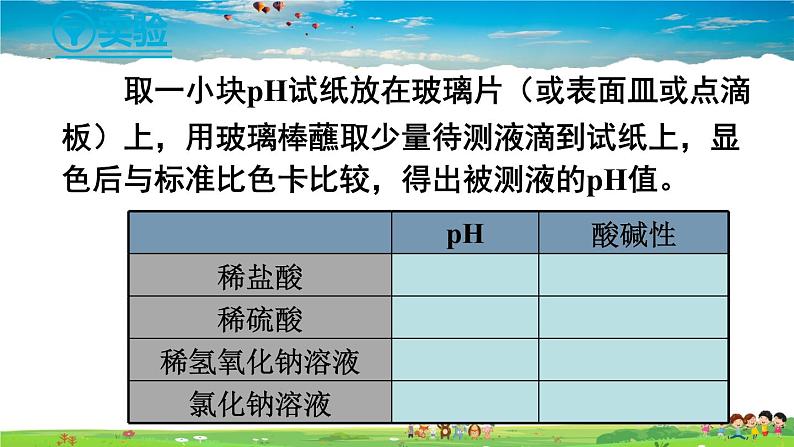
取一小块pH试纸放在玻璃片(或表面皿或点滴板)上,用玻璃棒蘸取少量待测液滴到试纸上,显色后与标准比色卡比较,得出被测液的pH值。
(1)用pH试纸只能粗略测定溶液的pH,一般读数是整数,不是小数。(2)不能将pH试纸直接插入待测液中检测溶液,防止污染待测液。(3)不能事先用蒸馏水润湿pH试纸,如果将试纸先用蒸馏水润湿,则相当于待测液被稀释了,所测得pH可能不准确。
这些物质的酸碱度是多少呢?
【提出问题】从实验结果中你有什么新的发现?【交流回答】pH<7的是酸性溶液,但不一定是酸溶液;pH>7的是碱性溶液,但不一定是碱溶液。
【例】下列检测某溶液pH的操作正确的是( )A.将pH试纸投入待测液,对照标准比色卡读数B.用干燥、洁净的玻璃棒蘸取少量待测液,滴在置于洁净表面皿的pH试纸上,半分钟内根据试纸呈现的颜色,对照标准比色卡读数C.用玻璃棒蘸取待测液滴在用蒸馏水润湿的pH试纸上,对照标准比色卡读数D.用玻璃棒蘸取待测液滴在pH试纸上,3分钟后对照标准比色卡读数
知识点2 了解溶液酸碱度的意义
化工生产中许多反应必须在一定pH溶液里才能进行。
在农业生产中,农作物一般适宜在pH=7或接近7的土壤中生长。
测定人体内或排出的液体的pH,可以了解人体的健康状况。
测定雨水的pH可以了解空气污染情况(正常雨水pH约为5.6,酸雨的pH<5.6)。
洗发时,用过洗发剂后再用护发剂,这样对头发有保护作用。你能解释这是为什么吗?
洗发水呈碱性,能够帮助头发的毛鳞片打开,彻底清洁的同时还能吸收营养;护发素呈酸性,能关闭头发的毛鳞片,使头发顺滑。
【例】化学物质及其变化与生活密切相关。(1)健康人的体液pH必须维持在一定范围内。如果体液pH超越正常范围,就会导致某些疾病的产生。胃液的pH 7(填“大于”“小于”或“等于”) 。人体内二氧化碳排出不畅时,会导致血液pH (填“升高”或“降低”)。
(2)下表是一些作物适宜生长的pH范围: 某地红土壤偏酸性。上述作物不适宜在红土壤中种植的是 。
1.溶液酸碱度的表示方法——pH。pH <7 为酸性 ;pH =7 为中性 ;pH >7 为碱性。2.测定pH的方法用pH试纸或者pH计3.改变溶液酸碱度的方法加水或加酸溶液、或碱溶液4.酸碱度在生产、生活及生命活动中的意义
这节课你有什么收获吗?
1.从课后习题中选取;2.完成练习册本课时的习题。
1.填空题(1)实验室中有A、B两种溶液,经测定,A溶液pH=4.5,B溶液pH=10.2。则A溶液呈____性,能使紫色石蕊溶液变____色;B溶液呈____性,能使无色酚酞溶液变___色。(2)测定pH最简单的方法是使用________。测定时,用 蘸取待测溶液,滴在_________上,然后再与_____________对照,得出该溶液的pH。
2. 一些食物的近似pH如下:下列说法中不正确的是()。A.鸡蛋清和牛奶显碱性B.苹果汁和葡萄汁显酸性C.苹果汁比葡萄汁的酸性强D.胃酸过多的人应少饮葡萄汁和苹果汁
3.某小型造纸厂向河中非法排放了大量碱性废液。请你根据所学的知识,设计两种检测碱性废液和受污染河水的方法,并试着提出治理的措施。
解:取样于试管:方法一:滴入酚酞溶液,若溶液变为红色,则说明河水已被碱性溶液污染。方法二:滴入石蕊溶液,若溶液变为蓝色,则说明河水已被碱性溶液污染。
方法四:在白瓷板或玻璃板上放一小片pH试纸,用玻璃棒蘸取河水样品滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,若读出该溶液的pH>7,则说明河水已被碱性溶液污染。治理措施:向该呈碱性的污染河水中加入适量的酸性溶液中和。造纸厂的废水经处理检验合格后再排放。
方法三:取样,滴入硫酸铜溶液,若生成蓝色沉淀,则说明河水已被碱性溶液污染。
4.某学校化学课外活动小组的同学开展了下列实验活动:取刚降到地面的雨水水样用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:(1 )所降雨水是否为酸雨?在测定期间,雨水的酸性是增强还是减弱?
初中人教版课题2 酸和碱的中和反应获奖课件ppt: 这是一份初中人教版课题2 酸和碱的中和反应获奖课件ppt,文件包含第2课时溶液酸碱度的表示方法pH课件pptx、第2课时溶液的pH及其应用导学案doc、第2课时溶液的pH及其应用教案doc、用pH试纸测定溶液pH值mp4等4份课件配套教学资源,其中PPT共30页, 欢迎下载使用。
人教版九年级下册课题2 酸和碱的中和反应习题课件ppt: 这是一份人教版九年级下册课题2 酸和碱的中和反应习题课件ppt,共21页。PPT课件主要包含了~14,pH试纸,标准比色卡,接近7,9~15,加水稀释,加入NaOH,加入金属锌,不一定,逐渐减小等内容,欢迎下载使用。
化学九年级下册课题2 酸和碱的中和反应教学课件ppt: 这是一份化学九年级下册课题2 酸和碱的中和反应教学课件ppt,共14页。PPT课件主要包含了洗洁精,柠檬汁或雨水,马铃薯,熟石灰,NaOH等内容,欢迎下载使用。













