






化学九年级下册课题2 酸和碱的中和反应评课ppt课件
展开浓度为1%的盐酸和浓度为10%的盐酸哪个酸性更强呢? 你能用什么方法区分两种溶液吗? 石蕊可以吗?
三、溶液酸碱度的表示法——pH
在生活、生产和科学研究中,不仅要知道溶液是酸性还是碱性,往往还需要知道溶液的酸碱性强弱程度,即溶液的酸碱度。
(一)溶液的酸碱度常用pH来表示,pH的范围通常在0~14之间。
测定pH最简便的方法是用pH试纸
溶液pH的测定操作:在白瓷板或玻璃片上放一小片pH试纸,将被测溶液滴到试纸上,把试纸显示的颜色与标准比色卡比较。
(1)测溶液酸碱度时, pH试纸要预先湿润吗?为什么?(2)测溶液酸碱度时, pH试纸能直接伸入待测液吗?
3. 中性溶液的pH=7 (如水、食盐溶液)
1. 酸性溶液的pH<7 (pH值越小表示酸性越强)
2. 碱性溶液的pH>7 (pH值越大表示碱性越强)
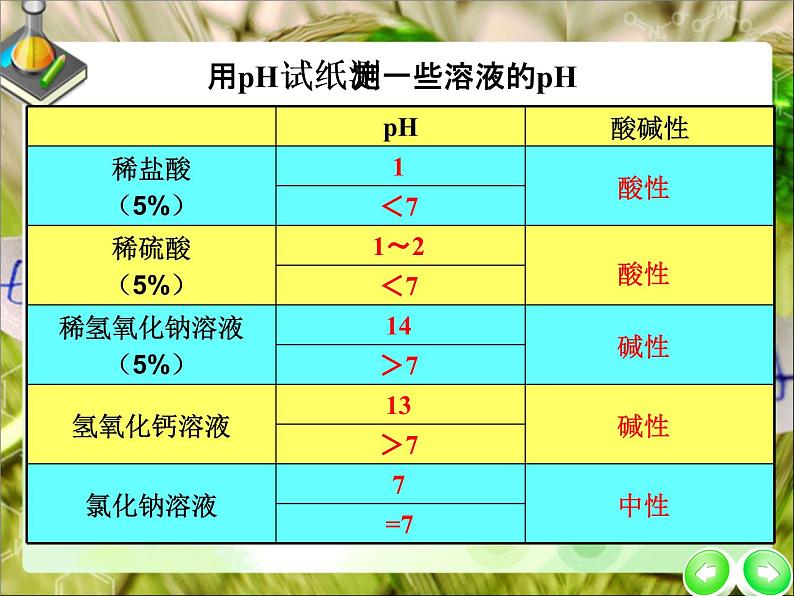
用pH试纸测定一些溶液的pH
【活动与探究 】测定生活中的一些物质的pH
(二)了解物质酸碱性的意义
★ 化工生产中许多反应必须在一定pH溶液里才能进行。如酿酒、醋;
★在农业生产中,农作物一般适宜在pH为7或接近7的土壤中生长;在pH<4的酸性土壤或pH>8的碱性土壤中,一般不适于种植;
★ 随时监测雨水的pH(因溶解有二氧化碳,正常雨水的pH约为5.6,酸雨的pH小于5.6),可以了解空气的污染情况,以便采取必要的措施;
★健康人的体液必须维持在一定的酸碱度的范围内,测定人体内或排出的液体的pH,可以帮助人们了解身体的健康状况。
人体内的一些液体和排泄物的正常pH范围
选择和使用洗发液与护发液,你学会了吗?
洗发剂和护发剂的酸碱性
谈谈本节课你在学习过程中收获的知识。
溶液酸碱度的表示法——pH
(一)溶液的酸碱度常用pH来表示,pH的范 围通常在0~14之间。
1.测定pH最简便的方法是用pH试纸。(也可用pH计测量)
2.溶液pH的测定操作:在白瓷板或玻璃片上放一小片pH试纸,将被测溶液滴到试纸上,把试纸显示的颜色与标准比色卡比较。
(3)中性溶液的pH=7 (如水、食盐溶液)
(1) 酸性溶液的pH<7 (pH值越小表示酸性越强)
(2) 碱性溶液的pH>7 (pH值越大表示碱性越强)
★ 化工生产中许多反应必须在一定pH溶液里才能进行。如酿酒;
★在农业生产中,农作物一般适宜在pH为7或接近7的土壤中生长;在pH<4的酸性土壤或pH>8的碱性土壤中,一般不适于种植;
★ 随时监测雨水的pH(因溶解有二氧化碳,正常雨水的pH约为5.6,酸雨的pH小于5.6),可以了解空气的污染情况,以便采取必要的措施;
★健康人的体液必须维持在一定的酸碱度的范围内,测定人体内或排出的液体的pH,可以帮助人们了解身体的健康状况。
1.根据下列实验现象可以判断某溶液一定呈碱性的是( ) A. 常温下,测得溶液的pH<7 B. 溶液中滴入酚酞显红色 C. 溶液中滴入石蕊显红色 D. 溶液中滴入酚酞不显色2.一些物质的近似pH:泡菜3.4、苹果汁3.1、西瓜汁5.8、鸡蛋清7.6,其中酸性最强的是( ) A. 泡菜 B. 苹果汁 C. 西瓜汁 D. 鸡蛋清
3.某同学用pH试纸测定日常生活中一些液体的pH。他的实验记录一定错误的是( ) A.肥皂水pH=10 B.纯碱溶液pH=11 C.橘子汁pH=4 D.食醋pH=74.(日照)下列说法错误的是( )A.碱中一定含有氢元素B.Ca和Ca2+两种微粒的质子数相同C.用pH试纸测定溶液的pH时,应先用蒸馏水将试纸润湿D.洗过的玻璃仪器内壁附着的水既不聚成水滴也不成股流下时, 表示仪器已洗净
6. (青岛)不同物质的溶液酸碱性不同。根据下表中 所列物质pH的情况判断,下列说法中正确的是( ) A. pH小于7的一定是酸溶液 B. pH大于7的一定是碱溶液 C. pH等于7的一定是水 D. 盐溶液可能显酸性、碱性或中性
7. 酸和碱能发生中和反应,生成盐和水。已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,图中表示向甲中加入乙时溶液pH的变化曲线。请你写出从图中所获取的信息:(1)甲是 ;(2)乙是 ;(3) ;(4) 。
c点表示酸和碱恰好完全反应或c点的pH=7或反应前溶液的pH<7
乙过量后溶液显碱性(或pH>7)或随着乙溶液的加入,溶液的pH逐渐增大等
8. (泰安)下表是部分农作物生长对土壤pH的要求。如果某地区经常降酸雨,则该地区最不适合种植的农作物是( ) A.大豆 B.茶 C.玉米 D.马铃薯
9.(兰州)某校化学课外活动小组在一次活动中,取刚降到地面的雨水水样,每隔5分钟用pH计测定一次pH,某数据如下表:已知:正常雨水的pH约为5.6,酸雨的pH小于5.6。所取的雨水是否为酸雨? (填“是”或“否”);在测定的期间,雨水水样的酸性随着时间的变化逐渐 (填“增强”或“减弱”)。
谈谈本节课你的收获和困惑
1.我在知识上的收获2.我在学习方法上的收获3.我存在的困惑
人教版九年级下册第十单元 酸和碱课题2 酸和碱的中和反应课前预习课件ppt: 这是一份人教版九年级下册<a href="/hx/tb_c9871_t3/?tag_id=26" target="_blank">第十单元 酸和碱课题2 酸和碱的中和反应课前预习课件ppt</a>,共12页。PPT课件主要包含了学习目标,重难点,引入新课,教学过程,讲授新课等内容,欢迎下载使用。
初中人教版课题2 酸和碱的中和反应备课课件ppt: 这是一份初中人教版<a href="/hx/tb_c9871_t3/?tag_id=26" target="_blank">课题2 酸和碱的中和反应备课课件ppt</a>,共11页。PPT课件主要包含了学习目标,重难点,引入新课,教学过程,讲授新课等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 酸和碱的中和反应多媒体教学课件ppt: 这是一份初中化学人教版九年级下册课题2 酸和碱的中和反应多媒体教学课件ppt,共28页。PPT课件主要包含了活动与探究,中和反应,思路一,播放中和反应实验,化学方程式,归纳并板书,思路二,思路三,氢氧化钠与盐酸反应,改良酸性土壤等内容,欢迎下载使用。













