





2022高考化学一轮复习(步步高)第七章 第33讲 微专题17 探究影响化学反应速率的因素课件
展开在研究影响化学反应速率的因素时,由于外界影响因素较多,故为搞清楚某个因素的影响需控制其他因素相同或不变,再进行实验。因此,常用控制变量思想解决该类问题。1.常见考查形式(1)以表格的形式给出多组实验数据,让学生找出每组数据的变化对化学反应速率的影响。(2)给出影响化学反应速率的几种因素,让学生设计实验分析各因素对化学反应速率的影响。
2.解题策略(1)确定变量解答这类题目时首先要认真审题,理清影响实验探究结果的因素有哪些。(2)定多变一在探究时,应该先确定其他的因素不变,只变化一种因素,看这种因素与探究的问题存在怎样的关系;这样确定一种以后,再确定另一种,通过分析每种因素与所探究问题之间的关系,得出所有影响因素与所探究问题之间的关系。
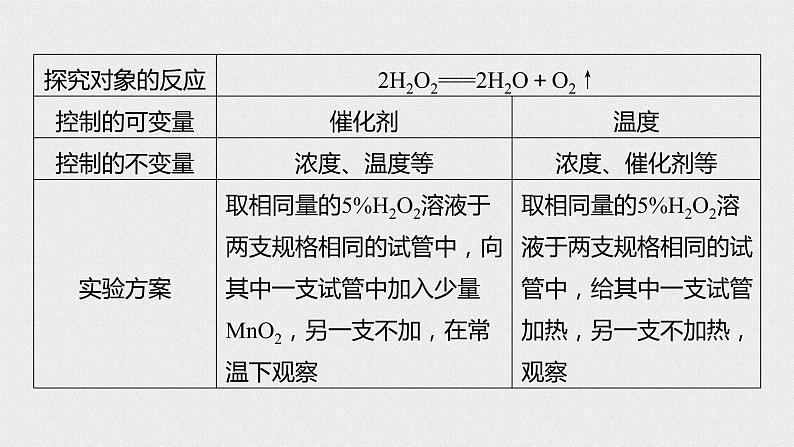
(3)数据有效解答时注意选择数据(或设置实验)要有效,且变量统一,否则无法作出正确判断。3.实例分析探究温度、催化剂对反应:2H2O2===2H2O+O2↑的影响,可以确定催化剂(是否加入MnO2)和温度(加热、常温)作为可变量,其他的则控制为不变量。
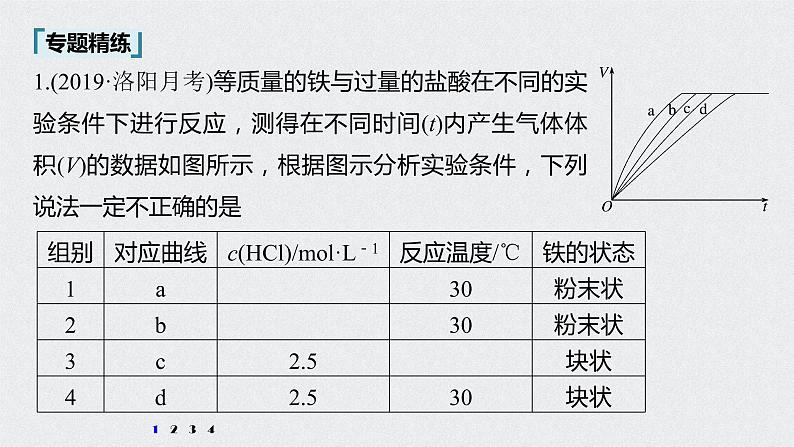
1.(2019·洛阳月考)等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如图所示,根据图示分析实验条件,下列说法一定不正确的是
A.第4组实验的反应速率最慢B.第1组实验中盐酸的浓度大于2.5 ml·L-1C.第2组实验中盐酸的浓度等于2.5 ml·L-1D.第3组实验的反应温度低于30 ℃
解析 由图像可知,1、2、3、4四组实验产生的氢气一样多,只是反应速率有快慢之分。第4组实验,反应所用时间最长,故反应速率最慢,A正确;第1组实验,反应所用时间最短,故反应速率最快,根据控制变量法原则知盐酸浓度应大于2.5 ml·L-1,B正确;第2组实验,铁是粉末状,与3、4组块状铁相区别,根据控制变量法原则知盐酸的浓度应等于2.5 ml·L-1,C正确;由3、4组实验并结合图像知第3组实验中反应温度应高于30 ℃,D错误。
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快C.图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
2.(2017·江苏,10)H2O2分解速率受多种因素影响。实验测得70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
解析 A项,浓度对反应速率的影响是浓度越大,反应速率越快,错误;B项,NaOH浓度越大,即pH越大,H2O2分解速率越快,错误;C项,由图可知,Mn2+存在时,0.1 ml·L-1 NaOH溶液中H2O2的分解速率比1.0 ml·L-1的NaOH中的快,错误;D项,由图可知,碱性条件下,Mn2+存在时,对H2O2分解速率影响大,正确。
3.(2020·石家庄模拟)为了研究一定浓度Fe2+的溶液在不同条件下被氧气氧化的氧化率,实验结果如图所示,判断下列说法正确的是A.pH越小,氧化率越大B.温度越高,氧化率越小C.Fe2+的氧化率仅与溶液的pH和温度有关D.实验说明降低pH、升高温度有利于提高 Fe2+的氧化率
解析 由②③可知,温度相同时,pH越小,氧化率越大,由①②可知,pH相同时,温度越高,氧化率越大;C项,Fe2+的氧化率除受pH、温度影响外,还受其他因素影响,如浓度等。
4.(1)某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
①本实验待测数据可以是________________________________________________________________,实验Ⅰ和实验Ⅱ可以探究__________对锌与稀硫酸反应速率的影响。
反应结束所需要的时间(或相同条件下产生等体积的氢气所需要的时间)
解析 实验Ⅰ和实验Ⅱ中,锌的质量和状态相同,硫酸的浓度不同,实验Ⅲ和实验Ⅳ中加入硫酸铜,Cu2+的氧化性强于H+,首先发生反应Zn+Cu2+===Zn2++Cu,生成的铜附着在锌表面,在稀硫酸溶液中构成原电池,加快锌失电子。但是加入的硫酸铜过多,生成的铜会覆盖在锌表面,阻止锌与稀硫酸进一步反应,产生氢气的速率会减慢。本实验待测数据可以是“反应结束所需要的时间”或“相同条件下产生等体积的氢气所需要的时间”,实验Ⅰ和实验Ⅱ可以探究硫酸的浓度对反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是__________________________________,写出有关反应的离子方程式:____________________________________________。
探究硫酸铜的质量对反应速率的影响
Zn+Cu2+===Zn2++Cu,Zn+2H+===Zn2+
解析 实验Ⅲ和实验Ⅳ加入的硫酸铜的质量不同,可以探究加入硫酸铜的质量与反应速率的关系。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中Vx=_____,理由是__________________________________________________。
保证反应物K2S2O8浓度的改变,而其他物质的
解析 实验的目的是探究K2S2O8溶液的浓度对化学反应速率的影响,故应保证每组实验中其他物质的浓度相等,即溶液的总体积相等(即为20.0 mL),从而可知Vx=2.0。
新教材适用2024版高考化学一轮总复习第10章化学实验基础第33讲高考化学综合实验题探究课件: 这是一份新教材适用2024版高考化学一轮总复习第10章化学实验基础第33讲高考化学综合实验题探究课件,共60页。PPT课件主要包含了考点一,考点二,考点三,必备知识·梳理夯实,氢氧化钠,酸性KMnO4,KMnO4,白色沉淀,先灭灯再停氢,冷凝回流等内容,欢迎下载使用。
2023版高考化学一轮总复习第八章微专题八控制变量法探究影响化学反应速率的因素课件: 这是一份2023版高考化学一轮总复习第八章微专题八控制变量法探究影响化学反应速率的因素课件,共8页。PPT课件主要包含了解题策略,实例分析,典例精析,溶液不会立即变蓝,应物浓度对速率的影响,质的量之比应小于2,答案C等内容,欢迎下载使用。
2022高三化学一轮复习优化探究 第十章 第33讲 化学实验热点课件PPT: 这是一份2022高三化学一轮复习优化探究 第十章 第33讲 化学实验热点课件PPT,共60页。PPT课件主要包含了2蒸馏装置,把握制备流程,答案210等内容,欢迎下载使用。












