

2020年高考化学真题分类训练 专题14 化学反应原理综合
展开专题14 化学反应原理综合
2020年高考真题
1.(2020年新课标Ⅰ)硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO2的催化氧化:SO2(g)+O2(g)SO3(g) ΔH=−98 kJ·mol−1。回答下列问题:
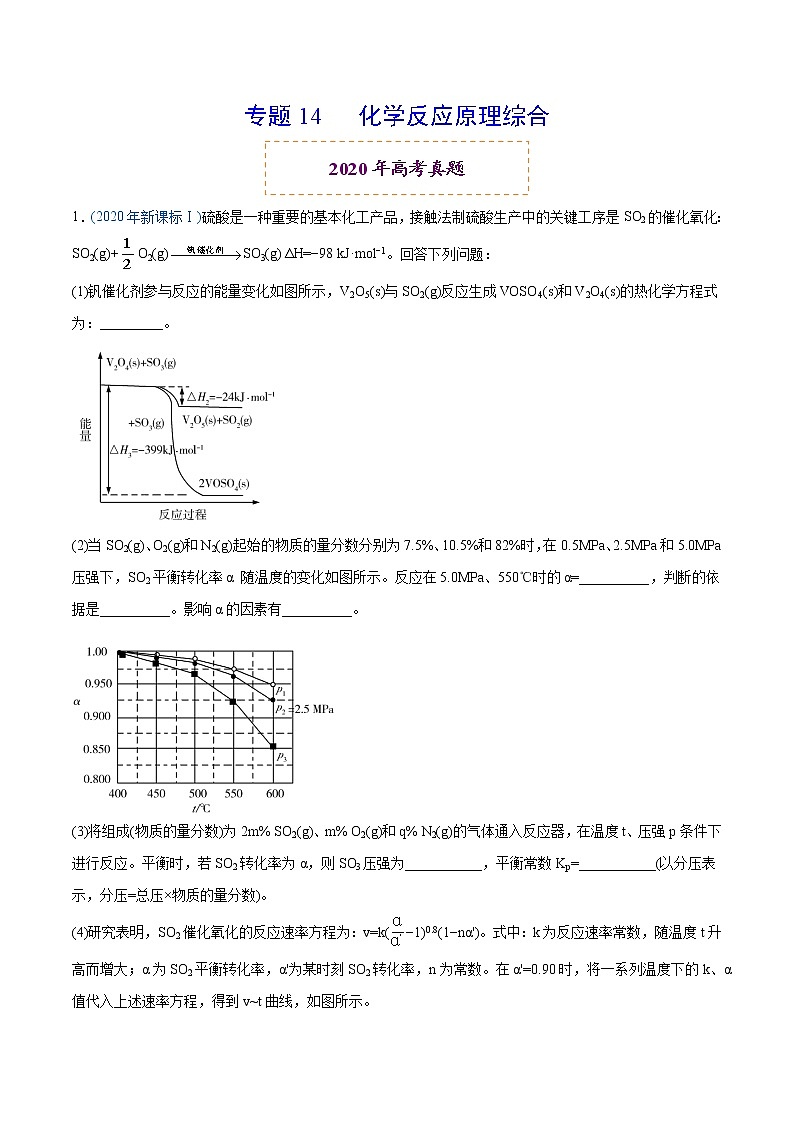
(1)钒催化剂参与反应的能量变化如图所示,V2O5(s)与SO2(g)反应生成VOSO4(s)和V2O4(s)的热化学方程式为:_________。
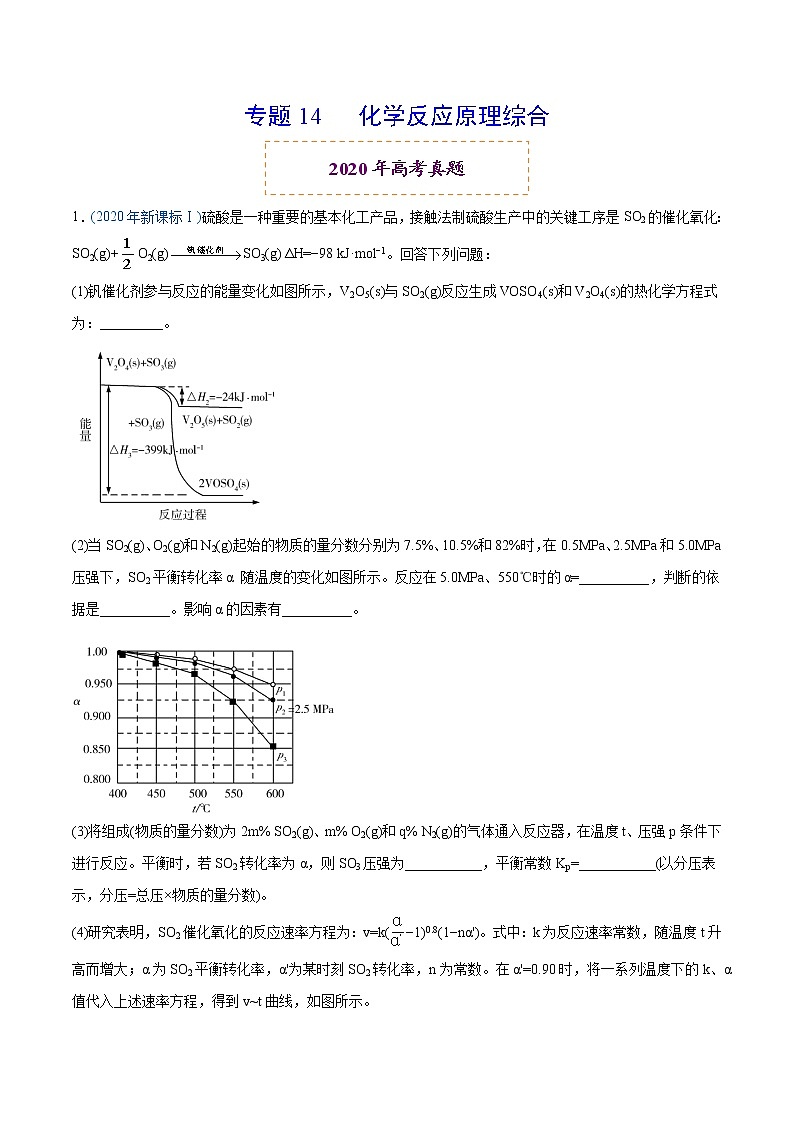
(2)当SO2(g)、O2(g)和N2(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α 随温度的变化如图所示。反应在5.0MPa、550℃时的α=__________,判断的依据是__________。影响α的因素有__________。
(3)将组成(物质的量分数)为2m% SO2(g)、m% O2(g)和q% N2(g)的气体通入反应器,在温度t、压强p条件下进行反应。平衡时,若SO2转化率为α,则SO3压强为___________,平衡常数Kp=___________(以分压表示,分压=总压×物质的量分数)。
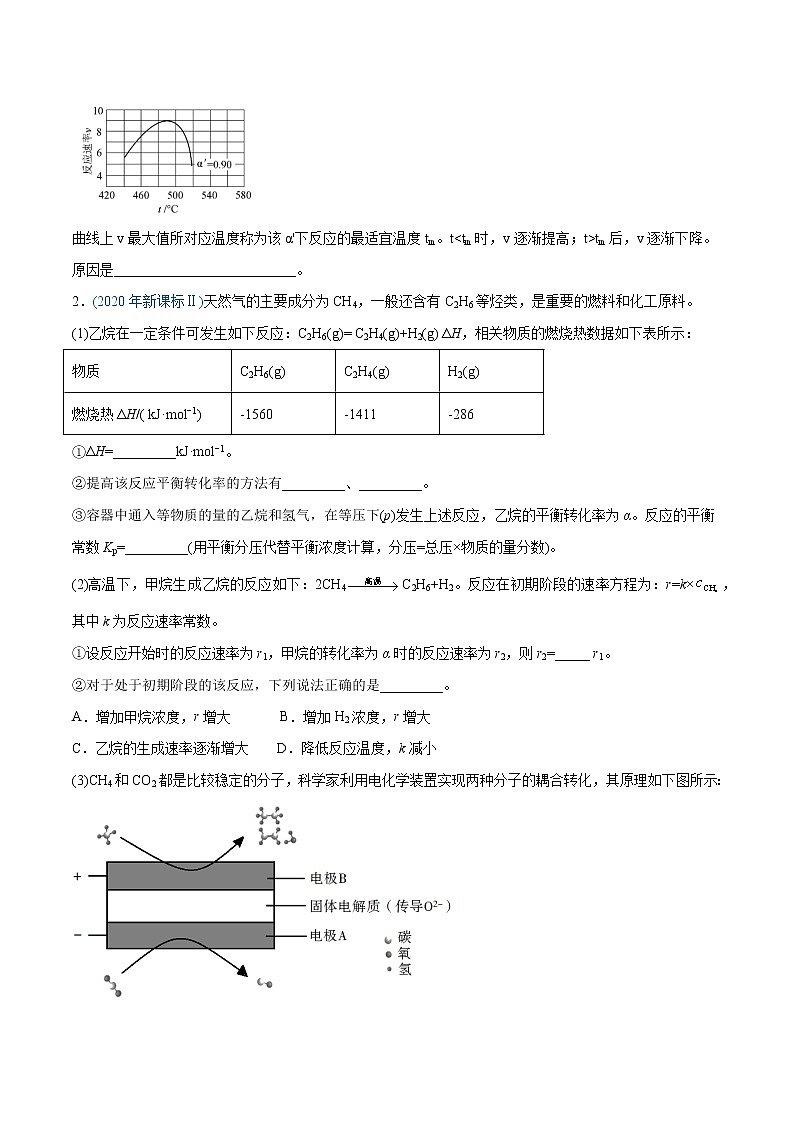
(4)研究表明,SO2催化氧化的反应速率方程为:v=k(−1)0.8(1−nα')。式中:k为反应速率常数,随温度t升高而增大;α为SO2平衡转化率,α'为某时刻SO2转化率,n为常数。在α'=0.90时,将一系列温度下的k、α值代入上述速率方程,得到v~t曲线,如图所示。
曲线上v最大值所对应温度称为该α'下反应的最适宜温度tm。t
【答案】(1)2V2O5(s)+ 2SO2(g)⇌ 2VOSO4(s)+ V2O4(s) ∆H= -351 kJ∙mol-1
(2)0.975 该反应气体分子数减少,增大压强,α提高。所以,该反应在550℃、压强为5.0MPa>2.5MPa=p2的,所以p1=5.0MPa 反应物(N2和O2)的起始浓度(组成)、温度、压强
(3)
(4)升高温度,k增大使v逐渐提高,但α降低使v逐渐下降。当t<tm,k增大对v的提高大于α引起的降低;当t>tm,k增大对v的提高小于α引起的降低
【解析】【分析】根据盖斯定律,用已知的热化学方程式通过一定的数学运算,可以求出目标反应的反应热;根据压强对化学平衡的影响,分析图中数据找到所需要的数据;根据恒压条件下总压不变,求出各组分的分压,进一步可以求出平衡常数;根据题中所给的速率公式,分析温度对速率常数及二氧化硫的转化率的影响,进一步分析对速率的影响。
【详解】(1)由题中信息可知:
①SO2(g)+O2(g)⇌SO3(g) ∆H= -98kJ∙mol-1
②V2O4(s)+ SO3(g)⇌V2O5(s)+ SO2(g) ∆H2= -24kJ∙mol-1
③V2O4(s)+ 2SO3(g)⇌2VOSO4(s) ∆H1= -399kJ∙mol-1
根据盖斯定律可知,③-②´2得2V2O5(s)+ 2SO2(g)⇌ 2VOSO4(s)+ V2O4(s),则∆H= ∆H1-2∆H2=( -399kJ∙mol-1)-( -24kJ∙mol-1)´2= -351kJ∙mol-1,所以该反应的热化学方程式为:2V2O5(s)+ 2SO2(g)⇌ 2VOSO4(s)+ V2O4(s) ∆H= -351 kJ∙mol-1;
(2) SO2(g)+O2(g)⇌SO3(g),该反应是一个气体分子数减少的放热反应,故增大压强可以使化学平衡向正反应方向移动。因此,在相同温度下,压强越大,SO2的平衡转化率越大,所以,该反应在550℃、压强为5.0MPa条件下,SO2的平衡转化率一定高于相同温度下、压强为2.5MPa的,因此,p1=5.0MPa,由图中数据可知,α=0.975。影响α的因素就是影响化学平衡移动的因素,主要有反应物(N2和O2)的浓度、温度、压强等。
(3)假设原气体的物质的量为100mol,则SO2、O2和N2的物质的量分别为2m mol、m mol和q mol,2m+m+q=3m+q=100,SO2的平衡转化率为α,则有下列关系:
平衡时气体的总物质的量为n(总)= 2m(1-α)+m(1-α)+2mαmol+q mol,则SO3的物质的量分数为。该反应在恒压容器中进行,因此,SO3的分压p(SO3)=,p(SO2)=,p(O2)=,在该条件下,SO2(g)+ O2(g)⇌2SO3(g) 的Kp=。
(4) 由于该反应是放热反应,温度升高后α降低。由题中信息可知,v=,升高温度,k增大使v逐渐提高,但α降低使v逐渐下降。当t<tm,k增大对v的提高大于α引起的降低;当t>tm,k增大对v的提高小于α引起的降低。
【点睛】本题有关化学平衡常数的计算是一个难点,尤其题中给的都是字母型数据,这无疑增大了难度。这也是对考生的意志的考验,只要巧妙假设、小心求算,还是可以得到正确结果的,毕竟有关化学平衡的计算是一种熟悉的题型。本题的另一难点是最后一问,考查的是速率公式与化学平衡的综合理解,需要明确化学反应速率与速率常数及平衡转化率之间的函数关系,才能作出正确的解答。所以,耐心和细心才是考好的保证。
2.(2020年新课标Ⅱ)天然气的主要成分为CH4,一般还含有C2H6等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:C2H6(g)= C2H4(g)+H2(g) ΔH,相关物质的燃烧热数据如下表所示:
物质
C2H6(g)
C2H4(g)
H2(g)
燃烧热ΔH/( kJ·mol−1)
-1560
-1411
-286
①ΔH=_________kJ·mol−1。
②提高该反应平衡转化率的方法有_________、_________。
③容器中通入等物质的量的乙烷和氢气,在等压下(p)发生上述反应,乙烷的平衡转化率为α。反应的平衡常数Kp=_________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)高温下,甲烷生成乙烷的反应如下:2CH4C2H6+H2。反应在初期阶段的速率方程为:r=k×,其中k为反应速率常数。
①设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=_____ r1。
②对于处于初期阶段的该反应,下列说法正确的是_________。
A.增加甲烷浓度,r增大 B.增加H2浓度,r增大
C.乙烷的生成速率逐渐增大 D.降低反应温度,k减小
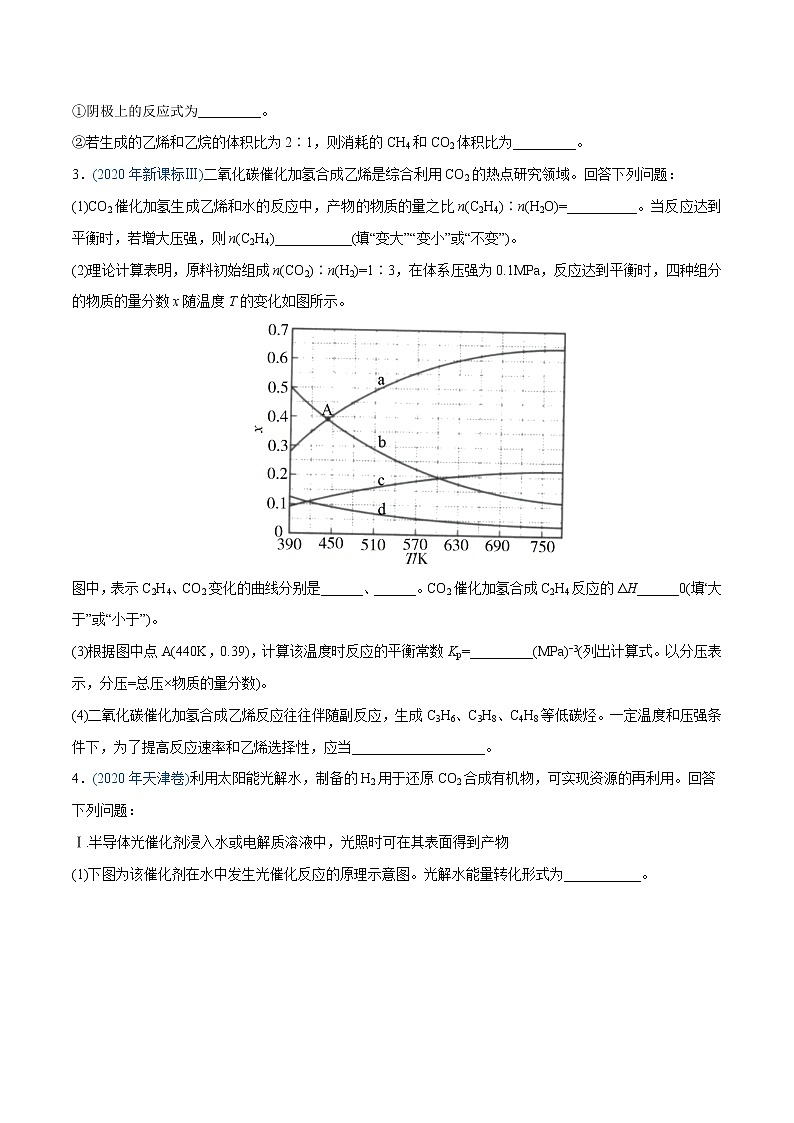
(3)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
①阴极上的反应式为_________。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH4和CO2体积比为_________。
【答案】(1)①137 ②升高温度 减小压强(增大体积) ③
(2)①1-α ②AD
(3)①CO2+2e−=CO+O2− ②6∶5
【解析】
【分析】(1)①先写出三种气体的燃烧热的热化学方程式,然后根据盖斯定律进行计算,得到目标反应的∆H;
②反应C2H6(g)C2H4(g) + H2(g)为气体体积增大的吸热反应,升高温度、减小压强平衡等都向正反应方向移动;
③根据已知乙烷的转化率,设起始时加入的乙烷和氢气各为1mol,列出三段式,求出平衡时各物质的分压,带入平衡常数的计算公式进行计算;
(2)①根据r=k×,若r1=kc,甲烷转化率为甲烷的浓度为c(1-),则r2= kc(1-);
②根据反应初期的速率方程为:r=k×,其中k为反应速率常数,据此分析速率变化的影响因素;
(3)①由图可知,CO2在阴极得电子发生还原反应,电解质传到O2-,据此写出电极反应;
②令生成乙烯和乙烷分别为2体积和1体积,根据阿伏加德罗定律,同温同压下,气体体积比等于物质的量之比,再根据得失电子守恒,得到发生的总反应,进而计算出为消耗CH4和CO2的体积比。
【详解】(1)①由表中燃烧热数值可知:
①C2H6(g)+O2(g)=2CO2(g) +3H2O(l) ∆H1= -1560kJ∙mol-1;②C2H4(g)+3O2(g)=2CO2(g) +2H2O(l) ∆H2= -1411kJ∙mol-1;③H2(g)+O2(g)=H2O(l) ∆H3= -286kJ∙mol-1;根据盖斯定律可知,①-②-③得C2H6(g) =C2H4(g) + H2(g),则∆H= ∆H1-∆H2-∆H3=( -1560kJ∙mol-1)-( -1411kJ∙mol-1)- ( -286kJ∙mol-1)=137kJ∙mol-1,故答案为137;
②反应C2H6(g) C2H4(g) + H2(g)为气体体积增大的吸热反应,升高温度、减小压强平衡都向正反应方向移动,故提高该反应平衡转化率的方法有升高温度、减小压强(增大体积);
③设起始时加入的乙烷和氢气各为1mol,列出三段式,
C2H6(g) C2H4(g) + H2(g)
起始(mol) 1 0 1
转化(mol) α α
平衡(mol) 1- 1+
平衡时,C2H6、C2H4和H2平衡分压分别为p、p和p,则反应的平衡常数为Kp=;
(2) ①根据r=k×,若r1= kc,甲烷转化率为甲烷的浓度为c(1-),则r2= kc(1-),所以r2=(1-)r1;
②A.增大反应物浓度反应速率增大,故A说法正确;
B.由速率方程可知,初期阶段的反应速率与氢气浓度无关,故B说法错误;
C.反应物甲烷的浓度逐渐减小,结合速率方程可知,乙烷的生成速率逐渐减小,故C说法错误;
D.化学反应速率与温度有关,温度降低,反应速率常数减小,故D正确。
答案选AD。
(3) ①由图可知,CO2在阴极得电子发生还原反应,电极反应为CO2+2e-=CO+O2-;
②令生成乙烯和乙烷分别为2体积和1体积,根据阿伏加德罗定律,同温同压下,气体体积比等于物质的量之比,再根据得失电子守恒,得到发生的总反应为:6CH4+5CO2=2C2H4+ C2H6+5H2O+5CO,即消耗CH4和CO2的体积比为6:5。
3.(2020年新课标Ⅲ)二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。回答下列问题:
(1)CO2催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C2H4)∶n(H2O)=__________。当反应达到平衡时,若增大压强,则n(C2H4)___________(填“变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1MPa,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
图中,表示C2H4、CO2变化的曲线分别是______、______。CO2催化加氢合成C2H4反应的ΔH______0(填“大于”或“小于”)。
(3)根据图中点A(440K,0.39),计算该温度时反应的平衡常数Kp=_________(MPa)−3(列出计算式。以分压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C3H6、C3H8、C4H8等低碳烃。一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当___________________。
3.【答案】(1)1∶4 变大
(2)d c 小于
(3)或等
(4)选择合适催化剂等
【解析】
【分析】根据质量守恒定律配平化学方程式,可以确定产物的物质的量之比。根据可逆反应的特点分析增大压强对化学平衡的影响。根据物质的量之比等于化学计量数之比,从图中找到关键数据确定代表各组分的曲线,并计算出平衡常数。根据催化剂对化反应速率的影响和对主反应的选择性,工业上通常要选择合适的催化剂以提高化学反应速率、减少副反应的发生。
【详解】(1)CO2催化加氢生成乙烯和水,该反应的化学方程式可表示为2CO2+6H2 ⇌ CH2 = CH2+4H2O,因此,该反应中产物的物质的量之比n(C2H4):n(H2O)=1:4。由于该反应是气体分子数减少的反应,当反应达到平衡状态时,若增大压强,则化学平衡向正反应方向移动,n(C2H4)变大。
(2) 由题中信息可知,两反应物的初始投料之比等于化学计量数之比;由图中曲线的起点坐标可知,c和a所表示的物质的物质的量分数之比为1:3、d和b表示的物质的物质的量分数之比为1:4,则结合化学计量数之比可以判断,表示乙烯变化的曲线是d,表示二氧化碳变化曲线的是c。由图中曲线的变化趋势可知,升高温度,乙烯的物质的量分数减小,则化学平衡向逆反应方向移动,则该反应为放热反应,∆H小于0。
(3) 原料初始组成n(CO2)∶n(H2)=1∶3,在体系压强为0.1Mpa建立平衡。由A点坐标可知,该温度下,氢气和水的物质的量分数均为0.39,则乙烯的物质的量分数为水的四分之一,即,二氧化碳的物质的量分数为氢气的三分之一,即,因此,该温度下反应的平衡常数(MPa)-3=(MPa)-3。
(4)工业上通常通过选择合适的催化剂,以加快化学反应速率,同时还可以提高目标产品的选择性,减少副反应的发生。因此,一定温度和压强下,为了提高反应速率和乙烯的选择性,应当选择合适的催化剂。
4.(2020年天津卷)利用太阳能光解水,制备的H2用于还原CO2合成有机物,可实现资源的再利用。回答下列问题:
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
(1)下图为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为___________。
(2)若将该催化剂置于Na2SO3溶液中,产物之一为,另一产物为__________。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________。
Ⅱ.用H2还原CO2可以在一定条下合成CH3OH(不考虑副反应):
(3)某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为___________。
(4)恒压下,CO2和H2的起始物质的量比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H2O。
①甲醇平衡产率随温度升高而降低的原因为____________。
②P点甲醇产率高于T点的原因为___________。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为___________°C。
Ⅲ.调节溶液pH可实现工业废气CO2的捕获和释放
(5)的空间构型为__________。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时,=1:_______:__________。
【答案】I.(1)光能转化为化学能 (2)H2
II.(3)
(4)①该反应为放热反应,温度升高,平衡逆向移动(或平衡常数减小)
②分子筛膜从反应体系中不断分离出H2O,有利于反应正向进行,甲醇产率升高
③210
(5)平面(正)三角形
【解析】I.(1)根据图示,该催化剂在水中发生光催化反应的方程式为2H2O2H2↑+O2↑,光解水能量转化形式为光能转化为化学能。
(2)若将该催化剂置于Na2SO3溶液中,产物之一为,被氧化成,则H+被还原为H2,即另一产物为H2;若将该催化剂置于AgNO3溶液中,产物之一为O2,氧元素的化合价升高,O2为氧化产物,则生成另一产物的反应为还原反应,由于Ag+得电子能力大于H+,故生成另一产物的离子反应式为Ag++e-=Ag。
II.(3) CO2和H2的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,CH3OH的产率为b,则生成的CH3OH物质的量浓度为abmol/L,根据三段式
则反应的平衡常数K== =。
(4)①该反应为放热反应(∆H<0),温度升高,平衡逆向移动(或平衡常数减小),故甲醇平衡产率随温度升高而降低;
②因为分子筛膜能选择性分离出H2O,c(H2O)减小,有利于反应正向进行,甲醇产率升高,故P点甲醇产率高于T点。
③根据图示,使用该分子筛膜210℃时甲醇的产率最大,故在此条件下采用该分子筛膜时的最佳反应温度为210℃。
III.(5)中C的孤电子对数为×(4+2-3×2)=0,σ键电子对数为3,价层电子对数为3,C上没有孤电子对,故的空间构型为平面正三角形;H2CO3的电离方程式为H2CO3⇌H++、⇌ H++,则Ka1= 、Ka2=,当溶液的pH=12时,c(H+)=1×10-12mol/L,将其代入Ka1、Ka2中分别求出c()=1012Ka1 c(H2CO3)、c()=1012Ka2 c()=1024Ka1Ka2 c(H2CO3),则c(H2CO3):c():c()=1:(1012Ka1):(1024Ka1Ka2)。
5.(2020年江苏卷)CO2/ HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO-,其离子方程式为__________;其他条件不变,HCO3-转化为HCOO-的转化率随温度的变化如图-1所示。反应温度在40℃~80℃范围内,HCO3-催化加氢的转化率迅速上升,其主要原因是_____________。
(2) HCOOH燃料电池。研究 HCOOH燃料电池性能的装置如图-2所示,两电极区间用允许K+、H+通过的半透膜隔开。
①电池负极电极反应式为_____________;放电过程中需补充的物质A为_________(填化学式)。
②图-2所示的 HCOOH燃料电池放电的本质是通过 HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为_______________。
(3) HCOOH催化释氢。在催化剂作用下, HCOOH分解生成CO2和H2可能的反应机理如图-3所示。
①HCOOD催化释氢反应除生成CO2外,还生成__________(填化学式)。
②研究发现:其他条件不变时,以 HCOOK溶液代替 HCOOH催化释氢的效果更佳,其具体优点是_______________。
【答案】(1) 温度升高反应速率增大,温度升高催化剂的活性增强 (2)① H2SO4
②或
(3)①HD ②提高释放氢气的速率,提高释放出氢气的纯度
【解析】
【分析】(1)根据元素守恒和电荷守恒书写离子方程式;从温度对反应速率的影响以及温度对催化剂的影响的角度分析。
(2)该装置为原电池装置,放电时HCOOˉ转化为被氧化,所以左侧为负极,Fe3+转化为Fe2+被还原,所以右侧为正极。
(3)HCOOH生成HCOOˉ和H+分别与催化剂结合,在催化剂表面HCOOˉ分解生成CO2和Hˉ,之后在催化剂表面Hˉ和第一步产生的H+反应生成H2。
【详解】(1)含有催化剂的KHCO3溶液中通入H2生成HCOOˉ,根据元素守恒和电荷守恒可得离子方程式为:+H2HCOOˉ+H2O;反应温度在40℃~80℃范围内时,随温度升高,活化分子增多,反应速率加快,同时温度升高催化剂的活性增强,所以的催化加氢速率迅速上升;
(2)①左侧为负极,碱性环境中HCOOˉ失电子被氧化为,根据电荷守恒和元素守恒可得电极反应式为HCOOˉ+2OHˉ-2eˉ= +H2O;电池放电过程中,钾离子移向正极,即右侧,根据图示可知右侧的阴离子为硫酸根,而随着硫酸钾不断被排除,硫酸根逐渐减少,铁离子和亚铁离子进行循环,所以需要补充硫酸根,为增强氧气的氧化性,溶液最好显酸性,则物质A为H2SO4;
②根据装置图可知电池放电的本质是HCOOH在碱性环境中被氧气氧化为,根据电子守恒和电荷守恒可得离子方程式为2HCOOH+O2+2OHˉ = 2+2H2O或2HCOOˉ+O2= 2;
(3)①根据分析可知HCOOD可以产生HCOOˉ和D+,所以最终产物为CO2和HD(Hˉ与D+结合生成);
②HCOOK是强电解质,更容易产生HCOOˉ和K+,更快的产生KH,KH可以与水反应生成H2和KOH,生成的KOH可以吸收分解产生的CO2,从而使氢气更纯净,所以具体优点是:提高释放氢气的速率,提高释放出氢气的纯度。
【点睛】第3小题为本题难点,要注意理解图示的HCOOH催化分解的反应机理,首先HCOOH分解生成H+和HCOOˉ,然后HCOOˉ再分解成CO2和Hˉ,Hˉ和H+反应生成氢气。
6.(2020年江苏卷)吸收工厂烟气中的SO2,能有效减少SO2对空气的污染。氨水、ZnO水悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。
已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、HSO3-、SO32-的物质的量分数随pH的分布如图-1所示。
(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为___________;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是_____________(填化学式)。
(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40mim内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是____________(填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为_______________。
(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低SO生成速率越大,其主要原因是__________;随着氧化的进行,溶液的pH将__________(填“增大”、“减小”或“不变”)。
【答案】(1)或 HSO
(2)ZnSO3 或
(3)随着pH降低,HSO浓度增大 减小
【解析】
【分析】向氨水中通入少量的SO2,反应生成亚硫酸铵,结合图像分析pH=6时溶液中浓度最大的阴离子;通过分析ZnO吸收SO2后产物的溶解性判断吸收率变化的原因;通过分析与氧气反应的生成物,分析溶液pH的变化情况。
【详解】(1)向氨水中通入少量SO2时,SO2与氨水反应生成亚硫酸铵,反应的离子方程式为2NH3+H2O+SO2=2+(或2NH3·H2O +SO2=2++H2O);根据图-1所示,pH=6时,溶液中不含有亚硫酸,仅含有和,根据微粒物质的量分数曲线可以看出溶液中阴离子浓度最大的是;
(2)反应开始时,悬浊液中的ZnO大量吸收SO2,生成微溶于水的ZnSO3,此时溶液pH几乎不变;一旦ZnO完全反应生成ZnSO3后,ZnSO3继续吸收SO2生成易溶于水的Zn(HSO3)2,此时溶液pH逐渐变小,SO2的吸收率逐渐降低,这一过程的离子方程式为ZnSO3+SO2+H2O=Zn2++2(或ZnO+2SO2+H2O=Zn2++2)
(3)可以经氧气氧化生成,这一过程中需要调节溶液pH在4.5~6.5的范围内,pH越低,溶液中的的浓度越大,使得催化氧化过程中反应速率越快;随着反应的不断进行,大量的反应生成,反应的离子方程式为2+O2=2+2H+,随着反应的不断进行,有大量的氢离子生成,导致氢离子浓度增大,溶液pH减小。
专题十三 化学反应原理的综合应用五年高考化学真题分类训练(2019-2023)Word版含解析: 这是一份专题十三 化学反应原理的综合应用五年高考化学真题分类训练(2019-2023)Word版含解析,共17页。试卷主要包含了5 kJ⋅ml−1 ,8℃ 时平衡常数K′p=1,00转化压强/kPa等内容,欢迎下载使用。
2023年高考化学真题分类汇编 专题14 化学反应原理综合题: 这是一份2023年高考化学真题分类汇编 专题14 化学反应原理综合题,文件包含专题14化学反应原理综合题解析版docx、专题14化学反应原理综合题原卷版docx等2份试卷配套教学资源,其中试卷共63页, 欢迎下载使用。
高中化学专题14 化学反应原理综合-2021年高考化学真题与模拟题分类训练(学生版): 这是一份高中化学专题14 化学反应原理综合-2021年高考化学真题与模拟题分类训练(学生版),共44页。












