





中考化学专项复习课件 专项04 探究氢氧化钠与二氧化碳 课件
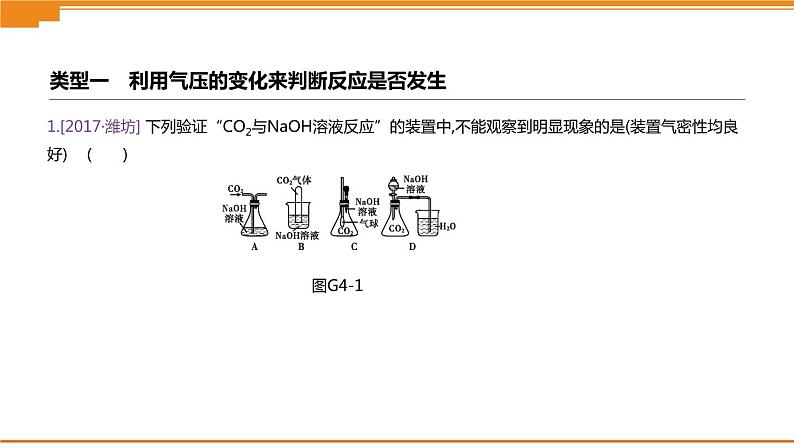
展开1.[2017·潍坊] 下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)( )
类型一 利用气压的变化来判断反应是否发生
[解析] 二氧化碳和氢氧化钠反应无明显现象,要借助反应中气压的变化或者反应中生成物的性质来验证二者发生了化学反应。
实验设计:三颈烧瓶中充满二氧化碳气体,A颈、B颈分别连接充满氢氧化钠溶液和盐酸的注射器,C颈插有两端开口的玻璃导管(伸入瓶内的一端连有小气球),装置气密性良好。实验操作:先通过A颈往瓶内注入氢氧化钠溶液,观察到小气球的形状发生了变化;过一段时间后再通过B颈往瓶中注入盐酸,发现小气球的形状又发生了改变。请描述小气球形状的变化情况,并对此作出合理的解释: 。
2.[2018·金华] 某拓展性学习小组在学校科学实验创新比赛中,做了一个有趣的实验,装置如图G4-2。
[解析] 先通过A颈往瓶内注入氢氧化钠溶液,氢氧化钠与二氧化碳反应导致瓶内的压强减小,气球胀大,过一段时间后再通过B颈往瓶中注入盐酸,盐酸与碳酸钠反应生成二氧化碳,瓶内压强增大,气球变瘪。
[答案]开始时,氢氧化钠与二氧化碳反应导致瓶内压强变小,气球变大;注入盐酸后,盐酸与碳酸钠反应生成二氧化碳,导致瓶内的压强增大,气球变瘪
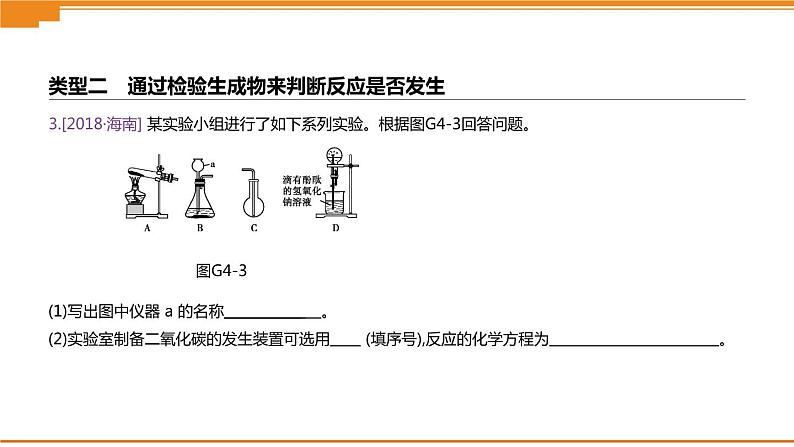
3.[2018·海南] 某实验小组进行了如下系列实验。根据图G4-3回答问题。
类型二 通过检验生成物来判断反应是否发生
(1)写出图中仪器 a 的名称 。 (2)实验室制备二氧化碳的发生装置可选用 (填序号),反应的化学方程为 。
②对于无明显现象的反应,根据化学反应的基本特征,应如何证明其发生了化学反应? 请写出你的设计思路: 。
(3)二氧化碳通入氢氧化钠溶液中无明显现象。该实验小组的同学为了使二氧化碳与氢氧化钠溶液反应产生明显现象,用烧瓶收集二氧化碳后,按 D 装置进行实验,挤压胶头滴管(胶头滴管中盛有浓的氢氧化钠溶液),打开止水夹,形成红色喷泉。 有同学提出疑问,该实验中二氧化碳减少是否能证明二氧化碳确实与氢氧化钠发生了反应?①若二氧化碳与氢氧化钠发生了反应,则需要证明反应后的溶液中有 生成。请你设计实验证明(简要说明操作、现象和结论):
[答案] (1)长颈漏斗
(3)①碳酸钠 取少量反应后的溶液于试管中,加入几滴氯化钡(或氢氧化钡)溶液,如有白色沉淀产生,则证明有碳酸钠生成(若加稀盐酸或稀硫酸产生气泡也可,但必须指明酸要足量) ②证明反应物消失或有新物质生成
[解析] (1)据图可知仪器 a 的名称为长颈漏斗。(2)实验室用稀盐酸和大理石或石灰石反应生成氯化钙、二氧化碳和水,反应的化学方程式为CaCO3+2HCl CaCl2+H2O+CO2↑,可选用发生装置B。(3)①二氧化碳与氢氧化钠发生反应后,生成了碳酸钠,若要检验二氧化碳确实与氢氧化钠发生了反应,只需证明有碳酸钠生成就可以了。设计实验方案如下:取少量反应后的溶液于试管中,加入几滴氯化钡(或氢氧化钡)溶液,如有白色沉淀产生,则证明有碳酸钠生成(若加稀盐酸或稀硫酸产生气泡也可,但必须指明酸要足量)。②对于无明显现象的反应,根据化学反应的基本特征,可以采用证明反应物消失或有新物质生成进行验证。
4.[2018·黄冈] 对比实验是化学研究中经常采用的方法。化学兴趣小组的同学在研究CO2通入NaOH溶液是否发生了反应,设计了下列两组实验。请和化学兴趣小组的同学一起探究并回答问题。设计与实验
探究与结论(1)实验Ⅰ中步骤一看不到明显现象,步骤二产生的现象是 。 (2)实验Ⅱ中步骤二看到有白色沉淀析出,则发生反应的化学方程式是 。 (3)在实验Ⅱ的步骤一中,CO2和NaOH溶液一定发生了化学反应,但却看不到明显的现象,原因是 。
[答案] (1)有气泡冒出 (2)CaCl2+Na2CO3 CaCO3↓+2NaCl (3)CO2与NaOH溶液反应生成水和易溶于水的Na2CO3
请你和化学兴趣小组的同学一起利用以上信息再设计实验Ⅲ,证明CO2确实与NaOH发生了化学反应。实验Ⅲ的操作为 。 看到的现象是 。
[答案]向氢氧化钠的乙醇溶液中通入二氧化碳 有白色沉淀析出
[解析] 20 ℃时,氢氧化钠在乙醇中溶解度为17.3 g,碳酸钠在乙醇中的溶解度<0.01 g,所以氢氧化钠在乙醇中可溶,碳酸钠在乙醇中为沉淀,因此在乙醇中生成的碳酸钠不能溶在乙醇中。实验Ⅲ的操作为向氢氧化钠的乙醇溶液中通入二氧化碳,看到的现象是有白色沉淀生成。
5.[2018·泰州] 为探究CO2与NaOH溶液发生的反应,某兴趣小组尝试用不同的方式进行实验。查阅资料 Ⅰ.20 ℃时,几种物质在水中的溶解度见下表:
Ⅱ.本实验条件下,Na2CO3溶液和NaHCO3溶液的pH分别约为11.0和8.5。
(1)实验一:小雨取一充满CO2的矿泉水瓶,加入一定量的水,立即拧紧瓶盖,振荡,发现瓶子变瘪;小雨另取一相同的充满CO2的矿泉水瓶,向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X,此时观察到的现象是 。实验中,小雨采用两只矿泉水瓶做对比实验的目的是 。 (2)实验二:为检验CO2与NaOH溶液反应的产物,小亮取实验一所得溶液X少许,向其中滴加BaCl2溶液,有白色沉淀产生,该反应的化学方程式为 。实验中不宜将BaCl2溶液换成CaCl2溶液的原因是 (3)实验三:小华取实验一所得溶液X少许,向其中加入过量的BaCl2溶液,振荡,静置,取上层清液,滴入1滴酚酞溶液,发现溶液呈 色,证明溶液X中有NaOH剩余。实验中,小华没有直接向少量溶液X中滴入酚酞溶液,理由是 。
(4)实验四:兴趣小组将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中溶液的pH和温度变化,结果如图G4-5甲、乙所示。
图甲中,BC段发生反应的化学方程式为 。图乙中,DE段温度变化的原因是 。 反思感悟 (5)实验从CO2减少、NaOH减少,Na2CO3生成等物质的变化,以及 转化等视角多维度探究CO2与NaOH发生了反应,对于现象不明显的化学反应,可以通过现代技术手段进行数据测定,实现反应过程的“可视化”。
中考化学二轮复习专题课件- 氢氧化钠变质的探究 (含答案): 这是一份中考化学二轮复习专题课件- 氢氧化钠变质的探究 (含答案),共16页。PPT课件主要包含了氢氧化钠是否变质了,课堂练习一,氢氧化钠没有变质,氢氧化钠全部变质,氢氧化钠部分变质,种情况,只有NaOH,只有Na2CO3,课堂练习二,课堂练习三等内容,欢迎下载使用。
中考化学二轮复习实验课件:氢氧化钠和二氧化碳反应的探究(含答案): 这是一份中考化学二轮复习实验课件:氢氧化钠和二氧化碳反应的探究(含答案),共9页。
2023年中考化学复习---探究氢氧化钠变质课件: 这是一份2023年中考化学复习---探究氢氧化钠变质课件,共21页。PPT课件主要包含了学习目标,已变质等内容,欢迎下载使用。












