

河北省邯郸市2026届高三上学期11月阶段检测化学试卷(学生版)
展开 这是一份河北省邯郸市2026届高三上学期11月阶段检测化学试卷(学生版),共9页。试卷主要包含了 下列离子方程式正确的是等内容,欢迎下载使用。
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案字母涂黑,如需改动,用橡皮擦干净后,再选涂其他答案字母。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
考试时间75分钟,满分100分
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Na-23 Al-27 Cl-35.5 K-39 Fe-56 Cu-64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 我国古代文献中记载有丰富的化学知识。下列说法错误的是
A. 《吕氏春秋》中记载有关青铜的知识,青铜的熔点比纯铜高,硬度比铜大
B. 《抱朴子内篇·黄白》中“曾青涂铁,铁赤色如铜”(“曾青”即硫酸铜溶液),说明铁比铜活泼
C. 《本草纲目》中载有一药物,名“铜青”,即铜器上的绿色物质,该物质属于碱式盐
D. 《新修本草》中关于青矾()的描述“本来绿色,新出窟未见风者,正如瑠璃…烧之赤色…”,赤色物质是
2. 劳动创造了人,劳动离不开化学。下列劳动过程涉及的化学知识解释错误的是
A. 高铁列车服务员每天用“84”消毒液消毒车厢,因为含氯消毒剂具有强氧化性
B. 工人利用铝热反应焊接钢轨,是利用高温下铝能还原氧化铁
C. 豆腐坊制作豆腐时加入石膏或卤水,是由于电解质可以与溶液反应生成沉淀
D. 工厂生产的漂白粉需要密封避光保存,原因是漂白粉在空气中易变质
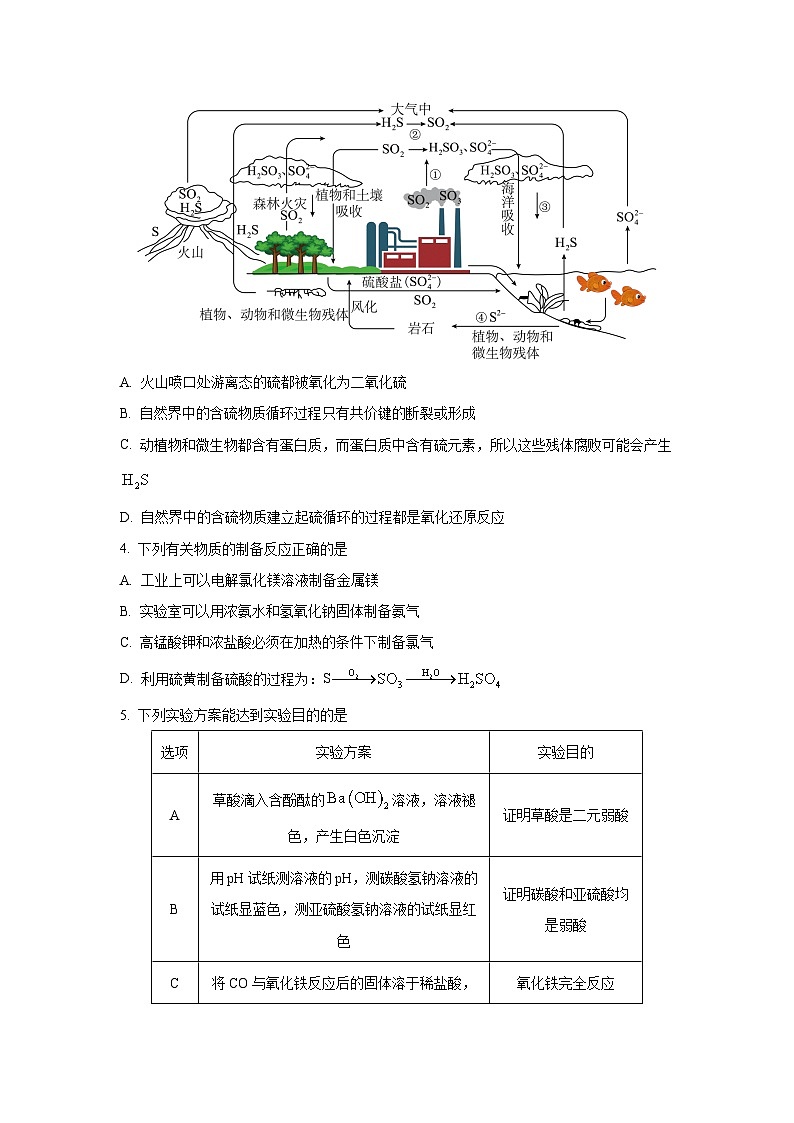
3. 自然界中的含硫物质通过各种化学过程建立起硫循环,其循环过程如下图所示,下列说法正确的是
A. 火山喷口处游离态的硫都被氧化为二氧化硫
B. 自然界中的含硫物质循环过程只有共价键的断裂或形成
C. 动植物和微生物都含有蛋白质,而蛋白质中含有硫元素,所以这些残体腐败可能会产生
D. 自然界中的含硫物质建立起硫循环的过程都是氧化还原反应
4. 下列有关物质的制备反应正确的是
A. 工业上可以电解氯化镁溶液制备金属镁
B. 实验室可以用浓氨水和氢氧化钠固体制备氨气
C. 高锰酸钾和浓盐酸必须在加热的条件下制备氯气
D. 利用硫黄制备硫酸的过程为:S
5. 下列实验方案能达到实验目的的是
A. AB. BC. CD. D
6. 摩尔盐[]是一种重要的化工原料,用途十分广泛,可以作净水剂,还可以与鞣酸、没食子酸等混合后配制蓝黑墨水;在空气中比稳定,是分析化学中重要的基准物质。摩尔盐加热分解,反应为。用废铁屑(含有少量)制备摩尔盐的流程如图:
下列说法正确的是
A. 步骤1和步骤2加热的最好方式是用酒精灯直接加热
B. 稀硫酸处理后的溶液中加入KSCN溶液,溶液变成红色(忽略空气的氧化)
C. 步骤3实验操作有蒸发浓缩、冷却结晶、过滤、洗涤和干燥
D. 摩尔盐分解反应中被氧化的元素有1种
7. 由和NO反应生成和的能量变化如图所示。下列说法错误的是
A. 该反应涉及氮元素的四种化合价
B. 反应过程中有极性键的断裂和极性键的形成
C. 该反应是放热反应
D. 每有139 kJ能量变化,转移4 ml电子
8. 下列离子方程式正确的是
A. 将过量浓氨水加入硫酸铜溶液中:
B. 碳酸氢镁溶液中加入过量的石灰乳:
C. 将通入溶液中:
D. 氧化亚铁溶于稀硝酸:
9. 某无色废水可能存在、、、、、、、、、、中的几种,且各种离子浓度相等。取100 mL该废水进行如图所示实验,下列说法错误的是
A. 不用实验即可确定无色废水中不含有和
B. 白色沉淀的质量最大是7.8 g
C 该废水中加入溶液,产生白色沉淀
D. 对该废水进行焰色试验,火焰显紫色
10. 设为阿伏加德罗常数值,下列说法错误的是
A. 0.1 ml氯气溶于水中,溶液中氯离子数小于0.1
B. 1 ml 晶体中含离子总数为3
C. 常温下,5.6 g铁分别与足量浓硝酸和稀硝酸反应,转移电子数都是0.3
D. 在含0.1 ml 硫化钠的溶液中,
11. 化学学习小组通过如图所示装置探究与能否反应产生,已知的升华温度为315℃。下列相关说法正确的是
A. 试管壁附着的黄色液滴是,黄色气体一定是氯气
B. 试管A中氧化了全部氯元素
C. 试管B中发生的反应只有,使淀粉变蓝
D. 该实验会有试管塞弹出或试管破裂的风险
12. 部分含硫、氮元素的价-类二维图如下。
已知:d为红棕色物质。下列说法正确的是
A. a与a'、d与c'都可以发生氧化还原反应
B. c、d都是大气污染物,利用a可以消除它们的污染
C. e和e'的浓溶液按体积比1:3混合,可以溶解金、铂等绝大多数金属
D. a'和c'反应的氧化产物和还原产物的物质的量之比是1:2
13. 锂硫电池的工作原理如图所示。下列说法正确的是
已知:一个电子带有的电量为C。
A. 该电池的电解质换成高浓度的水溶液,可以增强的导电性
B. 电池充电时,从左侧通过阳离子膜移到右侧
C. 电池放电时,电子的流动方向为金属锂片→用电器→集流板→阳离子膜→金属锂片
D. 金属锂质量每减小14 g,经过用电器电量约是C
14. 减少排放,捕集并利用是我国能源领域的一个重要战略方向。在一定温度和压强下,以、为原料制备二甲醚的主要反应如下:
① ;
② ;
③
下列说法错误的是
A. 反应①的反应物总能量低于生成物总能量
B. 反应②中形成新化学键释放的总能量大于破坏旧化学键吸收的总能量
C. 反应③能表示其在标准状况下的热化学方程式
D. 反应③的
二、非选择题:本题共4小题,共58分。
15. 四水合草酸铜钾{,}可作为合成复杂无机物的前驱体或中间体,制备方法如下:
已知晶体极易风化。回答下列问题:
(1)向溶液中加入NaOH溶液并加热的现象是______。
(2)时制得和的混合液,该反应的化学方程式为______。
(3)趁热过滤目的是______。
(4)晶体的保存方法是______。
(5)测定产品纯度时需要高锰酸钾溶液70 mL,配制高锰酸钾标准液用到的玻璃仪器有______(填字母)。
(6)热重分析是测定结晶水合物分解和失重过程的常用方法之一,晶体的热重曲线如图所示,B点时化合物的化学式是______,开始加热至C点时发生反应的化学方程式是______。
16. 海洋经济发展区建设已经上升为国家战略,浩瀚的海洋里蕴藏着丰富的化学资源。下图是某工厂对海水资源的综合利用的示意图。
请回答以下问题:
(1)流程图中发生分解反应的有______(填序号),发生氧化还原反应的有______(填序号)。
(2)粗盐制备精盐的过程中发生的变化是______(填“物理变化”“化学变化”或“物理变化和化学变化”)。
(3)电解饱和食盐水的离子方程式是______,生成标准状况下22.4 L,可以得到50% NaOH溶液______g,在阳极区生成的物质是______(填化学式)。
(4)脱盐工序在实验室中利用NaOH和NaCl溶解度上的差异,通过______(填操作名称)可以除去氯化钠。
17. “84”消毒液是生活中常见的一种消毒剂,常用于环境的消毒,其主要成分是NaClO。今有一瓶某品牌“84”消毒液1000 mL,质量分数为25%,密度为1.192 。
(1)资料表明,“84”消毒液使用过程中起主要消毒作用的是次氯酸。在日常生活中使用“84”消毒液,需要在空气中放置一段时间后,漂白效果更好。用化学方程式解释产生次氯酸的原因:______。
(2)该“84”消毒液的物质的量浓度为______;一瓶上述“84”消毒液理论上能吸收空气中______L的(标准状况下),所以“84”消毒液应该密封保存。
(3)探究“84”消毒液的性质。取6 mL“84”消毒液,分装在3支试管中。
①向试管1中滴入3滴紫色石蕊溶液,溶液变为蓝色,说明漂白液呈______(填“酸性”或“碱性”),加入1 mL蒸馏水,蓝色变浅,一段时间后蓝色褪去。
②向试管2中滴入3滴紫色石蕊溶液,滴入1 mL 0.0002 盐酸,溶液迅速褪色,原因是(用文字和离子方程式表示)______。
③向试管3中滴入3滴紫色石蕊溶液,加入1 mL 4 盐酸,溶液迅速褪色,并产生黄绿色气体,发生反应的离子方程式为______。试管2和试管3中反应现象有所不同,说明______。
18. 纳米级硒化铜()是钠离子电池的正极材料。某小组以黄铜矿(主要含有,还有少量、等)为原料,在酸性条件下生物催化氧化法制备纳米级硒化铜的工艺流程如图:
回答下列问题:
(1)为了提高浸取率,可以采取的措施有______(答出两种即可)。
(2)黄铜矿浸取并过滤后得到的化合物滤渣是______(填化学式)。
(3)实验室完成过滤操作用到的玻璃仪器有______。
(4)加入过量氨水时,发生多种反应,写出硫酸铁参与反应的离子方程式:______。
(5)是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞组成变化如图所示:
放电时由转化为NaCuSe的电极反应式为______;充电时由转化为的电极反应式为______。
选项
实验方案
实验目的
A
草酸滴入含酚酞的溶液,溶液褪色,产生白色沉淀
证明草酸是二元弱酸
B
用pH试纸测溶液的pH,测碳酸氢钠溶液的试纸显蓝色,测亚硫酸氢钠溶液的试纸显红色
证明碳酸和亚硫酸均是弱酸
C
将CO与氧化铁反应后的固体溶于稀盐酸,滴加KSCN溶液,溶液无明显现象
氧化铁完全反应
D
向蔗糖中加入浓硫酸,并将产生的气体通过适量溴水,蔗糖变黑、膨胀,溴水褪色,有气泡冒出
浓硫酸具有脱水性和强氧化性
实验装置
实验操作和现象
①加热试管A,部分固体溶解,上方出现白雾,稍后,试管A中产生黄色气体,试管壁附着黄色液滴
②试管B中溶液变蓝
③将试管A中固体产物分离得到固体和溶液
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





