




四川省遂宁市射洪中学2026届高三上学期第一次模拟考试(一模)化学试卷(Word版附解析)
展开 这是一份四川省遂宁市射洪中学2026届高三上学期第一次模拟考试(一模)化学试卷(Word版附解析),文件包含四川省遂宁市射洪中学2026届高三上学期第一次模拟考试一模化学试题原卷版docx、四川省遂宁市射洪中学2026届高三上学期第一次模拟考试一模化学试题Word版含解析docx等2份试卷配套教学资源,其中试卷共34页, 欢迎下载使用。
(考试时间:75 分钟 满分:100 分)
注意事项:
1.答卷前,考生务必将自己的班级、姓名、考号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡对应题号的位置上。写在本试卷上无效。
4.考试结束后,将答题卡交回。
可能用到的相对原子量:H-1 Be-9 C-12 O-16 S-32 Cl-35.5 Cu-64 Zn-65 Sr-88
Zr-91
第 I 卷(选择题,共 45 分)
一、选择题:本题共 15 小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 物质性质决定用途,下列两者对应关系错误的是
A. 明矾溶液显酸性,中国古代利用明矾溶液清除铜镜表面的铜锈
B. NaHCO3 溶液显碱性,常做烘焙糕点的膨松剂
C. 维生素 C 具有还原性,可用作食品抗氧化剂
D. 聚乳酸制备的一次性餐具具有很高的生物降解性
【答案】B
【解析】
【详解】A. 明矾(KAl(SO4)2·12H2O)水解后溶液呈酸性,能与铜锈(碱式碳酸铜)反应,A 正确;
B. NaHCO3 的膨松作用源于其受热分解产生 CO2,而非溶液呈碱性,B 错误;
C. 维生素 C 具有还原性,可还原与食品接触的氧化性物质,从而防止食品被氧化,也就是可用作食品抗氧
化剂,C 正确;
D 聚乳酸由乳酸聚合而成,可被微生物降解,所以可制作一次性餐具,D 正确;
故选 B。
2. 下列化学用语表示正确的是
A. H2O 分子的球棍模型:
第 1页/共 24页
B. BF3 的价层电子对互斥模型:
C. KI 的电子式:
D. CH3CH(CH2CH3)2 的名称:3−甲基戊烷
【答案】D
【解析】
【详解】A.H2O 分子为 V 形结构,图示为直线形,A 错误;
B.BF3 中 B 原子价层电子对数 ,无孤电子对,价层电子对互斥模型应为平面三角形,B
错误;
C.KI 是离子化合物,电子式中 I⁻需标注最外层电子(用中括号括起来并注明电荷),钾离子用离子符号代
表,则正确 电子式为 ,C 错误;
D.CH3CH(CH2CH3)2 主链为 5 个碳(戊烷),3 号碳连甲基,名称为 3−甲基戊烷,D 正确;
故答案选 D。
3. 工业制备硫酸流程如下,设 NA 为阿伏加德罗常数的值。下列说法正确的是
A. 1 ml 中 S 原子的价层电子对数为 4NA
B. 足量 SO2 与 32 gO2 充分反应,生成 SO3 的分子数为 2 NA
C. 黄铁矿与足量 O2 反应,生成 1 mlSO2,转移电子数 5 NA
D. 标准状况下,22.4 LSO3 所含的原子数为 4 NA
【答案】A
【解析】
【分析】黄铁矿在空气中加热反应生成二氧化硫,随后二氧化硫继续被氧化为三氧化硫,三氧化硫被浓硫
酸吸收生成硫酸,以此解题。
【详解】A. 中 S 原子的价层电子对数为 4+ =4,则 1 ml 中 S 原子的价层电子对数
为 ,A 正确;
B.32 gO2 的物质的量为 1 ml,二氧化硫和氧气的反应为: ,该反应为可
逆反应,则足量 SO2 与 32 gO2 充分反应,生成 SO3 的分子数小于 ,B 错误;
第 2页/共 24页
C.黄铁矿与 O2 反应的方程式为:4FeS2+11O2 2Fe2O3+8SO2,该反应转移 44 个电子,则生成 1 mlSO2,
转移电子数为 ,C 错误;
D.三氧化硫,标准状况下三氧化硫固体,无法计算其物质的量,D 错误;
故选 A。
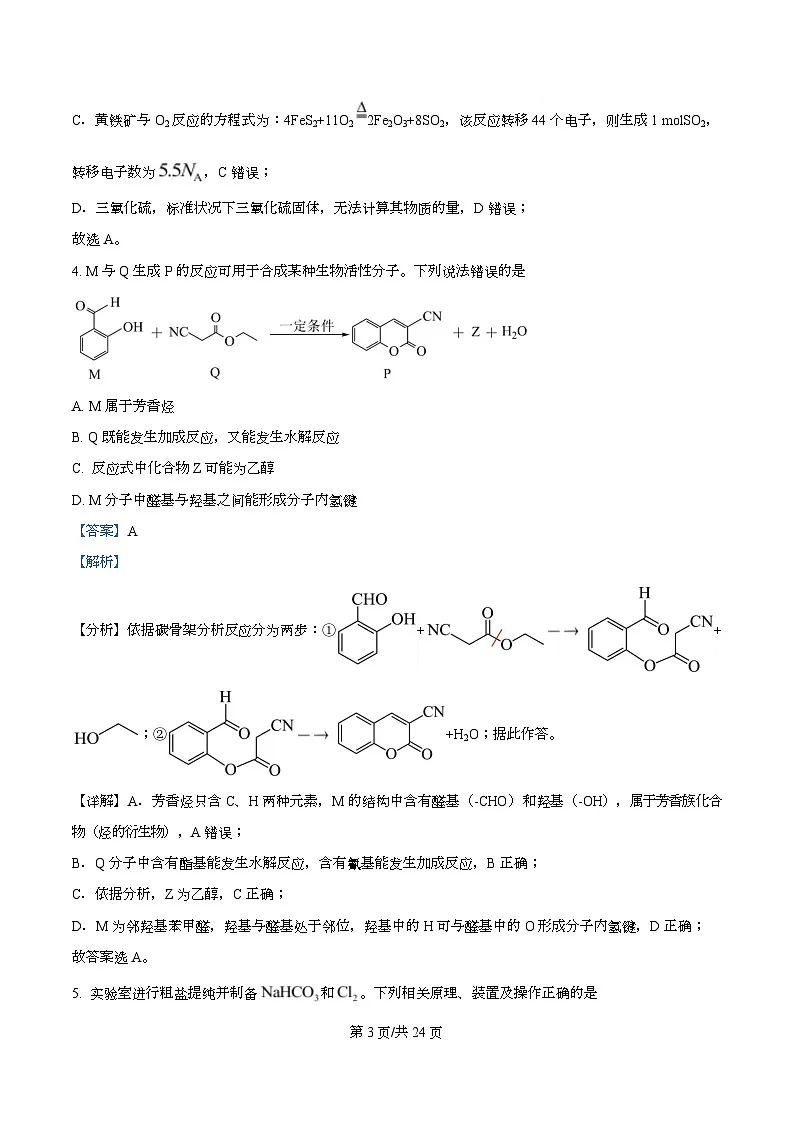
4. M 与 Q 生成 P 的反应可用于合成某种生物活性分子。下列说法错误的是
A. M 属于芳香烃
B. Q 既能发生加成反应,又能发生水解反应
C. 反应式中化合物 Z 可能为乙醇
D. M 分子中醛基与羟基之间能形成分子内氢键
【答案】A
【解析】
【分析】依据碳骨架分析反应分为两步:① + +
;② +H2O;据此作答。
【详解】A.芳香烃只含 C、H 两种元素,M 的结构中含有醛基(-CHO)和羟基(-OH),属于芳香族化合
物(烃的衍生物),A 错误;
B.Q 分子中含有酯基能发生水解反应,含有氰基能发生加成反应,B 正确;
C.依据分析,Z 为乙醇,C 正确;
D.M 为邻羟基苯甲醛,羟基与醛基处于邻位,羟基中的 H 可与醛基中的 O 形成分子内氢键,D 正确;
故答案选 A。
5. 实验室进行粗盐提纯并制备 和 。下列相关原理、装置及操作正确的是
第 3页/共 24页
A. 装置甲除粗盐水中的泥沙 B. 装置乙蒸发 溶液
C. 装置丙制备 D. 装置丁制备
【答案】C
【解析】
【详解】A.过滤需要用玻璃棒引流,A 错误;
B.蒸发 溶液用蒸发皿,B 错误;
C.向氨化的饱和食盐水中通入二氧化碳,生成碳酸氢钠沉淀和氯化铵,C 正确;
D.电解饱和食盐水时,阳极发生氧化反应生成氯气,阳极应该用石墨等惰性电极,D 错误;
故选 C。
6. 制备铁触媒的主要原料三草酸合铁酸钾 可在光照下发生分解:
。 中每
个配体 中两个单键氧向中心 配位,下列说法错误的是
A. 的基态价电子排布图为
B. 中 O 原子的杂化方式为
C. 的中心离子的配位数为 6
D. 分子中 键和 键数目比为 1:1
【答案】A
【解析】
【详解】A.Fe3+的电子排布式为 1s22s22p63s23p63d5,则 Fe3+的基态价电子排布图为
第 4页/共 24页
,故 A 错误;
B. 中 O 原子含有 2 个单键和 2 个孤电子对,故杂化方式为 ,故 B 正确;
C. 中 Fe 提供空轨道,每个配体 中两个单键氧向中心 Fe3+配位,则铁离子的配位数
为 6,故 C 正确;
D.CO2 的结构式为 O=C=O,双键中有 1 个σ键和 1 个π键,所以 CO2 分子中有 2 个σ键和 2 个π键,σ
键和π键的数目比为 1:1,故 D 正确;
故选 A。
7. 下列离子方程式书写正确的是
A. Ca(ClO)2 溶液中通入少量 CO2:2ClO-+CO2+H2O=2HClO+
B. 向 NaHS 溶液中加入过量的 CuSO4 溶液:Cu2++HS-=CuS↓+H+
C. 氯化铁溶液中加入少量 Cu:2Fe3++3Cu=2Fe+3Cu2+
D. 试管壁上的银镜用氨水清洗:Ag+2NH3·H2O=[Ag(NH3)2]++2H2O
【答案】B
【解析】
【详解】A.Ca(ClO)2 溶液中通入少量 CO2 时,ClO-与 CO2 反应生成 HClO 和 ,Ca2+与碳酸根结合为
CaCO3 沉淀,方程式为: ,A 错误;
B.向 NaHS 溶液中加入过量 CuSO4 溶液时,Cu2+与 HS-直接反应生成 CuS 沉淀和 H+,B 正确;
C.Fe3+与 Cu 反应时,Fe3+被还原为 Fe2+而非 Fe 单质,正确反应为 ,C 错误;
D.氨水无法直接溶解银,需氧化剂(如硝酸)参与反应,D 错误;
故选 B。
8. X、Y、Z、W 均为短周期主族元素,Z 与 W 同主族,X、Y、Z 同周期,基态 X 原子的价层电子排布式
为 ,基态 Y 原子 s 能级上的电子总数是 p 能级上电子总数的 2 倍,Z 与 W 原子的质子数之和是 Y
原子序数的 4 倍。下列说法正确的是
A. 电负性: B. W 的单质易溶于
C. 键角: D. 基态 Y、Z 原子核外电子的空间运动状态均有 5 种
第 5页/共 24页
【答案】B
【解析】
【分析】X、Y、Z、W 均为短周期主族元素,Z 与 W 同主族,X、Y、Z 同周期,基态 X 原子的价层电子
排布式为 ,则 n=2,X 为氟;基态 Y 原子 s 能级上的电子总数是 p 能级上电子总数的 2 倍,则 Y
为 6 号元素碳;Z 与 W 原子的质子数之和是 Y 原子序数的 4 倍,设 Z 原子序数为 a,则 a+a+8=4×6,a=8,
Z 为氧、W 为硫。
【详解】A.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,金属性
增强,非金属性逐渐减弱,元素电负性减弱;电负性: ,A 错误;
B.硫单质易溶于 CS2,B 正确;
C.CF4 为正四面体形,键角 109°28',SO3 为平面三角形,键角 120°,C 错误;
D.把电子在原子核外的一个空间运动状态称为一个原子轨道,因而空间运动状态个数等于轨道数;基态 Y
(C)的电子占据 4 个轨道,Z(O)占据 5 个轨道,D 错误;
故选 B。
9. 碱性锌锰电池的总反应为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,电池构造示意图如图所示。下列
有关说法正确的是
A. 工作时 KOH 没有发挥任何作用
B. Zn 发生还原反应,MnO2 发生氧化反应
C. 电池工作时,OH-通过隔膜向正极移动
D. 反应中每生成 1mlMnO(OH),转移电子数约为 6.02×1023
【答案】D
【解析】
【分析】由题干原电池总反应为:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2 可知,Zn 发生氧化反应,则
Zn 作负极,电极反应为:Zn-2e-+2OH-=Zn(OH)2,则 MnO2 一极为正极,电极反应为:MnO2
+e-+H2O=MnO(OH)+OH-,据此分析解题。
【详解】A.KOH 作为电解质,提供碱性环境与负极产生的 Zn2+反应并传导离子,并非无作用,A 错误;
第 6页/共 24页
B.Zn 从 0 价升至+2 价,失电子发生氧化反应;MnO2 中 Mn 从+4 价降至+3 价,得电子发生还原反应,B
错误;
C.电池工作时阴离子(OH⁻)向负极移动,阳离子向正极移动,C 错误;
D.生成 2mlMnO(OH)时,Zn 失去 2ml 电子(转移 2ml 电子),则生成 1mlMnO(OH)转移 1ml 电子,电
子数约为 6.02×1023,D 正确;
故答案为:D。
10. 根据实验操作及现象,下列结论中正确的是
选项 实验操作及现象 结论
常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生 稀硝酸的氧化性比浓硝 A
无色气体,后者无明显现象 酸强
取一定量 Na2SO3 样品,溶解后加入 BaCl2 溶液,产生
B 此样品中含有
白色沉淀,再加入稀 HNO3 酸化,仍有沉淀
将银和 AgNO3 溶液与铜和 Na2SO4 溶液构成双液原电
C 池。连通后银表面有银白色金属沉积,铜电极附近溶 Cu 的金属性比 Ag 强
液逐渐变蓝
D 向溴水中加入苯,振荡后静置,水层颜色变浅 溴与苯发生了加成反应
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.铁和稀硝酸反应生成一氧化氮气体,铁和浓硝酸钝化,导致现象不明显,所以不能通过该实验
现象比较浓硝酸和稀硝酸的氧化性强弱,实际上硝酸的浓度越大氧化性越强,A 错误;
B.亚硫酸钠和氯化钡发生反应,生成亚硫酸钡沉淀,亚硫酸钡与硝酸发生氧化还原反应生成硫酸钡,故不
能证明此样品中含有硫酸根,B 错误;
C.铜、银和 AgNO3 溶液组成原电池,银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝,铜极是负极,
银是正极,Cu 的金属性比 Ag 强,C 正确;
D.向溴水中加入苯,苯萃取了溴水中的溴,振荡后静置,液体分为两层,下层为水,上层为溴的苯溶液,
并非是发生加成反应,D 错误;
第 7页/共 24页
故选 C。
11. 计算机模拟单个乙炔(HC≡CH)分子在 Hg2+催化作用下生成 CH3CHO 的反应历程及相对能量变化如图所
示(已知 ; )。
下列说法错误的是
A. 该反应历程中决速步骤能垒为 0.9eV
B. 历程①中有σ键生成,历程③中有π键断裂
C. 历程⑤中,体系能量下降,是因为断开 键放出能量
D. 该反应的热化学方程式为
【答案】C
【解析】
【详解】A.反应历程中,活化能最大的为决速步,其中历程④的活化能最高,为 0.9eV,A 正确;
B.历程①中有 Hg2+与 H2O 之间形成了配位键,即有σ键生成,历程③中碳碳三键变成碳碳双键,断裂了π
键,B 正确;
C.断键吸热,会使体系能量升高,成键放热,使体系能量下降,历程⑤中,体系能量下降,是因为生成
C=O 等化学键释放的能量大于断开 等键吸收的能量,C 错误;
D.反应的焓变只与始态、终态有关,故反应的热化学方程式为
,D 正确;
故答案选 C。
12. 锆酸锶主要用于玻璃、陶瓷工业,可用碳酸锶 和二氧化锆 在高温下反应制得,同时有
二氧化碳生成。二氧化锆的立方晶胞(图 1)、锆酸锶的立方晶胞(图 2)结构如图所示。设 为阿伏加德罗常
第 8页/共 24页
数的值,下列有关说法正确的是
A. 属于非极性分子,大 键可表示为
B. 图 2 晶胞沿 z 轴方向的投影图为
C. 若 a 点的原子分数坐标为 ,则 b 点的原子分数坐标为
D. 若图 2 晶体的密度为 ,则相邻 O 原子之间的最短距离为
【答案】D
【解析】
【详解】A. 属于非极性分子,大 键可表示为 ,A 项错误;
B.图 2 晶胞沿 轴方向的投影图为 ,B 项错误;
C.b 点的原子分数坐标为 ,C 项错误;
D. 图 2 晶 胞 的 化 学 式 为 , 设 该 晶 胞 参 数 为 , 由 可 得 :
,相邻氧原子之间的最短距离为面对角线的一半,即 ,D 项正确;
故选 D。
13. 以炼铁厂锌灰(主要成分为 ZnO,含少量的 CuO、SiO2、Fe2O3)为原料制备 ZnO 的流程如图所示。下列
说法正确的是
第 9页/共 24页
已知:“浸取”工序中 ZnO、CuO 分别转化为[Zn(NH3)4]2+和[Cu(NH3)4]2+。
A. H-N-H 键角:[Cu(NH3)4]2+”或“ ②. 反应Ⅰ放热,反应Ⅱ吸热,温度升高,温度较低时以反应Ⅰ为主,温度较高时以反
应Ⅱ为主 ③. 0.016
(3) ①. LixSi-xe-=Si+xLi+ ②. 32
【解析】
【小问 1 详解】
= =
【小问 2 详解】
升高温度,CH4 的选择性逐渐减小,说明主反应的平衡逆向移动,则主反应的正反应为放热反应;CO2 的
转化率先减小后增大,说明升高温度,副反应的平衡正向移动, ;
主反应为放热反应、副反应为吸热反应,升高温度,温度较低时以主反应为主,升高温度主反应 平衡逆
向移动,CO2 转化率减小;温度较高时,副反应为主,升高温度,副反应的平衡正向移动,CO2 的转化率
增加;
T℃,CO2 的转化率为 30%,CH4 的选择性为 80%,消耗的 ,生成的
,生成的 ,列三段式:
第 19页/共 24页
平衡时剩余
,剩余 , ,
, ,混合气体总物质的量为
,反应Ⅱ的前后气体计量数之和不变,该反应中生成物压强的
幂之积与反应物压强的幂之积的比等于生成物的物质的量分数幂之积与反应物的物质的量分数幂之积的比,
, , , ,所以反应Ⅱ的 =
。
【小问 3 详解】
由电极总反应式 ,可得放电作原电池,分为正负极,正极发生还
原反应,负极发生氧化反应,则其负极电极反应式为 LixSi-xe-=Si+xLi+;
用该电池电解水为宇航员提供 O2,根据电池反应式 ,正极反应式
为 ,电解水的过程中,生成 1 mlO2 转移 4 ml 电子,可得关系式
,则生成标准状况下 11.2 L(即 0.5 ml)O2,正极质量变化为
。
19. 化合物 L 是一种抗病毒药物,其合成路线如图所示:
第 20页/共 24页
已知: 。
回答下列问题:
(1)I 的化学名称是_____。
(2)B 中官能团名称是_____。
(3)K→L 的反应类型是_____。
(4)D 的结构简式是_____。
(5)E 与 I 生成 J 的化学方程式是_____。
(6)M 是 C 的同分异构体,M 能发生水解反应,酸性条件下的一种水解产物能与 FeCl3 溶液发生显色反应,
则 M 的结构共有_____种,其中不能发生银镜反应且苯环上一氯代物只有两种的结构简式是_____。
【答案】(1)4-氯苯甲醛或对氯苯甲醛
(2)羟基、酮羰基 (3)还原反应
( 4) ( 5)
(6) ①.
第 21页/共 24页
13 ②.
【解析】
【分析】A 的分子式为 C6H6O,结合 B 的结构简式,可知 A 的结构简式为 ;A 与 CH3COCl 发生取
代 反 应 生 成 B, B 与 CH3I 发 生 取 代 反 应 生 成 C, 结 合 C、 E 的 结 构 简 式 , 可 知 D 的 结 构 简 式 为
;D 到 E 又生成羟基,所以 CH3I 的作用是保护酚羟基;E 与 I 生成 J,结合已知可知
J 的结构简式为 ;J 在 PPA 条件下生成 K,K 发生还原反应生成 L;据此作答。
【小问 1 详解】
I 的结构简式为 ,依据有机化合物命名时官能团的优先次序,其化学名称是 4-氯苯甲醛或对氯苯
甲醛,答案为:4-氯苯甲醛或对氯苯甲醛;
【小问 2 详解】
B 的结构简式为 ,则官能团名称为羟基、酮羰基,答案为:羟基、酮羰基;
【小问 3 详解】
依据分析,K→L 的反应类型是还原反应,答案为:还原反应;
【小问 4 详解】
第 22页/共 24页
依据分析 D 的结构简式为 ,答案为: ;
【小问 5 详解】
依据分析,结合已知和 J 的分子式推测 E 与 I 生成 J 的化学方程式是:
,答案为:
;
【小问 6 详解】
M 是 的同分异构体,能发生水解反应(有酯基),其中酸性条件下的一种水解产物能与
FeCl3 溶液发生显色反应(含有酚羟基),则满足条件的 M 的结构:
① ,共 6 种;② ,共 3 种;③ ,共 3 种;④
,共 1 种;所以共有 13 种;其中不能发生银镜(无醛基)反应且苯环上一氯代物只有两
第 23页/共 24页
种(对位取代)的结构简式为: ;故答案为:13; 。
第 24页/共 24页
相关试卷
这是一份四川省遂宁市射洪中学校2026届高三上学期期中考试(强基班)化学试卷(含答案),共1页。
这是一份四川省遂宁市射洪中学2026届高三上学期期中考试化学试卷(Word版附答案),文件包含化学试题doc、化学答案doc等2份试卷配套教学资源,其中试卷共9页, 欢迎下载使用。
这是一份四川省遂宁市射洪中学2026届高三上学期9月第一次高考模拟考试 化学试卷,共9页。试卷主要包含了02×1023,9eV,424KJ/ml等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)




