

湖北省十堰市八校教联体联考2025-2026学年高二上学期9月月考化学试题(学生版)
展开 这是一份湖北省十堰市八校教联体联考2025-2026学年高二上学期9月月考化学试题(学生版),共10页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
可能用到的相对原子质量:H-1 N-14 O-16 Na-23 S-32
一、单选题(每小题只有一个正确答案,每题3分,共15小题)
1. 2024年6月3号,嫦娥六号在月球背面上展示的国旗是我国科研人员利用玄武岩熔融拉丝技术制作而成的。玄武岩石料由二氧化硅、氧化铝、氧化钙、氧化镁、氧化铁和二氧化钛等氧化物组成。下列说法中错误的是
A. 硅酸盐中,Si和O构成了硅氧四面体结构
B. 玄武岩纤维具有耐腐蚀、耐高温、耐低温的优异性能
C. 由,说明硅酸的酸性比碳酸强
D. 玄武岩纤维是一种无机非金属材料
2. 化学应用体现在生活的方方面面,下列用法不合理的是
A. 用明矾净化黄河水B. 用漂白粉漂白蚕丝制品
C. 用食醋去除水壶中水垢D. 用小苏打作烘焙糕点膨松剂
3. 少量纯铁片与100mL0.1ml/L的足量稀盐酸反应,反应速率太慢。为了加快此反应的速率而又不改变H2产量,下列方法不可行的是
A. 改用等质量的生铁片B. 滴加少量浓硫酸
C. 改用20mL1.0ml/L的盐酸D. 将铁片改为等质量的铁粉
4. “舌尖上的美食”闻名天下,十堰各县市美食也各具特色。下列有关十堰各县市美食的化学解读正确的是
A. AB. BC. CD. D
5. 设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 质量为46gNO2和N2O4的混合物中含有氧原子的数目为4NA
B. 标准状况下,2.24L乙烷分子中所含非极性共价键数为0.1NA
C. 1L0.1ml/L乙酸溶液中H+数为0.1NA
D. 一定条件下,0.2mlSO2与0.1mlO2混合后充分反应,转移的电子数目为0.4NA
6. 怀山药是河南省焦作市的特产。山药含有薯蓣皂甙、多巴胺、盐酸山药甙、多种氨基酸等成分,其中多巴胺的结构如图所示(由C、H、O、N元素组成)。
下列有关多巴胺的说法正确的是
A. 图示为多巴胺的空间填充模型B. 不能发生氧化反应
C. 分子式是C8H11NO2D. 所有原子共平面
7. 工业上制备纯硅反应的热化学方程式如下:
某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
A. 反应过程中,若增大压强能提高的平衡转化率
B. 当吸收热量时,生成的通入含的溶液中恰好反应
C. 反应至4min时,若浓度为,则的反应速率为
D. 若反应开始时为、为,则达到平衡时,吸收热量为
8. 对于化学反应能否自发,下列有关说法正确的是
A. 一定温度下,反应能自发进行,该反应的
B. 反应可用于纯硅的制备,该反应、
C. 反应常温下可自发进行,该反应为吸热反应
D. 反应的,
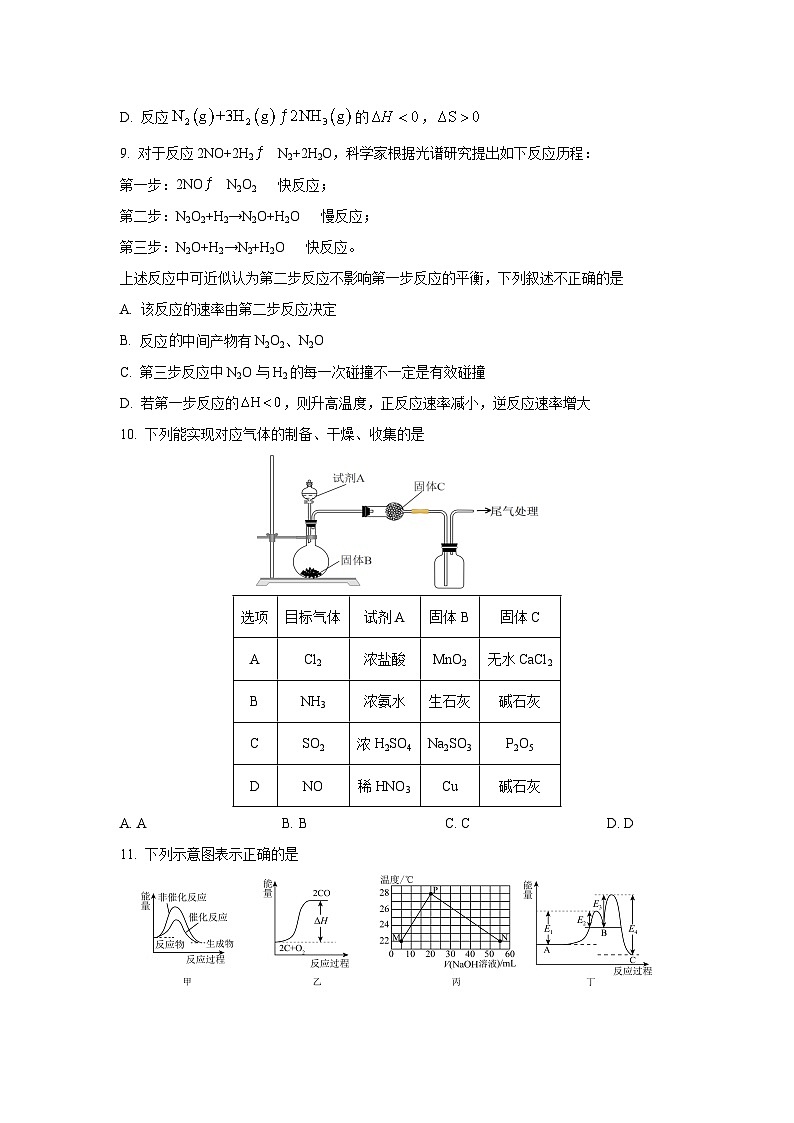
9. 对于反应2NO+2H2N2+2H2O,科学家根据光谱研究提出如下反应历程:
第一步:2NON2O2 快反应;
第二步:N2O2+H2→N2O+H2O 慢反应;
第三步:N2O+H2→N2+H2O 快反应。
上述反应中可近似认为第二步反应不影响第一步反应的平衡,下列叙述不正确的是
A. 该反应的速率由第二步反应决定
B. 反应中间产物有N2O2、N2O
C. 第三步反应中N2O与H2的每一次碰撞不一定是有效碰撞
D. 若第一步反应的,则升高温度,正反应速率减小,逆反应速率增大
10. 下列能实现对应气体的制备、干燥、收集的是
A. AB. BC. CD. D
11. 下列示意图表示正确的是
A. 甲图表示 的能量变化
B. 乙图表示碳完全燃烧的反应中能量的变化
C. 实验的环境温度为20℃,将物质的量浓度相等、体积分别为、的溶液、NaOH溶液混合,测量混合液温度,结果如丙图(已知)
D. 由丁图可知A生成B反应为吸热反应,B生成C的反应为放热反应
12. 某小组为了探究影响溶液与溶液在酸性条件下反应速率的因素,设计如表所示的实验方案。
下列说法不正确的是
A. ,
B. 实验1和2的对照说明溶液的酸碱性会影响该反应的速率
C. 实验1和4的对照说明能加快该反应的速率,是该反应的催化剂
D. 根据实验1的数据计算反应速率
13. 下列有关说法正确的是
A. 已知,,则a>b
B. 、下,将和置于密闭容器中反应生成,放热,其热化学方程式为N2(g)+3H2(g)⇌2NH3(g)ΔH=-38.6kJ•ml-1
C. 和反应中和热,则:
D. 已知,则白磷比红磷稳定
14. 下列叙述与图对应的是
A. 对于达到平衡状态的反应:N2(g)+3H2(g)2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动
B. 由图②可知,P2>P1、T1>T2,满足反应:2A(g)+B(g) 2C(g)ΔH<0
C. 图③表示的反应方程式为:2A=3B+C
D. 对于反应2X(g)+3Y(g) 3Z(g)ΔH<0,图④y轴可以表示Y的百分含量
15. 热化学离不开实验,更离不开对反应热的研究。下列有关说法正确的是
A. 向图1的试管A中加入某一固体和液体,若注射器的活塞右移,说明A中发生了放热反应
B. 将图1虚框中的装置换为图2装置,若注射器的活塞右移,说明锌粒和稀硫酸的反应为放热反应
C. 由图3可知,反应①的小于反应②的
D. 由图3可知,
二、填空题(四个大题,共55分)
16. 亚硝酸钠常用作食品防腐剂,实验室常用和反应制得。已知:是白色粉末,易溶于水。
回答下列问题:
(1)装浓硝酸的仪器名称是___________。滴入浓硝酸前先通入一段时间的,目的是___________。
(2)B装置中发生反应的化学方程式为___________、___________。
(3)C装置中试剂是___________(填名称)。
(4)观察到装置中溶液由紫红色变为无色,经检验氧化产物是,还原产物是。写出F装置中发生反应的离子方程式:___________。
(5)人体正常的血红蛋白中含,若误食,会导致血红蛋白中转化为而中毒,服用维生素可解毒。在中毒和解毒过程中,下列说法错误的是___________(填字母)。
A. 是还原剂B. 维生素C是还原剂
C. 维生素将还原为D. 被还原
(6)测定样品纯度。取样品溶于水,配制成溶液,量取所配溶液于锥形瓶中,加入适量稀硫酸,用酸性溶液滴定至恰好完全反应(杂质不参与反应),消耗酸性溶液样品纯度为___________%。
17. 某实验小组用溶液和溶液进行中和热的测定。测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示:
(1)配制硫酸溶液:实验至少要用到稀硫酸溶液,则需要量取12.5的浓硫酸___________。
(2)溶液与稀硫酸的反应热测定装置如图所示:
①仪器A的名称___________;
②仪器A的操作方式___________(填字母);
A.上下移动 B.左右移动 C.上下左右同时移动
③向装置中倒入NaOH溶液的正确操作是___________。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)纳米级由于具有优良的催化性能而受到关注。已知:
;
;
。
则工业上用炭粉在高温条件下还原制取和CO的热化学方程式为___________。
(4)和反应生成的过程中能量变化如图所示,写出该反应中每消耗时的热化学方程式:___________。
(5)通常把拆开某化学键吸收能量看做是该化学键的键能。下表是常见的键能数据:
写出的热化学方程式:___________。
18. T℃时,在恒容密闭容器中发生水煤气反应: 。
回答下列问题:
(1)若开始时充入、,达到平衡时放出热量。该温度下反应的平衡常数是________,的平衡转化率是________。
(2)若保持温度不变,开始时充入、、、,开始时化学反应速率________(填“大于”“小于”或“等于”),理由是________。
(3)在恒温恒容密闭容器中发生反应:,物质的浓度随时间的变化如图所示:
时改变的条件是________(填字母)。
A. 加压B. 增大反应物浓度
C. 升高温度D. 减小产物浓度
(4)恒温恒容条件下,以投料,开始时的压强是,达到平衡时的分压是,则此时的分压是________;达到平衡后将体积压缩为原来的一半,温度不变,体系的压强是________。
19. 我国科学家成功用二氧化碳人工合成淀粉,其中第一步是利用二氧化碳催化加氢制甲醇。
(1)在标准状态下,由最稳定的单质生成单位物质的量的某纯物质的焓变称为该物质的标准摩尔生成焓。几种物质的标准摩尔生成焓如下:
①由表中数据推测,的___________(填“>”“
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





