

福建省福州市第十六中学2024-2025学年九年级下学期开学考试化学试题(原卷版+解析版)
展开 这是一份福建省福州市第十六中学2024-2025学年九年级下学期开学考试化学试题(原卷版+解析版),共24页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
满分:100分 完卷时间:60分钟
相对原子质量H 1 C 12 O 16 Na 23 Mg 24 S 32 Fe 56 Zn 65
一、选择题(每小题3分,共30分)
1. 清明放风筝。下列与风筝制作、放飞相关部件中,用到金属材料的是
A. 竹质骨架B. 纸质风筝面C. 棉质捆扎线D. 不锈钢手握轮
2. 粽叶中的异荭草苷具有抗菌等作用。下列关于异荭草昔的说法错误的是
A 属于有机物B. 属于化合物C. 属于氧化物D. 属于纯净物
3. 下列生活中的物质,其主要成分属于金属单质的是
A. 钻戒——金刚石B. 体温计填充液-汞
C. 装饰材料——大理石D. 餐具——陶瓷
4. 越王勾践青铜剑,其主要成分为铜锡合金。下列有关铜锡合金说法错误的是
A. 属于混合物B. 熔点低于纯铜C. 硬度高于纯锡D. 铜能与稀硫酸反应
5. 下列物质通过金属与稀硫酸反应能直接得到的是
A. B. C. D.
6. 铁和铜在自然环境中都能被腐蚀。下列不能说明铁比铜活泼的事实是
A. 历史上铜比铁使用更早B. 铁的文物比铜的稀有
C. 铁的密度比铜的密度小D. 铁能与硫酸铜溶液反应
7. 下列根据实验证据进行的推理,正确的是
A. 铝的金属活动性比铁强,推测铝的抗腐蚀性能比铁差
B. 电解烧杯中水,两电极均产生气泡,推测水的化学式为
C. 在火焰上方罩干冷烧杯,内壁出现水雾,推测该可燃物含氢元素
D. 将带火星的木条伸入盛有的集气瓶中,木条复燃,可推测具有可燃性
8. 为证明Fe、Cu、Ag三种金属的活动性强弱,下列实验方案能达到目的的是
A. 将Fe、Cu、Ag分别放入稀盐酸中
B. 将Cu分别放入FeCl2、AgNO3溶液中
C. 将Cu、Ag分别放入FeSO4溶液中
D. 将Fe放入稀盐酸、Cu放入AgNO3溶液中
9. 我国商代时就已经发现,贮存于铅罐的酒(含乙醇)会发酵成醋(含醋酸,醋酸的化学性质与盐酸相似),铅与醋反应生成铅霜,铅霜在空气中转化为浮粉(PbCO3),加热浮粉得铅白(PbO)固体,铅白可用作白色颜料。下列说法错误的是
A. 酒能变醋体现乙醇的化学性质B. 铅能与醋酸反应产生氢气
C. 浮粉中铅元素的化合价为+2价D. 浮粉变铅白,固体质量增大
10. 在密闭容器中分别放入打磨过的等质量的镁片、铁片、锌片和等体积、等浓度的足量稀硫酸,用压强传感器测得容器内气体压强与反应时间的变化曲线如图所示。下列有关说法不正确的是
A. 三种金属消耗硫酸的质量:
B. 三种金属的活动性:
C. 三种金属最终产生气体的质量:
D. 该实验中放热现象的明显程度:
二、非选择题(共70分)
11. “福建舰”解缆启航,标志着我国航空母舰建设迈向新征程。
(1)航母建造需使用纯铜、钢铁、钛合金等。
①航母电缆用纯铜制作,主要利用铜的导电性和_______性。
②铁元素在元素周期表中的部分信息和铁原子的结构示意图如图所示。x和y的值分别为_______和_______。
③钛合金放在海水中数年仍光亮如初,说明其具有的优良性能是_______。
(2)航母动力由重油(含等多种成分)燃烧提供。在充足的氧气中完全燃烧的化学方程式为_______。
(3)食物和淡水是重要的生活保障。
①供给食物包含牛奶和青菜,其中主要为人体提供蛋白质的食品是_______。
②部分淡水可通过减小压强使水沸点_______(填“升高”或“降低”),进而使水汽化、冷凝而获得。
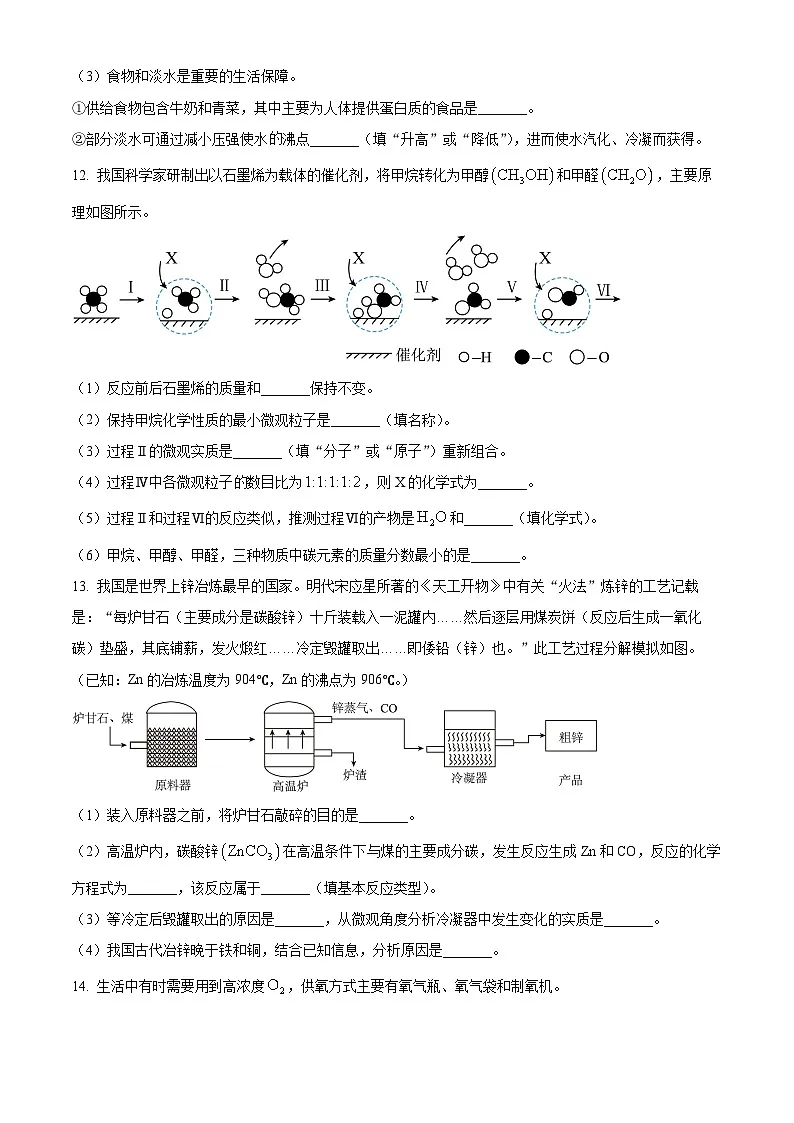
12. 我国科学家研制出以石墨烯为载体的催化剂,将甲烷转化为甲醇和甲醛,主要原理如图所示。
(1)反应前后石墨烯的质量和_______保持不变。
(2)保持甲烷化学性质的最小微观粒子是_______(填名称)。
(3)过程Ⅱ的微观实质是_______(填“分子”或“原子”)重新组合。
(4)过程Ⅳ中各微观粒子数目比为,则X的化学式为_______。
(5)过程Ⅱ和过程Ⅵ的反应类似,推测过程Ⅵ的产物是和_______(填化学式)。
(6)甲烷、甲醇、甲醛,三种物质中碳元素的质量分数最小的是_______。
13. 我国是世界上锌冶炼最早的国家。明代宋应星所著的《天工开物》中有关“火法”炼锌的工艺记载是:“每炉甘石(主要成分是碳酸锌)十斤装载入一泥罐内……然后逐层用煤炭饼(反应后生成一氧化碳)垫盛,其底铺薪,发火煅红……冷定毁罐取出……即倭铅(锌)也。”此工艺过程分解模拟如图。(已知:Zn的冶炼温度为904℃,Zn的沸点为906℃。)
(1)装入原料器之前,将炉甘石敲碎的目的是_______。
(2)高温炉内,碳酸锌在高温条件下与煤的主要成分碳,发生反应生成Zn和CO,反应的化学方程式为_______,该反应属于_______(填基本反应类型)。
(3)等冷定后毁罐取出的原因是_______,从微观角度分析冷凝器中发生变化的实质是_______。
(4)我国古代冶锌晚于铁和铜,结合已知信息,分析原因是_______。
14. 生活中有时需要用到高浓度,供氧方式主要有氧气瓶、氧气袋和制氧机。
氧气瓶和氧气袋中的一般用深冷法制得,该方法利用物质的沸点差异,从空气中分离出。制氧机有膜分离、变压吸附等制氧方式。膜分离制氧用到的膜材料有陶瓷、聚苯胺等,其中混合导电陶瓷分离膜的工作原理示意如图1.变压吸附制氧常用的吸附剂是沸石分子筛。科研人员在一定条件下分别将通过某种沸石分子筛,测定其对的吸附情况、结果如图2(纵坐标数值越大,代表吸附量越大)。吸氧对于缺氧人群有一定作用,但健康人短期内高流量吸氧会对机体造成不良影响,因此不能盲目吸氧。
(1)深冷法制氧利用了物质的_______(填“物理性质”或“化学性质”)差异。
(2)图1中,表示氧分子变成氧原子的是_______(填“Ⅰ”“Ⅱ”或“Ⅲ”)。
(3)由图2可知,25℃时吸附压越大越有利于分离和,证据是_______。
(4)健康人_______(填“能”或“不能”)盲目吸氧。
(5)探究某制氧机中药品用量和温度对反应速率的影响,实验数据如下表:
①制氧原理:第一步:;第二步:在二氧化锰催化下生成氧气。
写出第二步反应的化学方程式:_______。
②上表中a=_______。
③反思上述实验,再提出一个影响产氧速率的因素进一步探究。你的实验方案是_______。
15. 探秘古钱币。
(1)古币金属知多少。我国古代的钱币有多种,如金币、银铜币、铁币等。银铜币多为银白色,金币的颜色是_______。
(2)金属性质共探究。小郑同学做了下列实验:
①如图1,铜片加热时观察到的现象是_______(填标号)。
A.发光放热 B.产生黑色固体 C.生成氧化铜CuO
②如图2,三支试管里的液体均为稀硫酸,铁丝表面有气泡冒出,银丝和铜丝无明显变化。有气泡冒出的反应化学方程式为_______。
(3)货币流通有原因。铁硬度比铜大,密度比铜小,金和银做成的钱币比铜币腐蚀速度要慢得多,似乎更适合铸造钱币,但是中国历史上铜币的使用量远大于其它材质的货币。综上所述,古代铸造钱币选择金属考虑的一个因素是:_______。
16. 兴趣小组开展了与钢铁相关的探究活动。
Ⅰ.模拟炼铁(实验装置如右图所示)。
(1)玻璃管中发生的化学反应方程式为_______。
(2)为检验尾气中含有二氧化碳,乙装置中的试剂X是_______(填名称)。
(3)图丙装置的作用是_______。
Ⅱ.探究:加热一段时间后玻璃管中生成的黑色固体是什么?
【查阅资料】①CO与反应的固体生成物与温度的关系如下表:
②FeO为一种黑色固体,和Fe都能被磁铁吸引,和FeO不能被磁铁吸引。
③溶液不与铁的氧化物反应。
【作出猜想】
猜想Ⅰ:固体成分为Fe猜想Ⅱ:固体成分为 猜想Ⅲ:固体成分为FeO
【实验探究】
(4)完成下列实验报告
(5)步骤②中的化学方程式为_______。
(6)工业上冶炼铁的过程中,为了提高铁的产率,温度应不低于_______℃。
【拓展】
(7)1.0g某钢样在纯氧中完全燃烧,得到0.011g二氧化碳,则此钢样中碳的质量分数为_______。
17. 某化学兴趣小组利用以下实验装置探究铁生锈的条件。
【提出问题】铁生锈的条件是什么?
【设计实验】取3根无锈的铁丝设计如下图所示的三个实验。
【实验现象】
(1)实验Ⅰ中铁丝生锈,当铁丝足量,时间足够长,打开止水夹后,还能观察到的现象是_______。
【实验结论】
(2)对比实验_______(填序号),可以得出铁生锈需要水;得出“铁生锈需要与氧气接触”这一结论所依据的现象是_______。
【拓展与延伸】海边铁制渔船上的锈迹比江边铁制渔船的多,学生提出问题:海水会加快铁的生锈吗?为验证这一问题,设计以下数字化实验:
(3)①实验2的实验药品是_______。
②根据图像1,说明铁生锈会_______(选填“吸收”或“放出”)热量。
③根据图像2,可以得出结论是_______。
(4)①生活中使用铁制品时需注意的问题是_______。
②因生锈而废弃的铁制品,应如何处理:_______。
18. 曾作为照相中的显影剂,可由制得.取足量的溶液,加入固体,两者恰好完全反应。(的相对分子质量为104)
试计算:
(1)中硫元素与氧元素的质量比为_______。
(2)消耗的质量(根据化学方程式计算)。
2024-2025学年下学期福州第十六中学教育集团九年级开学练习
(化学学科)
满分:100分 完卷时间:60分钟
相对原子质量H 1 C 12 O 16 Na 23 Mg 24 S 32 Fe 56 Zn 65
一、选择题(每小题3分,共30分)
1. 清明放风筝。下列与风筝制作、放飞相关的部件中,用到金属材料的是
A. 竹质骨架B. 纸质风筝面C. 棉质捆扎线D. 不锈钢手握轮
【答案】D
【解析】
【分析】金属材料包括纯金属与合金
【详解】A、竹质骨架不含金属,不属于金属材料,A选项错误;
B、纸质风筝面不含金属,不属于金属材料,B选项错误;
C、棉质捆扎线不含金属,不属于金属材料,C选项错误;
D、不锈钢属于金属材料,D选项正确。
故选:D。
2. 粽叶中的异荭草苷具有抗菌等作用。下列关于异荭草昔的说法错误的是
A. 属于有机物B. 属于化合物C. 属于氧化物D. 属于纯净物
【答案】C
【解析】
【详解】A、异荭草苷是含有碳元素的化合物,属于有机物,说法正确,不符合题意;
B、异荭草苷是由碳、氢、氧三种元素组成的纯净物,属于化合物,说法正确,不符合题意;
C、氧化物是由两种元素组成且其中一种元素为氧元素的化合物,异荭草苷是由碳、氢、氧三种元素组成的纯净物,属于化合物,不属于氧化物,说法错误,符合题意;
D、异荭草苷只由一种物质组成,属于纯净物,说法正确,不符合题意。
故选:C。
3. 下列生活中的物质,其主要成分属于金属单质的是
A. 钻戒——金刚石B. 体温计填充液-汞
C. 装饰材料——大理石D. 餐具——陶瓷
【答案】B
【解析】
【详解】A、金刚石是由碳元素组成的纯净物,属于非金属单质,不符合题意;
B、汞是由汞元素组成的纯净物,属于金属单质,符合题意;
C、大理石主要成分是碳酸钙,属于混合物,不符合题意;
D、陶瓷属于无机非金属材料,不符合题意。
故选:B。
4. 越王勾践青铜剑,其主要成分为铜锡合金。下列有关铜锡合金说法错误的是
A. 属于混合物B. 熔点低于纯铜C. 硬度高于纯锡D. 铜能与稀硫酸反应
【答案】D
【解析】
【详解】A、铜锡合金中含有铜、锡等多种物质,属于混合物,说法正确,不符合题意;
B、一般情况下,合金的熔点比组成它的纯金属的熔点低,则铜锡合金的熔点低于纯铜,说法正确,不符合题意;
C、一般情况下,合金的硬度比组成它的纯金属的硬度大,则铜锡合金的硬度高于纯锡,说法正确,不符合题意;
D、根据金属活动性,铜与稀硫酸不反应,说法错误,符合题意。
故选:D。
5. 下列物质通过金属与稀硫酸反应能直接得到的是
A. B. C. D.
【答案】D
【解析】
【详解】A、银与稀硫酸不反应,不能直接得到,不符合题意;
B、铝与稀硫酸反应生成氢气和硫酸铝,不能直接得到,不符合题意;
C、铁与稀硫酸反应生成氢气和硫酸亚铁,不能直接得到,不符合题意;
D、铝与稀硫酸反应生成氢气和硫酸铝,能直接得到,符合题意。
故选:D。
6. 铁和铜在自然环境中都能被腐蚀。下列不能说明铁比铜活泼的事实是
A. 历史上铜比铁使用更早B. 铁的文物比铜的稀有
C. 铁的密度比铜的密度小D. 铁能与硫酸铜溶液反应
【答案】C
【解析】
【详解】A、金属的活动性越强,冶炼越困难,历史上铜比铁使用更早,能说明铁比铜活泼,故不符合题意;
B、铁的文物比铜的稀有,是因为铁比铜活泼,容易锈蚀,故不符合题意;
C、铁的密度比铜的密度小,不能说明铁比铜活泼,故符合题意;
D、铁能与硫酸铜溶液反应,说明铁比铜活泼,故不符合题意;
故选:C。
7. 下列根据实验证据进行的推理,正确的是
A. 铝的金属活动性比铁强,推测铝的抗腐蚀性能比铁差
B. 电解烧杯中的水,两电极均产生气泡,推测水的化学式为
C. 在火焰上方罩干冷烧杯,内壁出现水雾,推测该可燃物含氢元素
D. 将带火星的木条伸入盛有的集气瓶中,木条复燃,可推测具有可燃性
【答案】C
【解析】
【详解】A、铝的金属活动性比铁强,但铝的抗腐蚀性能比铁好,是因为铝在常温下能与空气中的氧气反应生成一层致密的氧化铝薄膜,能阻止内部铝进一步被氧化,故选项说法错误;
B、电解烧杯中的水,两电极均产生气泡,在未验证两个气体生成物的情况下,无法推测水的组成元素和化学式,故选项说法错误;
C、在火焰上方罩干冷烧杯,内壁出现水雾,说明该可燃物燃烧生成水,根据质量守恒定律,化学反应前后元素种类不变,生成物水中含有氢元素和氧元素,反应物氧气中含有氧元素,由此可推测该可燃物含氢元素,故选项说法正确;
D、将带火星的木条伸入盛有的集气瓶中,木条复燃,可推测氧气具有助燃性,故选项说法错误。
故选:C。
8. 为证明Fe、Cu、Ag三种金属的活动性强弱,下列实验方案能达到目的的是
A. 将Fe、Cu、Ag分别放入稀盐酸中
B. 将Cu分别放入FeCl2、AgNO3溶液中
C. 将Cu、Ag分别放入FeSO4溶液中
D. 将Fe放入稀盐酸、Cu放入AgNO3溶液中
【答案】B
【解析】
【详解】A、将Fe、Cu、Ag分别放入稀盐酸中,只有铁与稀盐酸反应生成气体产生气泡,而铜、银都不与稀盐酸反应,只能够证明铁的金属活动性比铜、银强,但不能验证铜、银活动性的关系,选项错误;
B、将Cu分别放入FeCl2、AgNO3溶液中,铜不与氯化亚铁反应,证明铜的活动性比铁弱,铜能够与硝酸银反应生成银和硝酸铜,证明铜的活动性比银强,选项正确;
C、将Cu、Ag分别放入FeSO4溶液中,铜、银都不与硫酸亚铁反应,证明铜、银的活动性都比铁弱,但不能验证铜、银活动性的关系,选项错误;
D、将Fe放入稀盐酸,铁与稀盐酸反应生成氢气产生气泡,证明铁位于金属活动性顺序表中氢的前面,Cu放入AgNO3溶液中反应生成硝酸铜和银,证明铜的活动性比银强,但不能验证铁与铜的活动性的关系,选项错误,故选B。
9. 我国商代时就已经发现,贮存于铅罐的酒(含乙醇)会发酵成醋(含醋酸,醋酸的化学性质与盐酸相似),铅与醋反应生成铅霜,铅霜在空气中转化为浮粉(PbCO3),加热浮粉得铅白(PbO)固体,铅白可用作白色颜料。下列说法错误的是
A. 酒能变醋体现乙醇的化学性质B. 铅能与醋酸反应产生氢气
C. 浮粉中铅元素的化合价为+2价D. 浮粉变铅白,固体质量增大
【答案】D
【解析】
【详解】A、酒能变醋,有新物质生成,属于化学变化,需要通过化学变化才能表现出来,体现乙醇的化学性质,故A说法正确;
B、铅属于氢前金属,铅能与醋酸反应产生氢气,故B说法正确;
C、浮粉的化学式为PbCO3,其中碳酸根显-2价,根据在化合物中正负化合价代数和为0,则铅元素的化合价为+2价,故C说法正确;
D、加热浮粉(PbCO3)得铅白(PbO)固体,浮粉变铅白,固体质量减小,故D说法错误;
故选:D。
10. 在密闭容器中分别放入打磨过的等质量的镁片、铁片、锌片和等体积、等浓度的足量稀硫酸,用压强传感器测得容器内气体压强与反应时间的变化曲线如图所示。下列有关说法不正确的是
A. 三种金属消耗硫酸的质量:
B. 三种金属的活动性:
C. 三种金属最终产生气体的质量:
D. 该实验中放热现象的明显程度:
【答案】A
【解析】
【详解】A、最终容器内气体压强由大到小的顺序是Mg>Fe>Zn,说明最终生成氢气的质量由大到小的顺序是Mg>Fe>Zn,金属与酸反应时产生的氢气来源于酸中的氢元素,则三种金属消耗硫酸的质量为Mg>Fe>Zn,故选项说法错误;
B、金属越活泼,反应速率越快,至完全反应所需的时间越短,由图中信息可知,至完全反应所需的时间Mg<Zn<Fe,则三种金属的活动性为Mg>Zn>Fe,故选项说法正确;
C、最终容器内气体压强由大到小的顺序是Mg>Fe>Zn,说明最终生成氢气的质量由大到小的顺序是Mg>Fe>Zn,故选项说法正确;
D、金属越活泼,反应速率越快,至完全反应所需的时间越短,由图中信息可知,至完全反应所需的时间Mg<Zn<Fe,则三种金属的活动性为Mg>Zn>Fe,根据金属越活泼,单位时间内放热越多,则该实验中放热现象的明显程度为Mg>Zn>Fe,故选项说法正确;
故选:A。
二、非选择题(共70分)
11. “福建舰”解缆启航,标志着我国航空母舰建设迈向新征程。
(1)航母建造需使用纯铜、钢铁、钛合金等。
①航母电缆用纯铜制作,主要利用铜的导电性和_______性。
②铁元素在元素周期表中的部分信息和铁原子的结构示意图如图所示。x和y的值分别为_______和_______。
③钛合金放在海水中数年仍光亮如初,说明其具有的优良性能是_______。
(2)航母动力由重油(含等多种成分)燃烧提供。在充足的氧气中完全燃烧的化学方程式为_______。
(3)食物和淡水是重要的生活保障。
①供给食物包含牛奶和青菜,其中主要为人体提供蛋白质的食品是_______。
②部分淡水可通过减小压强使水的沸点_______(填“升高”或“降低”),进而使水汽化、冷凝而获得。
【答案】(1) ①. 延展 ②. 26 ③. 14 ④. 耐腐蚀(合理即可)
(2)
(3) ①. 牛奶 ②. 降低
【解析】
小问1详解】
①航母电缆用纯铜制作,主要利用铜的导电性和延展性;
②根据铁元素在元素周期表中的部分信息可知,左上角的数字表示原子序数,根据铁原子结构示意图可知,圆圈内的数字表示质子数,则铁原子质子数=26,在原子中,在原子中,原子序数=质子数=核外电子数,则x=26=2+8+y+2,解得y=14;
③钛合金放在海水中数年仍光亮如初,说明钛合金的抗腐蚀性强;
【小问2详解】
在充足的氧气中完全燃烧的生成二氧化碳和水,化学方程式为;
【小问3详解】
①牛奶中富含蛋白质,青菜中富含维生素
②水的沸点与压强大小成正比,即压强增大,水的沸点也升高,压强降低,水的沸点降低,部分淡水可通过减小压强使水的沸点降低,进而使水汽化、冷凝而获得。
12. 我国科学家研制出以石墨烯为载体的催化剂,将甲烷转化为甲醇和甲醛,主要原理如图所示。
(1)反应前后石墨烯质量和_______保持不变。
(2)保持甲烷化学性质的最小微观粒子是_______(填名称)。
(3)过程Ⅱ的微观实质是_______(填“分子”或“原子”)重新组合。
(4)过程Ⅳ中各微观粒子的数目比为,则X的化学式为_______。
(5)过程Ⅱ和过程Ⅵ的反应类似,推测过程Ⅵ的产物是和_______(填化学式)。
(6)甲烷、甲醇、甲醛,三种物质中碳元素的质量分数最小的是_______。
【答案】(1)化学性质
(2)甲烷分子 (3)原子
(4)H2O2 (5)CHOOH
(6)甲醇
【解析】
【小问1详解】
石墨烯在反应中作催化剂,反应前后质量和化学性质不变;
【小问2详解】
甲烷是由甲烷分子构成的,保持甲烷化学性质的最小微观粒子是甲烷分子;
【小问3详解】
化学变化的实质是分子再分,原子进行重新组合;
【小问4详解】
过程Ⅳ中各粒子数目比为1:1:1:1:2,反应的化学方程式为:,根据质量守恒定律,化学反应前后原子的种类和数目均不变,反应前有1个C、4个H、1个O,反应后有1个C、6个H、3个O,则1个X分子中含有2个氢原子和2个氧原子,其化学式为H2O2;
【小问5详解】
从微观示意图看出,过程II的化学方程式是:;过程II和过程VI的反应类似,过程II的产物是CHOOH 和H2O;
【小问6详解】
甲烷中碳元素的质量分数为:,甲醇中碳元素的质量分数为:甲醛中碳元素的质量分数为:,三种物质中碳元素的质量分数最小的是甲醇。
13. 我国是世界上锌冶炼最早的国家。明代宋应星所著的《天工开物》中有关“火法”炼锌的工艺记载是:“每炉甘石(主要成分是碳酸锌)十斤装载入一泥罐内……然后逐层用煤炭饼(反应后生成一氧化碳)垫盛,其底铺薪,发火煅红……冷定毁罐取出……即倭铅(锌)也。”此工艺过程分解模拟如图。(已知:Zn的冶炼温度为904℃,Zn的沸点为906℃。)
(1)装入原料器之前,将炉甘石敲碎的目的是_______。
(2)高温炉内,碳酸锌在高温条件下与煤的主要成分碳,发生反应生成Zn和CO,反应的化学方程式为_______,该反应属于_______(填基本反应类型)。
(3)等冷定后毁罐取出的原因是_______,从微观角度分析冷凝器中发生变化的实质是_______。
(4)我国古代冶锌晚于铁和铜,结合已知信息,分析原因是_______。
【答案】(1)增大反应物接触面积,使反应更快、更充分
(2) ①. ②. 置换反应
(3) ①. 防止热的锌在空气中在被氧化 ②. 锌原子之间的间隔变小
(4)锌的金属活动性比铁、铜强,易被空气中的氧气氧化(合理即可)
【解析】
【小问1详解】
装入原料器之前,将炉甘石粉碎,能增大反应物的接触面积,使反应更快、更充分;
【小问2详解】
高温炉内,碳酸锌在高温条件下与煤的主要成分碳,发生反应生成Zn和CO,反应的化学方程式为;该反应是一种单质和一种化合物反应生成另一种单质好化合物,属于置换反应;
【小问3详解】
要冷却到常温才能“毁罐取出”的原因是防止热的锌在空气中在被氧化;
冷凝器中发生的变化是锌蒸气冷凝得到粗锌,只是状态发生改变,没有新物质生成,属于物理变化,从微观角度分析冷凝器中发生变化的实质是锌原子之间的间隔变小;
【小问4详解】
我国古代冶锌晚于铁和铜,原因是锌的金属活动性比铁、铜强,易被空气中的氧气氧化(合理即可)。
14. 生活中有时需要用到高浓度,供氧方式主要有氧气瓶、氧气袋和制氧机。
氧气瓶和氧气袋中的一般用深冷法制得,该方法利用物质的沸点差异,从空气中分离出。制氧机有膜分离、变压吸附等制氧方式。膜分离制氧用到的膜材料有陶瓷、聚苯胺等,其中混合导电陶瓷分离膜的工作原理示意如图1.变压吸附制氧常用的吸附剂是沸石分子筛。科研人员在一定条件下分别将通过某种沸石分子筛,测定其对的吸附情况、结果如图2(纵坐标数值越大,代表吸附量越大)。吸氧对于缺氧人群有一定作用,但健康人短期内高流量吸氧会对机体造成不良影响,因此不能盲目吸氧。
(1)深冷法制氧利用了物质的_______(填“物理性质”或“化学性质”)差异。
(2)图1中,表示氧分子变成氧原子的是_______(填“Ⅰ”“Ⅱ”或“Ⅲ”)。
(3)由图2可知,25℃时吸附压越大越有利于分离和,证据是_______。
(4)健康人_______(填“能”或“不能”)盲目吸氧。
(5)探究某制氧机中药品用量和温度对反应速率的影响,实验数据如下表:
①制氧原理:第一步:;第二步:在二氧化锰催化下生成氧气。
写出第二步反应的化学方程式:_______。
②上表中a=_______。
③反思上述实验,再提出一个影响产氧速率的因素进一步探究。你的实验方案是_______。
【答案】(1)物理性质
(2)Ⅲ (3)在相同温度下,随着吸附压的增大,N2和O2的吸附量差值逐渐增大
(4)不能 (5) ①. ②. 10 ③. 取相同质量(如10g)的过碳酸钠,分别加入相同质量(如0.3g)但颗粒大小不同的二氧化锰,加入相同体积(如100mL)的水,在相同温度(如26°C)下进行实验,记录收集100mL氧气所用的时间,比较不同颗粒大小催化剂对产氧速率的影响。
【解析】
【小问1详解】
深冷法制氧利用了物质的利用物质的沸点差异,从空气中分离出,过程中没有发生化学反应,利用了物质的物理性质差异;
【小问2详解】
在图甲中,表示氧分子变成氧原子的过程需要涉及到化学变化,即氧分子被分解成氧原子的过程,然而,观察图甲中的三个过程,只有过程II由氧分子变成了氧原子,因此,表示氧分子变成氧原子的是过程II;
【小问3详解】
由图乙可知,在25°℃时,随着吸附压的增大,N2和O2的吸附量都在增加,但是,N2的吸附量增加得更快,而O2的吸附量虽然也在增加,但相对较慢,这意味着在较大的吸附压下,N2和O2之间的吸附差异变得更加明显,从而更有利于它们的分离,因此,证据是在相同温度下,随着吸附压的增大,N2和O2的吸附量差值逐渐增大;
【小问4详解】
健康人短期内高流量吸氧会对人体造成不良影响,如醉氧,所以健康人不可盲目吸氧;
【小问5详解】
①第二步反应是在二氧化锰催化下生成氧气,反应的化学方程式:;
②探究试剂用量和温度对反应速率的影响,实验I 和llI中温度不同,其他条件应相同,所以a=10;
③影响产氧速率的因素还有催化剂的颗粒大小等,实验方案为:取相同质量(如10g)的过碳酸钠,分别加入相同质量(如0.3g)但颗粒大小不同的二氧化锰,加入相同体积(如100mL)的水,在相同温度(如26℃)下进行实验,记录收集100mL氧气所用的时间,比较不同颗粒大小催化剂对产氧速率的影响。
15. 探秘古钱币。
(1)古币金属知多少。我国古代的钱币有多种,如金币、银铜币、铁币等。银铜币多为银白色,金币的颜色是_______。
(2)金属性质共探究。小郑同学做了下列实验:
①如图1,铜片加热时观察到的现象是_______(填标号)。
A.发光放热 B.产生黑色固体 C.生成氧化铜CuO
②如图2,三支试管里的液体均为稀硫酸,铁丝表面有气泡冒出,银丝和铜丝无明显变化。有气泡冒出的反应化学方程式为_______。
(3)货币流通有原因。铁硬度比铜大,密度比铜小,金和银做成的钱币比铜币腐蚀速度要慢得多,似乎更适合铸造钱币,但是中国历史上铜币的使用量远大于其它材质的货币。综上所述,古代铸造钱币选择金属考虑的一个因素是:_______。
【答案】(1)金黄色 (2) ①. B ②. (3)金属的价格
【解析】
【小问1详解】
银铜币多为银白色,金币的颜色是金黄色;
【小问2详解】
①铜片加热时,与氧气反应生成氧化铜,会观察到产生黑色固体,故选B;
②铁丝表面有气泡冒出,是因为铁和稀硫酸反应生成硫酸亚铁和氢气,化学方程式为;
【小问3详解】
铁硬度比铜大,密度比铜小,金和银做成的钱币比铜币腐蚀速度要慢得多,似乎更适合铸造钱币,但是中国历史上铜币的使用量远大于其它材质的货币,金银的价格昂贵,成本高,铜的价格便宜,所以说古代铸造钱币选择金属考虑金属的价格。
16. 兴趣小组开展了与钢铁相关探究活动。
Ⅰ.模拟炼铁(实验装置如右图所示)。
(1)玻璃管中发生的化学反应方程式为_______。
(2)为检验尾气中含有二氧化碳,乙装置中的试剂X是_______(填名称)。
(3)图丙装置的作用是_______。
Ⅱ.探究:加热一段时间后玻璃管中生成的黑色固体是什么?
【查阅资料】①CO与反应的固体生成物与温度的关系如下表:
②FeO为一种黑色固体,和Fe都能被磁铁吸引,和FeO不能被磁铁吸引。
③溶液不与铁的氧化物反应。
【作出猜想】
猜想Ⅰ:固体成分为Fe猜想Ⅱ:固体成分为 猜想Ⅲ:固体成分为FeO
【实验探究】
(4)完成下列实验报告
(5)步骤②中的化学方程式为_______。
(6)工业上冶炼铁的过程中,为了提高铁的产率,温度应不低于_______℃。
【拓展】
(7)1.0g某钢样在纯氧中完全燃烧,得到0.011g二氧化碳,则此钢样中碳的质量分数为_______。
【答案】(1) (2)澄清的石灰水
(3)处理尾气防止空气污染
(4) ①. Ⅲ ②. 溶液由蓝色变成浅绿色
(5)Fe+CuSO4=FeSO4+Cu
(6)700 (7)设碳的质量为x
x=0.003g
此钢样中碳的质量分数为:
答:此钢样中碳的质量分数为0.3%。
【解析】
【小问1详解】
玻璃管中发生的反应是一氧化碳还原氧化铁,生成铁和二氧化碳,化学方程式为:;
【小问2详解】
二氧化碳能使澄清石灰水变浑浊,常用澄清的石灰水检验二氧化碳,故乙装置中的试剂X是澄清石灰水;
【小问3详解】
一氧化碳有毒,会污染空气,且一氧化碳难溶于水,在图丙装置中点燃一氧化碳,故图丙装置的作用是点燃一氧化碳,防止污染空气;
【小问4详解】
①玻璃管冷却后,将固体倒出,用磁铁吸引;Fe3O4和Fe能被磁铁吸引,Fe2O3和FeO不能被磁铁吸引,固体全部被吸引,故固体不可能是FeO,故猜想III不正确;
②根据结论猜想I正确,固体成分为铁,铁能与硫酸铜反应生成硫酸亚铁和铜,向样品中加入足量CuSO4溶液,可观察到有红色固体析出,溶液由蓝色变成浅绿色(或变成浅绿色),说明固体为铁,则猜想 I正确;
【小问5详解】
步骤②中铁能与硫酸铜反应生成硫酸亚铁和铜,发生的化学反应方程式为: Fe+CuSO4=FeSO4+Cu;
【小问6详解】
由题干信息可知,温度在700~800°时,一氧化碳与氧化铁反应生成铁,故为了提高铁的产率,温度应不低于700℃;
【小问7详解】
见答案。
17. 某化学兴趣小组利用以下实验装置探究铁生锈的条件。
【提出问题】铁生锈的条件是什么?
【设计实验】取3根无锈铁丝设计如下图所示的三个实验。
【实验现象】
(1)实验Ⅰ中铁丝生锈,当铁丝足量,时间足够长,打开止水夹后,还能观察到的现象是_______。
【实验结论】
(2)对比实验_______(填序号),可以得出铁生锈需要水;得出“铁生锈需要与氧气接触”这一结论所依据的现象是_______。
【拓展与延伸】海边铁制渔船上的锈迹比江边铁制渔船的多,学生提出问题:海水会加快铁的生锈吗?为验证这一问题,设计以下数字化实验:
(3)①实验2的实验药品是_______。
②根据图像1,说明铁生锈会_______(选填“吸收”或“放出”)热量。
③根据图像2,可以得出结论是_______。
(4)①生活中使用铁制品时需注意的问题是_______。
②因生锈而废弃的铁制品,应如何处理:_______。
【答案】(1)玻璃管左侧液面上升至刻度1处
(2) ①. Ⅰ、Ⅱ ②. 实验Ⅰ中铁丝生锈,实验Ⅲ中铁丝表面无明显变化
(3) ①. 长5cm、直径1mm铁丝,15mL海水 ②. 放出 ③. 海水会加快铁的生锈
(4) ①. 保持铁制品表面干燥等(合理即可) ②. 回收利用
【解析】
【小问1详解】
铁生锈的条件为铁与氧气和水同时接触,铁丝生锈消耗氧气,氧气约占空气体积的,实验Ⅰ中铁丝生锈,当铁丝足量,时间足够长,打开止水夹后,则观察到的现象是玻璃管左侧液面上升至刻度1处;
【小问2详解】
实验Ⅰ铁丝与氧气和水同时接触,会生锈,实验Ⅱ铁丝只与氧气接触,不会生锈,对比实验Ⅰ、Ⅱ可以得出铁生锈需要水;
实验Ⅰ中铁丝与氧气和水同时接触,会生锈,实验Ⅲ中铁丝只与水接触,不会生锈,对比实验Ⅰ、Ⅲ可以得出铁生锈需要氧气,则得出“铁生锈需要与氧气接触”这一结论所依据的现象是实验Ⅰ中铁丝生锈,实验Ⅲ中铁丝表面无明显变化;
【小问3详解】
①该实验是探究海水是否会加快铁的生锈,根据对比实验中,控制变量唯一的原则,除了实验的变量海水外,保证其它条件一致,则表格中实验2实验药品是长5cm、直径1mm铁丝,15mL海水;
②分析图1的曲线可知,随着反应的进行,温度逐渐升高,说明铁生锈放出热量;
③分析图2曲线可知,相同时间内,实验2压强减小比实验1多,说明其它条件下相同时,铁丝在海水中的生锈速率快,故可以得出结论:海水会加快铁的生锈;
【小问4详解】
①铁生锈条件是铁与氧气和水同时接触,隔绝氧气或水,可以达到防锈目的,生活中使用铁制品时需注意的问题是保持铁制品表面干燥,可以有效防止铁制品生锈;
②生锈而废弃的铁制品,回收利用,是保护金属资源的有效措施。
18. 曾作为照相中的显影剂,可由制得.取足量的溶液,加入固体,两者恰好完全反应。(的相对分子质量为104)
试计算:
(1)中硫元素与氧元素的质量比为_______。
(2)消耗的质量(根据化学方程式计算)。
【答案】(1)2:3 (2)设:消耗的质量为x
x=10.4g
答:消耗的质量为10.4g。
【解析】
【小问1详解】
Na2SO3中硫元素与氧元素的质量比为32:(16×3)=2:3;
【小问2详解】
见答案。
实验序号
过碳酸钠的质量/g
二氧化锰的质量/g
水的体积/mL
温度/℃
收集100mL氧气所用的时间/s
Ⅰ
10
0.3
100
26
36.59
Ⅱ
20
0.3
100
26
11.67
Ⅲ
a
0.3
100
41
22
温度
400~500℃
600~680℃
700~800℃
生成物
FeO
Fe
实验步骤
现象
结论
①玻璃管冷却后,将固体倒出,用磁铁吸引
固体全部被吸引
猜想_______不正确
②向样品中加入足量溶液,充分反应。
_______
猜想Ⅰ正确
实验
实验药品
实验1
长5cm、直径1mm铁丝,15mL蒸馏水
实验2
实验序号
过碳酸钠的质量/g
二氧化锰的质量/g
水的体积/mL
温度/℃
收集100mL氧气所用的时间/s
Ⅰ
10
0.3
100
26
36.59
Ⅱ
20
0.3
100
26
11.67
Ⅲ
a
0.3
100
41
22
温度
400~500℃
600~680℃
700~800℃
生成物
FeO
Fe
实验步骤
现象
结论
①玻璃管冷却后,将固体倒出,用磁铁吸引
固体全部被吸引
猜想_______不正确
②向样品中加入足量溶液,充分反应。
_______
猜想Ⅰ正确
实验
实验药品
实验1
长5cm、直径1mm铁丝,15mL蒸馏水
实验2
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

.png)
.png)


