





主题排查5 化学工艺流程(讲义+课件 2份打包)2025年高考化学二轮复习
展开
这是一份主题排查5 化学工艺流程(讲义+课件 2份打包)2025年高考化学二轮复习,文件包含主题排查5化学工艺流程pptx、主题排查5化学工艺流程DOC等2份课件配套教学资源,其中PPT共20页, 欢迎下载使用。
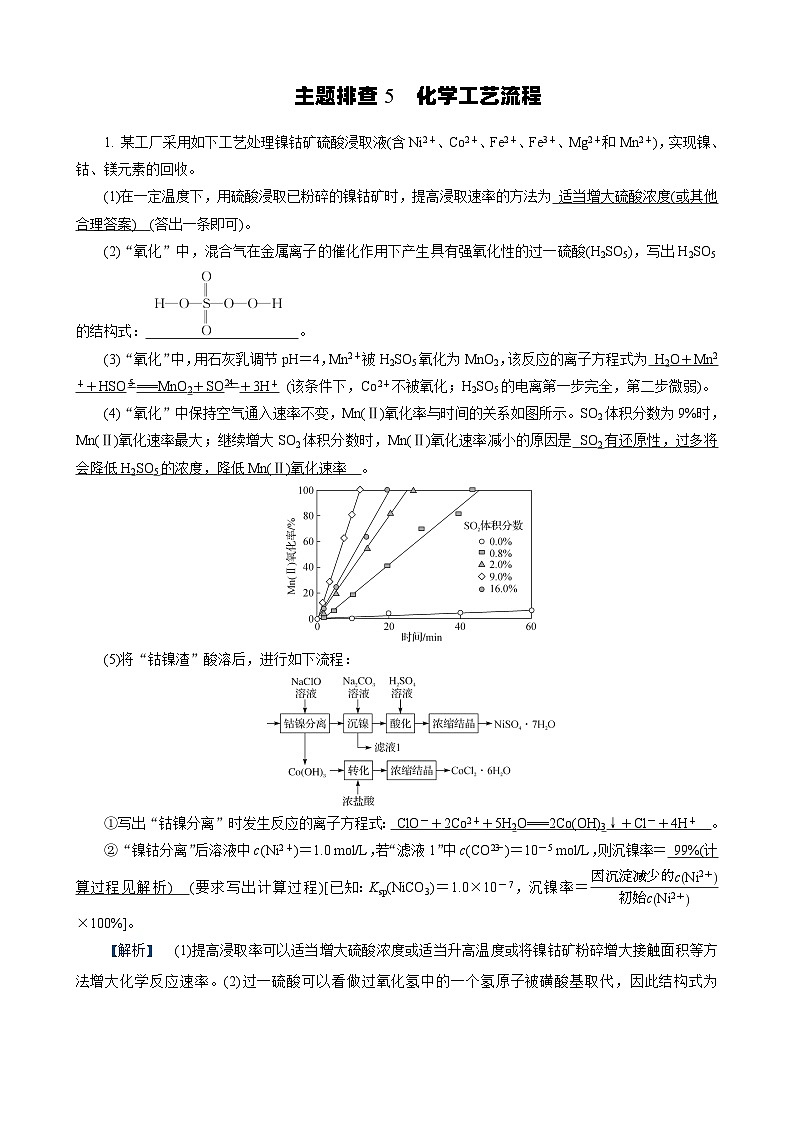
1. 某工厂采用如下工艺处理镍钴矿硫酸浸取液(含Ni2+、C2+、Fe2+、Fe3+、Mg2+和Mn2+),实现镍、钴、镁元素的回收。(1)在一定温度下,用硫酸浸取已粉碎的镍钴矿时,提高浸取速率的方法为_____________________________________答出一条即可)。(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H2SO5),写出H2SO5的结构式:_________________________。(3)“氧化”中,用石灰乳调节pH=4,Mn2+被H2SO5氧化为MnO2,该反应的离子方程式为__________________________________________(该条件下,C2+不被氧化;H2SO5的电离第一步完全,第二步微弱)。
适当增大硫酸浓度(或其他合理答案)
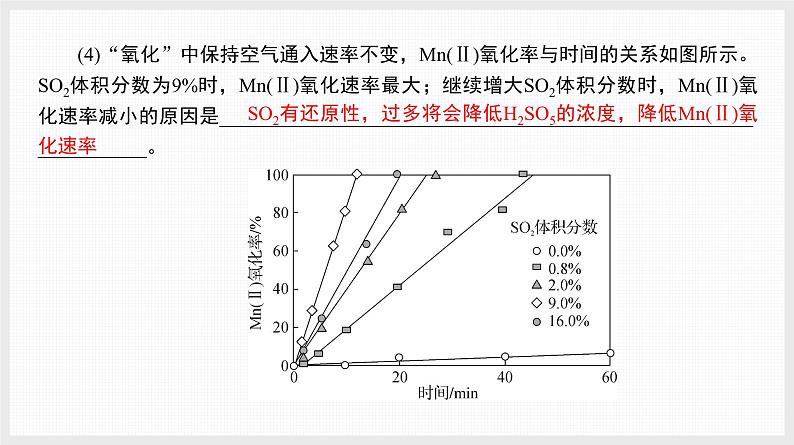
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如图所示。SO2体积分数为9%时,Mn(Ⅱ)氧化速率最大;继续增大SO2体积分数时,Mn(Ⅱ)氧化速率减小的原因是______________________________________________________ ___________。
SO2有还原性,过多将会降低H2SO5的浓度,降低Mn(Ⅱ)氧化速率
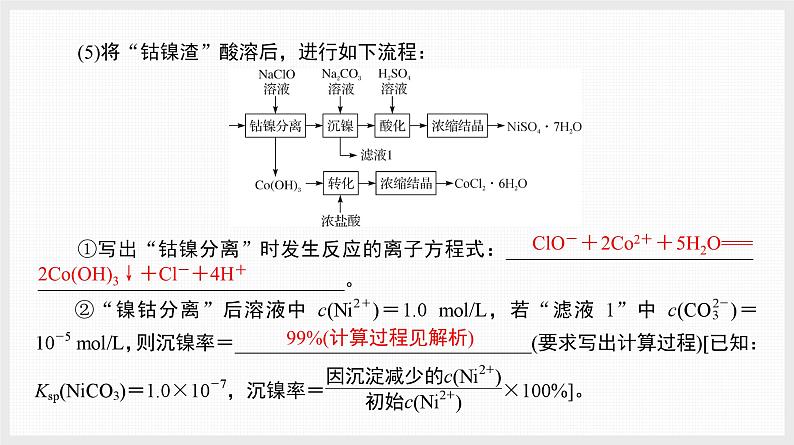
(5)将“钴镍渣”酸溶后,进行如下流程:
①写出“钴镍分离”时发生反应的离子方程式:_________________________ _______________________________。
ClO-+2C2++5H2O=== 2C(OH)3↓+Cl-+4H+
99%(计算过程见解析)
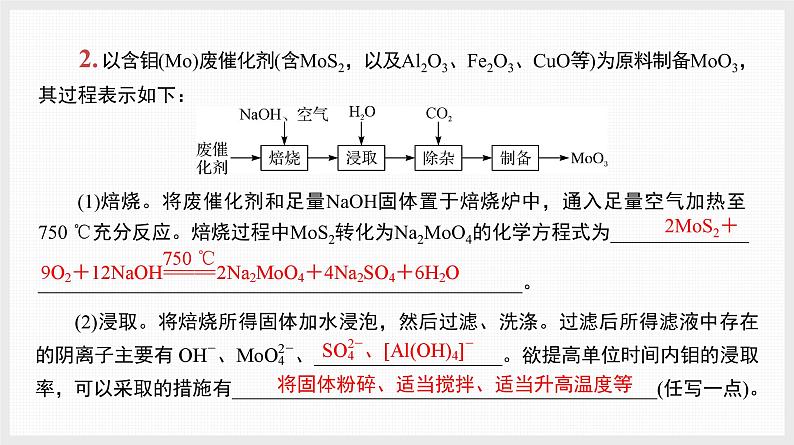
2. 以含钼(M)废催化剂(含MS2,以及Al2O3、Fe2O3、CuO等)为原料制备MO3,其过程表示如下:
(1)焙烧。将废催化剂和足量NaOH固体置于焙烧炉中,通入足量空气加热至 750 ℃充分反应。焙烧过程中MS2转化为Na2MO4的化学方程式为______________ _________________________________________________。
将固体粉碎、适当搅拌、适当升高温度等
(3)除杂。向浸取后的滤液中通入过量CO2,过滤。通入过量CO2的目的是______________________________________________。
将[Al(OH)4]-全部转化为Al(OH)3沉淀除去
7MO3+6NH3↑+7H2O
(5)应用。将MO3制成V2O5-WO3-MO3/TiO2催化剂,用于氨催化还原氮氧化物,一定压强下,将氨氮比为1.0的混合气体按一定流速通入装有上述催化剂的反应装置,测得NOx的转化率随温度的变化关系如图所示。在温度160~240 ℃之间,NOx转化率不高的原因是___________________________________________________ _____________________________________。
温度160~240 ℃之间,催化剂的活性低,同时温度较低反应速率较慢,所以NOx的转化率不高
(1)基态砷原子的电子排布式为______________________________________。
[Ar]3d104s24p3或1s22s22p63s23p63d104s24p3
(2)砷的还原。常温下,As(Ⅴ)溶液中各种微粒的物质的量分数随pH的变化曲线如图所示。向酸性废水中通入SO2,能把As(Ⅴ)转化为As(Ⅲ)。
①H3AsO4的二级电离平衡常数Ka2=________________。②pH为1时“还原”的主要反应的离子方程式为__________________________________________。
(3)中和除杂。当溶液中离子浓度小于1×10-5 ml/L,可认为已经完全除去。已知:Zn(OH)2在pH=10.5时开始转化为[Zn(OH)4]2-,Ksp[Zn(OH)2]=1.2× 10-17,Ksp[Cd(OH)2]=2.5×10-14,lg 2=0.3。①“一级中和”控制pH为2左右,滤渣X的主要成分有___________。②“二级中和”沉淀重金属离子应控制pH范围为_________________。
(4)应用碘量法可测定亚砷酸铜中的铜含量。称取2.000 g试样溶于稀硫酸搅拌后过滤,洗涤滤渣,将洗涤后的滤液与原滤液合并,配成250 mL溶液,取25.00 mL所配溶液于碘量瓶中加入过量的碘化钾溶液,用0.030 00 ml/L Na2S2O3标准溶液滴定至终点,消耗25.00 mL。①计算样品中铜元素的质量分数(写出计算过程)。答案:24.00%(计算过程见解析)
样品中可能含有Cu(OH)2、CuO
4. 硼化钛(TiB2)常用于制备导电陶瓷材料。Ⅰ. 高钛渣(主要含TiO2、SiO2、Al2O3和CaO,少量MgO、Fe2O3)为原料制取TiB2的流程如图:
已知:①B2O3高温易挥发;②TiO2可溶于热的浓硫酸形成TiO2+。(1)“酸浸”后的滤液中的阳离子有:H+、Fe3+、______________________。(2)“水解”需在沸水中进行,离子方程式为__________________________ _________________________。
Al3+、Ca2+、Mg2+
TiO2·xH2O↓+2H+
Ⅱ. 气相沉积法获得硼化钛:以TiCl4和BCl3为原料,在过量的H2参与下,沉积温度为800~1 000 ℃,可制得具有空间网状结构的磨料级硼化钛。(4)制得硼化钛的化学方程式为________________________________________,硼化钛能作为磨料的原因是____________________________。(5)生产硼化钛,当BCl3和TiCl4投料比[m(BCl3)∶m(TiCl4)]超过1.25时硼化钛的纯度下降,原因是___________________________________。Ⅲ. 硼砂(Na2B4O7·10H2O)与NaOH的混合溶液中加入H2O2可以制备X(Na2B2O8H4)。已知X的阴离子[B2O8H4]2-只有一种化学环境的B原子,结构中有1个六元环且B和O原子最外层都达到8电子稳定结构。(6)X阴离子的结构式为_________________________。
硼化钛是共价晶体,硬度大
BCl3过量,被过量的氢气还原为单质硼
【解析】 (1)“酸浸”加入稀盐酸与Al2O3、CaO、MgO、Fe2O3反应生成AlCl3、CaCl2、MgCl2、FeCl3,“酸浸”后的滤液中的阳离子有H+、Fe3+、Al3+、Ca2+、Mg2+。(3)“热还原”中B2O3的实际用量超过了理论化学计量所要求的用量,原因是B2O3高温下蒸气压大、易挥发。(4)硼化钛由Ti和B原子相连构成空间网状结构,说明硼化钛是共价晶体,硬度大。(5)当BCl3和TiCl4投料比[m(BCl3):m(TiCl4)]超过1.25时硼化钛的纯度下降,原因是BCl3过量,被过量的氢气还原为单质硼。(6)X的阴离子[B2O8H4]2-只有一种化学环境的B原子说明结构对称,结构中有1个六元环且B和O原子最外层都达到8电子稳定结构,则B原子与4个O原子相连,X阴离子的结构式见答案。
相关课件
这是一份基础排查5 实验操作、现象与结论(讲义+课件 2份打包)2025年高考化学二轮复习,文件包含基础排查5实验操作现象与结论pptx、基础排查5实验操作现象与结论DOC等2份课件配套教学资源,其中PPT共9页, 欢迎下载使用。
这是一份主题排查8 有机推断与合成(讲义+课件 2份打包)2025年高考化学二轮复习,文件包含主题排查8有机推断与合成pptx、主题排查8有机推断与合成DOC等2份课件配套教学资源,其中PPT共20页, 欢迎下载使用。
这是一份主题排查6 归因分析 过程描述(讲义+课件 2份打包)2025年高考化学二轮复习,文件包含主题排查6归因分析过程描述pptx、主题排查6归因分析过程描述DOC等2份课件配套教学资源,其中PPT共35页, 欢迎下载使用。









