

进贤县第一中学2024-2025学年高三上学期11月期中考试化学试卷(含答案)
展开
这是一份进贤县第一中学2024-2025学年高三上学期11月期中考试化学试卷(含答案),共19页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。
一、单选题
1.下列有关化学用语使用正确的是( )
A.氢氧化钠的电子式:
B.S原子的结构示意图:
C.离子半径:
D.分子的结构式:
2.关于反应,下列说法不正确的是( )
A.是这个反应的还原产物
B.产生大量红棕色刺激性气味的气体,溶液呈蓝绿色
C.硝酸在反应中表现氧化性的物质的量与表现酸性的物质的量之比为2:1
D.从上述反应中可以得出物质氧化性强弱关系:
3.下列离子方程式书写正确的是( )
A.Fe与过量稀硝酸反应:
B.向NaOH溶液中通入过量:
C.用热NaOH溶液洗涤试管内壁的硫黄:
D.将金属钠投入水中:
4.下列有关几种试纸使用的描述中,不正确的是( )
A.用湿润的红色石蕊试纸检验某种气体是否是
B.某种有色溶液可使淀粉试纸变蓝色,则该溶液中可能含有
C.用玻璃棒蘸取溶液点在用蒸馏水湿润过的pH试纸上可测量该溶液的pH
D.将湿润的蓝色石蕊试纸片粘在玻璃棒上置于氯气中,试纸先变红后褪色
5.下列实验操作中,不正确的是( )
A.AB.BC.CD.D
6.在给定条件下,下列物质间的转化均能实现的是( )
A.
B.
C.
D.
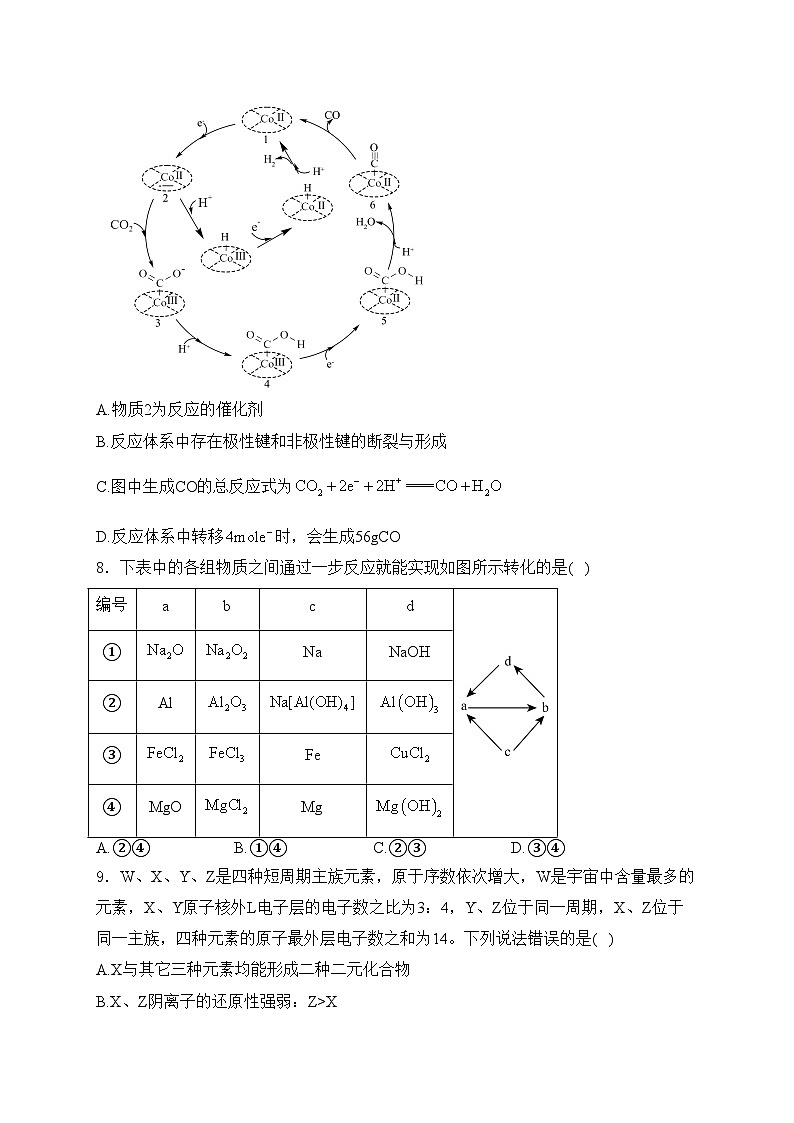
7.为了应对日益加剧的能源需求和气候变化,科学家开发了一种利用过渡金属大环配合物(虚线圈表示大环配体)电催化生成CO的方法,该方法中同时存在竞争性的析氢反应,反应过程如右图所示。下列说法正确的是( )
A.物质2为反应的催化剂
B.反应体系中存在极性键和非极性键的断裂与形成
C.图中生成CO的总反应式为
D.反应体系中转移时,会生成56gCO
8.下表中的各组物质之间通过一步反应就能实现如图所示转化的是( )
A.②④B.①④C.②③D.③④
9.W、X、Y、Z是四种短周期主族元素,原于序数依次增大,W是宇宙中含量最多的元素,X、Y原子核外L电子层的电子数之比为3:4,Y、Z位于同一周期,X、Z位于同一主族,四种元素的原子最外层电子数之和为14。下列说法错误的是( )
A.X与其它三种元素均能形成二种二元化合物
B.X、Z阴离子的还原性强弱:Z>X
C.X、Y、Z的简单离子半径大小:Z>X>Y
D.X和Z的简单氢化物沸点:XS,非金属性越强,对应阴离子的还原性越弱,则X、Z阴离子的还原性强弱:Z>X,故B正确;
C.氧离子和钠离子具有相同电子层,核电荷数越大离子半径越小,则简单离子半径X>Y,硫离子半径氧离子半径,即离子半径大小:Z>X>Y
,故C正确;
D.水分子之间存在氢键,导致水的沸点较高,即X和Z的简单氢化物沸点:X>Z,故D错误;
故选:D。
10.答案:B
解析:A.氯化钠在溶液中电离产生钠离子和氯离子,所以氯化钠溶液中存在自由移动的离子,能导电,故A正确;
B.碳酸钙与稀盐酸反应生成二氧化碳和水,离子方程式为:,故B错误;
C.NaOH固体和铝粉混合,铝与氢氧化钠溶液反应生成四羟基合铝酸钠和氢气,离子方程式为:,故C正确;
D.铝粉和氧化铁组成的铝热剂用于焊接钢轨,铝与氧化铁反应生成氧化铝和铁,化学方程式为:,故D正确;
故选:B。
11.答案:A
解析:A.①中HCl遇KI溶液不能发生反应产生,所以不会出现溶液变蓝的现象,A错误;
故选A。
12.答案:B
解析:A.分子是由C原子和O原子构成的,A项错误;
B.溶解度随温度的升高而降低,升高温度,不饱和溶液会变为饱和溶液,B项正确;
C.Mg与稀硫酸反应生成硫酸镁和氢气,则1.2g镁与10g稀硫酸充分反应后所得的溶液质量小于11.2g,C项错误;
D.和化学性质不同,D项错误;
故选B。
13.答案:C
解析:A.标准状况下乙醇不是气态,22.4L乙醇的物质的量不是1ml,A错误;
B.1ml甲基中含有的电子数为,B错误;
C.乙炔和苯的最简式相同,均是CH,可以按CH计算,则13g乙炔和苯的混合气体中含有原子总数为,C正确;
D.乙酸是弱酸,不能完全电离,则乙酸溶液中数目小于,D错误,
答案选C。
14.答案:D
解析:A.电子从基态到激发态需要吸收能量,产生的光谱是吸收光谱,A错误;
B.氯化铵的电子式应为,B错误;
C.Ca为20号元素,原子核外有20个电子,电子排布式为,C错误;
D.中心原子孤电子对数等于,a是中心原子的价电子数,x是中心原子结合的原子数,b是与中心原子结合的原子最多能接受的电子数,据此可知的孤电子对数=1,的孤电子对数=2,的中心原子的孤电子对数=0,但O原子的孤电子对数=4,所以中孤电子对数为4,HCl的孤电子对数=3,所以孤电子对数最多的是,D正确;
综上所述正确答案为D。
15.答案:(1)粉碎固体颗粒;空气大大过量
(2)
(3);
(4)PbS
(5)当,,,所以会析出沉淀
(6)“结晶”得到的粗品溶解得到溶液,蒸发浓缩,冷却结晶,过滤、洗涤、干燥
解析:(1)可采取将钼精矿粉碎或通入过量的空气提高焙烧效率;
答案为:①粉碎固体颗粒,②空气大大过量;
(2)中M和S的化合价分别为+4、-2,“焙烧”时转化为和,M和S的化合价均升高,所以,该反应过程的氧化产物是和;
答案为:;
(3)根据题意分析可知,“碱浸”时和反应生成,所以,该化学方程式为:;在碱性条件下,加入NaClO溶液,也生成钼酸钠,同时有生成,M和S被氧化,则Cl应被还原成,根据电子守恒、电荷守恒、质量守恒,可写出该反应的离子方程式:;
答案为:;;
(4)若“除重金属离子”时加入的沉淀剂为,则有反应:,所以废渣成分为PbS;
答案为:PbS;
(5) 当,,,所以会析出沉淀;
答案为:当,,,所以会析出沉淀;
(6)“重结晶”过程的具体操作是:为除去“结晶”得到的粗品中的可溶性杂质,可将粗品溶解得到溶液,蒸发浓缩,冷却结晶,过滤、洗涤、干燥;
答案为:“结晶”得到的粗品溶解得到溶液,蒸发浓缩,冷却结晶,过滤、洗涤、干燥。
16.答案:(1)
(2)
(3)还原反应;
(4)10
(5)
解析:(1)相对分子质量为92的某芳香烃X是一种重要的有机化工原料,令分子组成为CxHy,则,由烷烃中C原子与H原子关系可知,该烃中C原子数目不能小于7,故该芳香烃X的分子式为、结构简式为,其中A是X的一氯代物,A经过一系列反应可得醛C,故A为,分子式为,故答案为:;
(2)H是一种功能高分子,为通过形成肽键发生缩聚反应形成的,高聚物H的结构简式为,故答案为:;
(3)在浓硫酸、加热条件下与浓硝酸发生取代反应生成F,结合反应③的产物可知F为,F转化生成G,由于苯胺容易被氧化,由信息反应Ⅰ、信息反应Ⅱ可知,G为,故先氧化后还原,所以反应③的反应类型为还原反应。X与氯气发生取代反应生成A,A转化生成B,B催化氧化生成C,C能与银氨溶液反应生成D,故B含有醇羟基、C含有醛基,B为,C为,D酸化生成E,故D为,E为,故反应⑤的离子反应方程式是,
故答案为:还原反应;;
(4)阿司匹林有多种同分异构体,其中含有2个羧基的芳香族化合物,分离出2个羧基,剩下的骨架为甲苯,相当于找甲苯的二羧基代物,用-A代表-COOH,则有10种同分异构体,如图所示,
故答案为:10;
(5)在催化剂条件下发生加成反应生成,再在氢氧化钠醇溶液、加热条件下发生消去反应生成,与氯气发生加成反应生成,最后在氢氧化钠水溶液中发生水解反应生成,合成反应流程图为;
故答案为:;
17.答案:(1)第三周期第IVA族
(2)最外层均为4个电子,均与氯形成4个公用电子对达到稳定结构
(3)N
(4)H为-1价
(5)平面三角形;B原子提供空轨道,OH-中的氧原子提供孤电子对,形成配位键
(6);均属共价晶体,结构相似,B-N键长比Si-C键短,键能更大;
解析:(1)Si是14号元素,原子核外由3个电子层,最外层电子数为4,则硅在元素周期表中的位置为第三周期第IVA族;
(2)硅和锗都位于第IVA族,最外层均为4个电子,均与氯形成4个共用电子对达到稳定结构;
(3)镓()是31号元素,处于第四周期第ⅢA族,最高能层的符号为N;
(4)中的H为-1价,体现出强还原性易被氧化为0价,所以具有强还原性;
(5)①硼酸分子中的B原子采取杂化,键数为3,没有孤电子对,故空间构型为平面三角形;
②硼酸具有弱酸性是由于B与水中的OH-形成配位键,B原子的价电子式为,可提供一个p轨道作为空轨道,接受OH-中O原子提供的孤电子对形成配位键;
(6)①由图可知每个B原子距离最近的N原子由4个,B原子的价层电子对数为4,轨道杂化类型为杂化;
②该种氮化硼的熔点和硬度均高于SiC的原因是由于N原子的半径小于C,B原子的半径小于Si,N-B键的键长小于C-Si键,N-B键的键能大于C-Si键,故该种氮化硼的熔点和硬度均高于SiC;
③已知该晶体的密度为,阿伏伽德罗常数为,晶胞中N为4个,B为4个,设晶胞的变成为acm,,则晶胞的边长为。
18.答案:(1)圆底烧瓶
(2)脱水;黑色固体体积膨胀;;浓硫酸溶于水时放热,为后续反应提供较高温度;品红溶液褪色
(3)有漂白性
(4)产生黄色浑浊
(5)酸性溶液;溶液不褪色
解析:(1)根据仪器的构造可知,仪器A的名称是圆底烧瓶;
(2)A中滴入浓硫酸后,观察到蔗糖逐渐变黑,这是因为浓硫酸具有脱水性;因脱水产生的碳继续被浓硫酸氧化产生二氧化硫和二氧化碳气体,故之后观察到的现象是黑色固体体积膨胀,有关反应的化学方程式;蔗糖中滴加少量水的目的是浓硫酸溶于水时放热,为后续反应提供较高温度;
(3)装置B中观察到的现象是品红溶液褪色,由此得出的结论是有漂白性;
(4)二氧化硫进行装置C后,生成的亚硫酸与硫离子反应产生硫单质,故装置C中观察到的现象是产生黄色浑浊;
(5)为证明实验最终排放的气体不污染空气,装置D中的X应是能与二氧化硫反应的物质,故可以装有酸性溶液,且应该过量,故试管中的现象是溶液不褪色。
A加热液体
B取用固体粉末
C稀释浓硫酸
D点燃酒精灯
编号
a
b
c
d
①
Na
NaOH
②
Al
③
Fe
④
MgO
Mg
实验
现象
①中溶液变蓝
②中溶液产生胶状沉淀
③中生成沉淀
④中产生刺激性气体
物质
熔点/℃
硬度
碳化硅(SiC)
2830
9-9.5
氮化棚(BN)
3000
9.5
相关试卷
这是一份大庆第一中学2024-2025学年高三上学期期中考试化学试卷,共13页。
这是一份上海市育民中学2024-2025学年高三上学期期中考试化学试卷(含答案),共12页。试卷主要包含了苯乙烯的制备,三氯化铬的制备和性质探究,有机物的性质与合成,合成盐酸文法拉辛等内容,欢迎下载使用。
这是一份江西省进贤县第一中学2024-2025学年高二上学期10月月考化学试题,共7页。试卷主要包含了单选题等内容,欢迎下载使用。








