






2025版高考化学全程一轮复习第12讲铁及其化合物课件
展开
这是一份2025版高考化学全程一轮复习第12讲铁及其化合物课件,共50页。PPT课件主要包含了考点一,考点二,考点三,+2+3,答案D,提供水蒸气,FeO,①②③⑤,恒压滴液漏斗,防止Fe2+被氧化等内容,欢迎下载使用。
1.掌握铁及其化合物的主要性质及其应用。2.了解铁及铁氢氧化物的制备方法。3.能鉴别溶液中的Fe2+、Fe3+。
考点一 铁的单质、氧化物1.变价金属——铁(1)物理性质银白色固体,熔点较高,具有良好的导热、导电、延展性,能被磁体吸引。(2)化学性质①与非金属的反应Fe与Cl2:2Fe+3Cl2 2FeCl3;Fe与S:________________________;Fe与I2:________________________。②Fe与水蒸气的反应:____________________________。
③与酸反应Fe与H+:Fe+2H+===Fe2++H2↑;常温下,Fe遇浓HNO3、浓H2SO4发生钝化反应,加热时可将铁氧化为+3价铁盐。④与某些盐溶液的反应与CuSO4溶液反应的离子方程式:Fe+Cu2+===Fe2++Cu。与FeCl3溶液反应的离子方程式:________________________。
Fe+2Fe3+===3Fe2+
(3)生铁的冶炼(苏教版教材)①原料:铁矿石、焦炭、空气、石灰石。②设备:高炉。③主要反应a.还原剂的生成:C+O2 CO2,CO2+C 2CO;b.铁的还原:____________________________;c.造渣反应:CaCO3 CaO+CO2↑,CaO+SiO2 CaSiO3。【师说·助学】 铁在空气中形成铁锈的主要成分是Fe2O3·xH2O,在纯氧中燃烧的产物是Fe3O4。
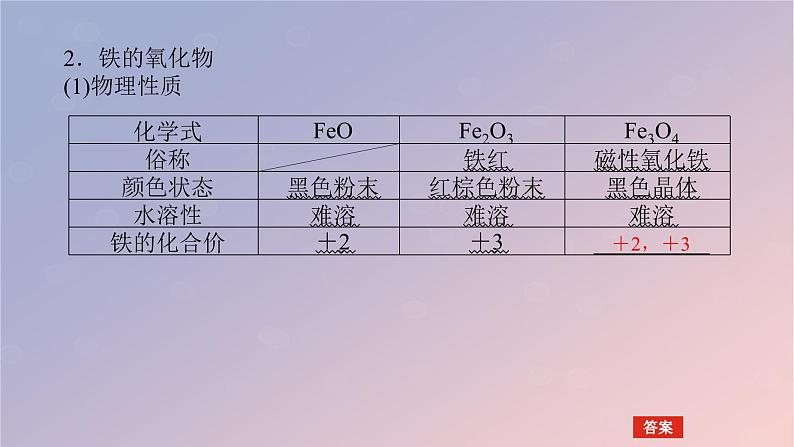
2.铁的氧化物(1)物理性质
(2)化学性质①与盐酸反应的离子方程式分别为:FeO:FeO+2H+===Fe2++H2O;Fe2O3:Fe2O3+6H+===2Fe3++3H2O;Fe3O4:____________________________。②FexOy与CO反应:FexOy+yCO xFe+yCO2。
Fe3O4+8H+===2Fe3++Fe2++4H2O
【易错诊断】 判断正误,错误的说明理由。1.铁与过量的硫粉共热产物是Fe2S3:__________________________________________________________。2.用铁制容器可以运输浓硝酸和浓硫酸:__________________________________________________________。3.Fe在O2中燃烧或高温下与水蒸气反应均能得到Fe3O4:__________________________________________________________。4.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2:__________________________________________________________。
错误。铁与硫粉共热产物是FeS,与硫粉的用量无关。
错误。Fe与Cl2反应只生成FeCl3,与Cl2的用量无关。
【教考衔接】典例 铁与水蒸气反应实验改进前后的装置如图所示:
下列说法错误的是( )A.将湿棉花改为浸水的尿不湿,酒精灯由单头改为双头,可提供足量的水蒸气B.用具支试管可将试管口附近冷凝的水导出,避免冷凝水与灼热铁粉接触C.肥皂液改为吹泡泡水,收集H2效果更好,点燃效果更明显D.悬挂的磁铁仅能吸引铁粉,不能吸引反应产物
解析:铁与水蒸气在高温下反应生成四氧化三铁和氢气,铁、四氧化三铁均可被磁铁吸引,故D错误。
【师说·延伸】 铁与水蒸气反应实验装置对比——回归教材
【对点演练】考向一 铁及其氧化物的性质1.写出下列反应的离子方程式。(1)FeO溶于足量稀硝酸中:__________________________________。(2)Fe2O3溶于足量HI溶液中:________________________________。
Fe2O3+6H++2I-===2Fe2++I2+3H2O
2.铁与水蒸气反应,通常有以下两种装置,请回答下列问题:
(1)装置一中,装置A的作用:____________。装置二中,装湿棉花的作用:____________。(2)实验完毕后,取出装置一的少量固体,溶于足量稀盐酸,再滴加KSCN溶液,溶液颜色无明显变化,试解释原因:___________________________________。
在溶液中Fe3+被未反应的铁粉完全还原为Fe2+
考向二 计算铁氧化物的组成3.有一块铁的“氧化物”样品,用140 mL 5.0 ml·L-1盐酸恰好将之完全溶解,所得溶液还能吸收0.025 ml Cl2,恰好使其中的Fe2+全部转变为Fe3+,计算确定该氧化物的化学式。
解析:根据2Fe2++Cl2===2Fe3++2Cl-,可知铁的“氧化物”样品用盐酸溶解后所得溶液中n(Fe2+)=0.025 ml×2=0.05 ml,根据电荷守恒得2n(Fe2+)+3n(Fe3+)=n(Cl-),则n(Fe3+)=0.2 ml,故n(Fe2+)∶n(Fe3+)=0.05∶0.2=1∶4,故该氧化物可表示为FeO·2Fe2O3,即Fe5O7。答案:Fe5O7
4.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4.00 g,则该氧化物的化学式为______。
考点二 铁的氢氧化物1.性质比较
白色沉淀迅速变成灰绿色,最后变成红褐色
4Fe(OH)2+O2+2H2O===4Fe(OH)3
【师说·助学】 Fe2O3、Fe3O4、Fe(OH)3与足量氢碘酸(HI)反应时,Fe3+被I-还原成Fe2+。
2.制备方法(1)Fe(OH)2:可溶性亚铁盐与碱溶液反应。(2)Fe(OH)3:可溶性铁盐与碱溶液反应。
错误。应得到Fe(OH)3沉淀。
错误。应生成FeI2,反应的离子方程式为2Fe(OH)3+2I-+6H+===2Fe2++I2+6H2O。
【教考衔接】典例 用FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。(1)除去蒸馏水中溶解的O2常采用______的方法。(2)用硫酸亚铁晶体配制上述FeSO4溶液时还需要加入________________。(3)生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是__________________________________。
避免生成的Fe(OH)2沉淀接触O2而被氧化
解析:(1)气体的溶解度是随温度升高而降低的,所以煮沸后的蒸馏水中溶解的O2变少。(2)Fe2+易水解,要加入稀H2SO4防止其水解;Fe2+易被空气中的O2氧化,要加铁粉,将被氧化生成的Fe3+还原成Fe2+。
【对点演练】探究制备氢氧化亚铁的可行性方案1.下列各图示中能较长时间看到Fe(OH)2白色沉淀的是________(填序号)。
解析:因为Fe(OH)2在空气中很容易被氧化为红褐色的Fe(OH)3,即4Fe(OH)2+O2+2H2O===4Fe(OH)3,因此要较长时间看到Fe(OH)2白色沉淀,就要排除装置中的氧气或空气。①、②原理一样,都是先用氢气将装置中的空气排尽,并使生成的Fe(OH)2处在氢气的保护中;③的原理为铁作阳极产生Fe2+,与电解水产生的OH-结合生成Fe(OH)2,且液面用汽油保护,能防止空气进入;⑤中液面加苯阻止了空气进入;④由于带入空气中的氧气能迅速将Fe(OH)2氧化,因而不能较长时间看到白色沉淀。
2.用如图所示装置(夹持仪器省略)制备氢氧化亚铁。实验步骤如下:Ⅰ.检查装置气密性后,关闭K2、K5、K6,打开K1、K3、K4,使装置A中产生的气体进入装置B中,排尽装置B中空气。Ⅱ.待装置B中空气排尽后,关闭K3,打开K2,将装置A中溶液压入装置B中并观察现象。Ⅲ.关闭K1、K2,打开K5、K6,使装置C中气体通入装置B中并观察现象。
回答下列问题:(1)仪器a的名称是_____________,B中长玻璃管的作用是______________________________。(2)步骤Ⅲ装置B中的现象是________________________________,其发生反应的化学方程式为________________________________。
平衡气压,辅助排出装置B中的空气
白色沉淀迅速变为灰绿色,最后变为红褐色
解析:氢氧化亚铁容易被氧气氧化,因此打开K1、K3、K4,关闭K2、K5、K6,装置A中产生H2,排出装置B中的空气,因此长导管作用之一是辅助排出装置B中的空气,作用之二是平衡压强,防止装置中压强过大,发生危险。
归纳总结防止Fe(OH)2被氧化的方法(1)将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。(2)将盛有NaOH溶液的胶头滴管尖端插入试管的亚铁盐溶液底部,并慢慢挤出NaOH溶液。(3)在亚铁盐溶液上面充入保护气,如H2、N2、稀有气体等。(4)在亚铁盐溶液上面加保护层,如苯、植物油等。(5)用Fe作阳极,石墨作阴极,电解NaOH溶液,利用新产生的Fe2+与OH-反应制取。
考点三 亚铁盐与铁盐1.亚铁盐含有Fe2+的溶液呈浅绿色,既有氧化性,又有还原性,其中还原性为主。(1)还原性Fe2+的酸性溶液与H2O2反应的离子方程式为_______________________________。(2)弱氧化性Fe2+与Zn反应的离子方程式为Zn+Fe2+===Fe+Zn2+。
2Fe2++H2O2+2H+===2Fe3++2H2O
2Fe3++2I-⇌2Fe2++I2
3.Fe2+、Fe3+的检验方法(1)用KSCN溶液和氯水(2)用NaOH溶液
3Fe2++2[Fe(CN)6]3-===Fe3[Fe(CN)6]2↓
错误。中性溶液中Fe3+完全水解为Fe(OH)3。
错误。离子方程式应为Fe3++3SCN-===Fe(SCN)3,其中Fe(SCN)3溶于水。
错误。酸性KMnO4溶液遇Cl-能褪色,Cl-的存在干扰Fe2+的检验。
【教考衔接】典例 [全国卷Ⅱ]某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 ml·L-1的溶液。在FeCl2溶液中需加入少量铁屑,其目的是__________________。(2)甲组同学取2 mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_____________________。(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是___________________________________。
2Fe2++Cl2===2Fe3++2Cl-
隔绝空气(排除氧气对实验的影响)
解析:(1)亚铁离子具有还原性,能被空气中的氧气氧化,所以在配制的FeCl2溶液中加入少量铁屑的目的是防止Fe2+被空气氧化。
(4)丙组同学取10 mL 0.1 ml·L-1KI溶液,加入6 mL 0.1 ml·L-1 FeCl3溶液混合。分别取2 mL此溶液于3支试管中进行如下实验:①第一支试管中加入1 mL CCl4充分振荡、静置,CCl4层显紫色;②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;③第三支试管中加入1滴KSCN溶液,溶液变红。实验②检验的离子是________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有________(填离子符号),由此可以证明该氧化还原反应为__________。
解析:(4)根据Fe2+的检验方法,向溶液中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀,一定含有Fe2+,则实验②检验的离子是Fe2+;Fe3+遇KSCN溶液显红色,实验①和③说明,在I-过量的情况下,溶液中仍含有Fe3+,由此可以证明该氧化还原反应为可逆反应。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为________________________________;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是__________________________,生成沉淀的原因是________________________________________(用平衡移动原理解释)。
H2O2+2Fe2++2H+===2Fe3++2H2O
Fe3+催化H2O2分解产生O2
H2O2分解反应放热,促进Fe3+的水解平衡正向移动
【对点演练】考向一 Fe2+、Fe3+的检验1.下列离子的检验方法合理的是( )A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+B.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+C.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+
解析:A项中只能说明含有Fe3+,不能说明不含Fe2+;B项原溶液中也可能只有Fe3+而没有Fe2+;D项中氧化后生成的红褐色沉淀Fe(OH)3也可能掩盖了生成的白色沉淀Mg(OH)2。
2.为探究某绿矾样品的变质情况,化学兴趣小组的同学设计了下列实验方案。可供选择的试剂:硫氰化钾溶液、酸性高锰酸钾溶液、氯水、氢氧化钠溶液、氯化钡溶液,请参与完成方案设计。实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液。(1)如何证明绿矾已经被氧化___________________________________________________________。(2)如何证明绿矾已经被完全氧化________________________________________________________________________。(3)在使用硫酸亚铁时,防止Fe3+的干扰的方法_____________________________,写出相关离子方程式。
取少量溶液,加入几滴硫氰化钾溶液,若溶液变红色,则证明绿矾样品已被氧化。
取少量溶液,加入几滴酸性高锰酸钾溶液,若溶液不褪色,则证明绿矾样品已被完全氧化。
加入适量铁粉,Fe+2Fe3+===3Fe2+
归纳总结检验Fe2+和Fe3+时的注意事项(1)检验Fe2+时不能先加氯水后加KSCN溶液,也不能将加KSCN后的混合溶液加入到足量的新制氯水中(新制氯水能氧化SCN-)。(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO4溶液检验Fe2+(Cl-能还原酸性KMnO4,有干扰)。(3)检验Fe2+、Fe3+的其他方法:检验Fe3+也可用苯酚(C6H5OH);检验Fe2+最好用K3[Fe(CN)6]溶液。
考向二 Fe2+与Fe3+的性质3.[2023·浙江1月,16]探究铁及其化合物的性质,下列方案设计、现象和结论都正确的是( )
解析:往FeCl2溶液中加入Zn片,发生反应Fe2++Zn===Fe+Zn2+,Fe2+的氧化能力比Zn2+的强,A项错误;往Fe2(SO4)3溶液中滴加KSCN溶液,发生反应Fe3++3SCN-⇌Fe(SCN)3,溶液变血红色,再加入少量K2SO4固体,对平衡无影响,故不能说明Fe3+与SCN-的反应不可逆,B项错误;若食品脱氧剂样品中有+3价铁,铁粉与+3价铁发生反应Fe+2Fe3+===3Fe2+,滴加KSCN溶液,溶液呈浅绿色,C项错误;向沸水中逐滴加5~6滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,得到Fe(OH)3胶体,持续煮沸,Fe(OH)3胶体发生聚沉,析出红褐色沉淀,D项正确。
4.在FeCl3、CuCl2混合溶液中,加入铁粉与铜粉的混合物。(1)若金属无剩余,则溶液中一定存在的金属阳离子有__________,可能存在的有________。(2)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有________,一定不存在___________。(3)若剩余固体中只有铜,则溶液中一定存在的金属阳离子有________,可能存在的有________,一定不存在________。
相关课件
这是一份新高考化学一轮复习讲义课件 第3章 第16讲 铁及其化合物的转化关系,共60页。PPT课件主要包含了复习目标,真题演练明确考向,课时精练巩固提高,内容索引,知识梳理·夯基础,递进题组·练能力,Cl2,FeCl3,FeOH2,S2-等内容,欢迎下载使用。
这是一份2025届高中化学全程复习构想课件全套12铁及其化合物,共51页。PPT课件主要包含了考点一,考点二,考点三,+2+3,答案D,提供水蒸气,FeO,①②③⑤,恒压滴液漏斗,防止Fe2+被氧化等内容,欢迎下载使用。
这是一份第8讲 铁及其化合物 课件—2025届高考化学大一轮复习,共60页。PPT课件主要包含了第8讲铁及其化合物,必备知识·强基固本,关键能力·核心突破,素养评价·真题演练,知识梳理,自主评价等内容,欢迎下载使用。









