

安徽省芜湖市第一中学2024-2025学年高二上学期期中考试 化学试题(原卷版)-A4
展开
这是一份安徽省芜湖市第一中学2024-2025学年高二上学期期中考试 化学试题(原卷版)-A4,共9页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
一、选择题(每小题只有一个正确答案,每小题3分)
1. 下列变化中的能量改变方式与其他三项不同的是
A. 碳酸钙受热分解B. 和反应
C. 制备水煤气D. 钠与水反应
2. 下列各说法中,正确的是
A. 能够自发进行的反应不一定都是放热反应
B. 能够自发进行的反应就一定能够发生并完成
C. 同一物质:固体→液体→气体变化是焓减和熵增的过程
D. -10℃的水结成冰,可用熵变判据来解释该变化过程的自发性
3. 已知温度T时水的离子积常数为Kw,该温度下,将浓度为a ml/L的一元酸HA与b ml/L的一元碱BOH等体积混合,可判断溶液呈中性的依据是
A. a=bB. 混合溶液中,c(H+)+c(B+)=c(OH﹣)+c(A﹣)
C. 混合溶液中,c(H+)=D. 混合溶液的pH=7
4. 工业生产硫酸过程中,在接触室中被催化氧化为,已知该反应为放热反应。现将2ml和1ml充入一密闭容器充分反应后,放出热量a kJ,此时测得的转化率为50%,则下列热化学方程式中正确的是
A.
B.
C.
D.
5. 下列事实不能用勒夏特列原理解释的是
A. 工业合成氨采用高温条件
B. 实验室中常用排饱和食盐水的方法收集氯气
C. 实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出
D. 工业生产硫酸使用过量的空气以提高二氧化硫的利用率
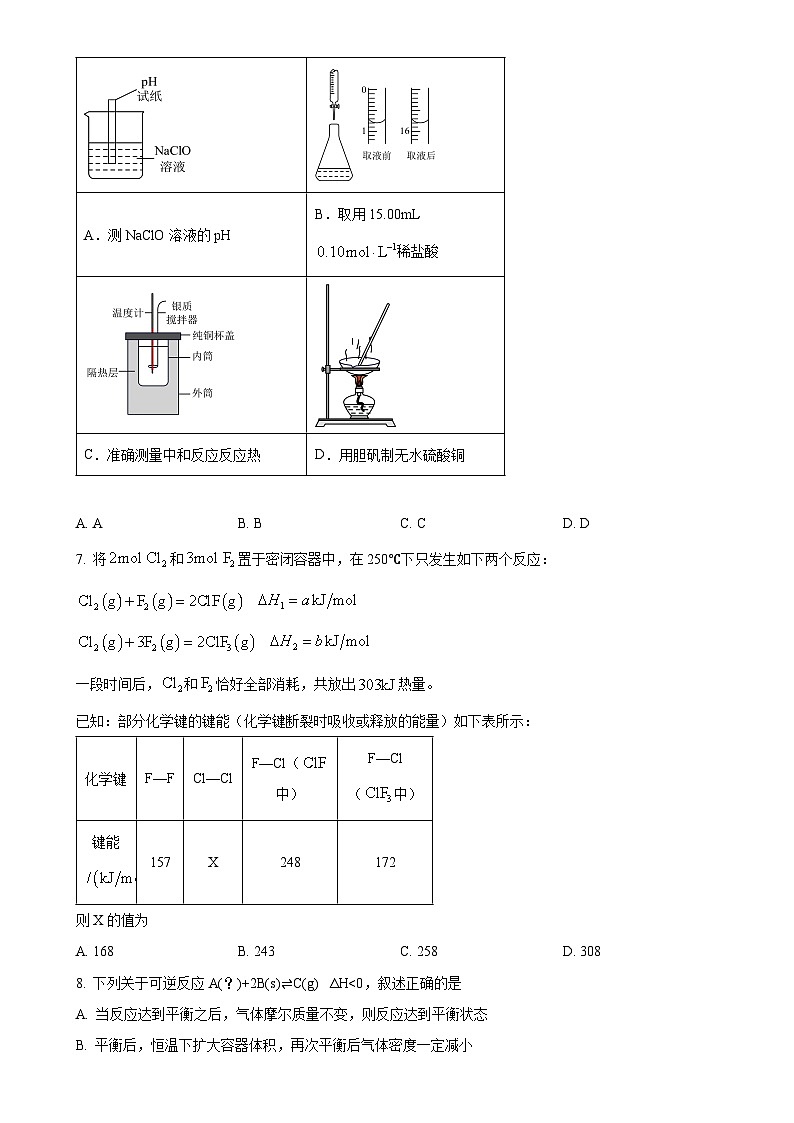
6. 下列实验中,能达到实验目的的是
A. AB. BC. CD. D
7. 将和置于密闭容器中,在250℃下只发生如下两个反应:
一段时间后,和恰好全部消耗,共放出热量。
已知:部分化学键的键能(化学键断裂时吸收或释放的能量)如下表所示:
则X的值为
A. 168B. 243C. 258D. 308
8. 下列关于可逆反应A(?)+2B(s)⇌C(g) ΔHv逆
C. 恒容下,再充入一定量的Ar气,平衡向正反应方向移动
D. 恒容下,再充入一定量的CH2=CH2(g),CH2=CH2(g)的平衡转化率增大
12. 向稀氨水中分别加入①蒸馏水、②NH3、③NH4Cl(s),并维持室温,相关判断正确的是
A. 加入①之后,的电离平衡得到促进,减小
B. 加入②之后,的电离平衡正向移动,电离程度增大
C. 加入③之后,增大,维持不变
D. 升高温度,的电离平衡得到促进,减小
13. 时,用溶液分别滳定的盐酸和醋酸溶液、滴定曲线如图所示。下列说法正确的是
A. 时,电离常数
B. a点时混合溶液中
C. d点时,曲线Ⅰ与曲线Ⅱ消耗NaOH的体积为曲线Ⅰ>曲线Ⅱ
D. a、b、c三点溶液中由水电离出的大小顺序为
14. 恒温条件下,将酸性溶液和溶液混合,发生反应:。用浓度的变化表示的反应速率随时间的变化关系如图所示。下列说法不正确的是
A. 时间段消耗的比时间段消耗的少
B. 与时刻的相等
C. 反应速率逐渐增大的原因可能是生成的起催化作用
D. 随着反应进行,溶液中减小
15. 一定温度下,在恒容密闭容器中充入1ml草酸镁,发生反应:。下列叙述正确的是
A. 当混合气体中CO体积分数不变时不一定达到平衡状态
B. 平衡时充入0.1ml CO和0.1ml达到新平衡时浓度大于原平衡
C. 平衡时充入氩气,正反应速率大于逆反应速率
D. 如果分离平衡向正反应方向移动,平衡常数增大
16. 温度为T时,在三个起始体积均为1L的密闭容器中发生反应:。达到平衡时,下列说法不正确的是
A. 容器Ⅰ中SO2的转化率小于容器Ⅱ中SO2的转化率
B. 容器Ⅰ中放出的热量为177.3kJ
C. 平衡时SO3的物质的量:a>1.8,b>1.8
D. 容器Ⅱ的平衡常数大于容器Ⅲ中的平衡常数
二、非选择题:(本题共3小题,每空2分,共52分)
17. 回答下列问题。
Ⅰ.和CO是常见的环境污染气体。
(1)对于反应来说,“”可作为此反应的催化剂。其总反应分两步进行:第一步为;则第二步为_______(写方程式)。已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能_______(填“大于”“小于”或“等于”)第二步反应的活化能。
Ⅱ.三氧化钼()是石油工业中常用的催化剂,也是瓷轴药的颜料,该物质常使用辉钼矿(主要成分为)通过一定条件来制备,回答下列相关问题。
已知:
①
②
③
(2)则的_______(用含、、的代数式表示)。
(3)若在恒温恒容容器中加入一定量,仅发生反应
①下列说法正确的是_______(填字母)。
a.气体的密度不变,则反应一定达到了平衡状态
b.气体的相对分子质量不变,反应不一定处于平衡状态
c.增加的量,平衡正向移动
②达到平衡时(g)的浓度为1.4,若时充入一定量的(g),到反应再次达到平衡,请在下图中画出-时间段(g)的浓度与时间的关系图_______。
(4)在2L恒容密闭容器中充入1.0ml (g)和1.5ml (g),若仅发生反应:,5min后反应达到平衡,此时容器压强为起始时的80%,则0~5min内,(g)的反应速率为_______
。
(5)在恒容密闭容器中,加入足量的和,仅发生反应:
。测得氧气的平衡转化率与起始压强、温度的关系如图所示。
①_______(填“>”“<”“=”)0;比较、、的大小:_______。
②若初始时通入7.0ml ,为7.0MPa,则A点平衡常数_______(用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,写出计算式即可)。压强为,温度为1100K时,平衡常数_______(填“>”“<”“=”)。
18. 研究小组利用溶液和酸性溶液的反应来探究外界条件改变对化学反应速率的影响,实验如下:
回答下列问题:
(1)通过实验①、②,可探究___________的改变对反应速率的影响,其中___________。
(2)通过实验___________(填实验序号)可探究温度变化对化学反应速率的影响,由实验②中数据可知___________。
(3)实验过程中,发现反应开始一段时间溶液褪色不明显,不久后迅速褪色。甲同学认为是反应放热导致溶液温度升高所致,重做实验②,测定反应过程中不同时间温度,结果如下:
①结合实验目的与表中数据,得出的结论是___________。
②你猜想可能是___________的影响。若证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的最佳试剂是___________(填标号)。
A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
19. 表格是几种常见弱酸的电离平衡常数(25℃),回答下列各题。
(1)可以证明醋酸是弱酸的事实是 ___________(填字母序号)。
A.醋酸和水能以任意比例混溶
B.在醋酸水溶液中还含有未电离的醋酸分子
C.醋酸与Na2CO3溶液反应放出CO2气体
D.1ml⋅L﹣1的醋酸水溶液能使紫色石蕊溶液变红色
E.等体积等pH醋酸和盐酸分别与足量氢氧化钠溶液充分反应,醋酸消耗的氢氧化钠更多
(2)结合表中给出电离常数回答下列问题:
①上述四种酸中,最强、最弱的酸分别是___________、___________(用化学式表示)。
②下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是 ___________。
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体 D.加少量冰醋酸 E.加氢氧化钠固体
③依表格数据判断醋酸和次氯酸钠溶液能否反应,如果不能反应说出理由,如果能发生反应请写出相应的离子方程式 ___________。
(3)已知草酸是一种二元弱酸,其电离常数K1=5.4×10-2,K2=5.4×10-5,试从电离平衡移动的角度解释K1>K2的原因___________。
(4)已知水溶液中c(H+)和c(OH﹣)的关系如图所示:
①图中A、B、C、D四点对应的水的离子积常数由大到小的顺序是 ___________。
②若A点到E点,可采用的措施是 ___________(填序号,下同);促进水的电离平衡正向移动的措施是 ___________。
A.测NaClO溶液的pH
B.取用15.00mL稀盐酸
C.准确测量中和反应反应热
D.用胆矾制无水硫酸铜
化学键
F—F
Cl—Cl
F—Cl(中)
F—Cl(中)
键能
157
X
248
172
容器编号
容器类型
起始物质的量/ml
平衡时SO3的物质的量/ml
SO2
O2
SO3
Ⅰ
恒温恒容
2
1
0
1.8
Ⅱ
恒温恒压
2
1
0
a
Ⅲ
绝热恒容
0
0
2
b
实验序号
实验
温度/K
参加反应的物质
溶液颜色褪至无色时所需时间/s
溶液(含硫酸)
溶液
V/mL
c/ml·L
V/mL
c/ml·L
V/mL
①
290
2
0.02
4
0.1
0
6
②
2
0.02
3
0.1
8
③
315
2
0.02
0.1
1
时间/s
0
2
4
6
8
10
温度/K
290
291
291
291.5
292
292
酸
CH3COOH
HNO2
HCN
HClO
电离平衡常数(Ka)
18×10-5
4.6×10-4
5×10-10
3×10-8
相关试卷
这是一份安徽省芜湖市第一中学2024-2025学年高二上学期期中考试 化学试题(解析版)-A4,共17页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份浙江省星辰联盟2024-2025学年高二上学期11月期中考试化学试题(原卷版)-A4,共7页。试卷主要包含了考试结束后,只需上交答题纸等内容,欢迎下载使用。
这是一份重庆市万州第二高级中学2024-2025学年高二上学期11月期中考试化学试题(原卷版)-A4,共7页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。








